聚焦超声(Focused Ultrasound,FUS)作用下的微泡 (microbubble)已被证明能够通过一种称为超声抗血管(antivascular ultrasound)或非热消融(nonthermal ablation)的方法在一系列组织类型中诱导血流停止和周围组织坏死[1-2]。在肿瘤学中,当与传统的化疗、放疗或免疫疗法相结合时,这种方法已经证明了抑制肿瘤生长和协同抗肿瘤作用。然而,虽然超声抗血管治疗最近已开始出现在临床试验中,但其在微血管尺度下的生物学效应和相关的微泡-血管相互作用仍然相对未被探索。迄今为止超声抗血管的众多研究所采用的治疗参数不统一,且作用机制仍不明晰,涉及的基本问题包括超声参数、针对的血管类型和大小,以及微泡本身发挥的作用及其导致血管损伤的空化声波特性都不明朗,这都阻碍了标准治疗方案的建立。
该研究将超声抗血管的相关参数应用于裸鼠脊背视窗(Dorsal window),利用双光子显微镜(two-photon microscopy)和空化监测 (cavitation monitoring)实时监测其血管效应,并将观察到的血管事件与已识别的空化特征结合起来,可以在微观尺度上更好地理解抗血管超声的机理。
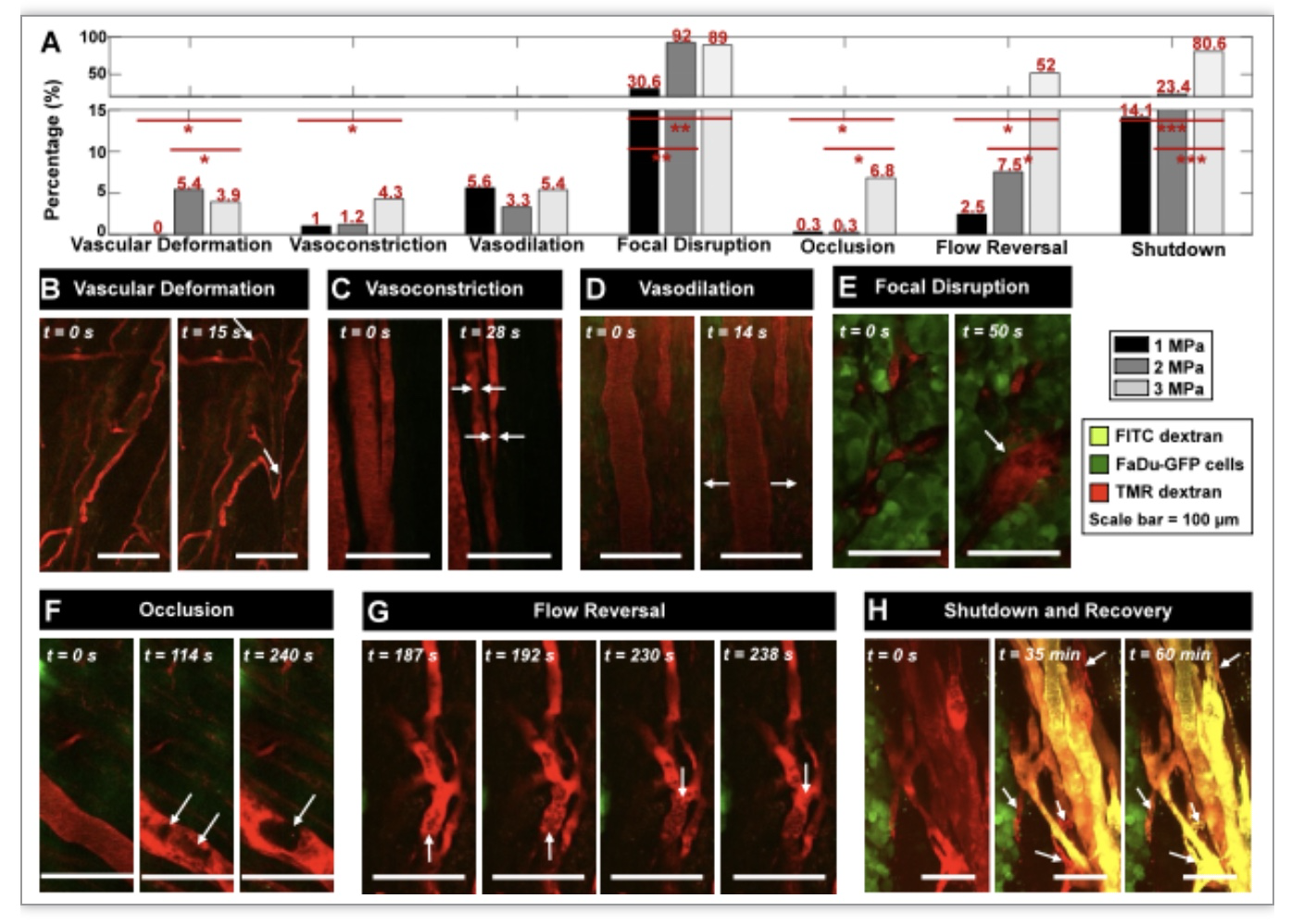
在此项研究中,超声发射器和接收器被集成到裸鼠脊背视窗模型(分为肿瘤组和正常组)中,用于活体显微镜研究。在裸鼠静脉内注射红色荧光染料(tetramethylrhodamine)和 Definity 微泡后,采用不同强度的超声抗血管治疗(1、2、3 MPa),在治疗期间和之后定期监测血管效应,在治疗后的30分钟时间点注入绿色荧光染料(fluorescein isothiocyanate)继续成像,以区分堵塞的血管并评估一小时后潜在的血管恢复情况。图像分析量化了受治疗影响的堵塞血管大小,并且将采集到的空化信号做傅里叶分析并与微泡行为和治疗效果相关联。该研究发现了治疗过程中血管移位, 扩张, 收缩,局部破坏,血液倒流, 闭塞以及停止等一系列血管效应(图1)。 这些效应优先发生在受肿瘤影响的血管中,且在较小的血管中和血管分叉处发生率更高,并且随着超声能量的增加而变得更严重。
图1 多光子显微镜下超声抗血管治疗下的不同血管效应
(图源:Zhao X et al., Theranostics, 2023)
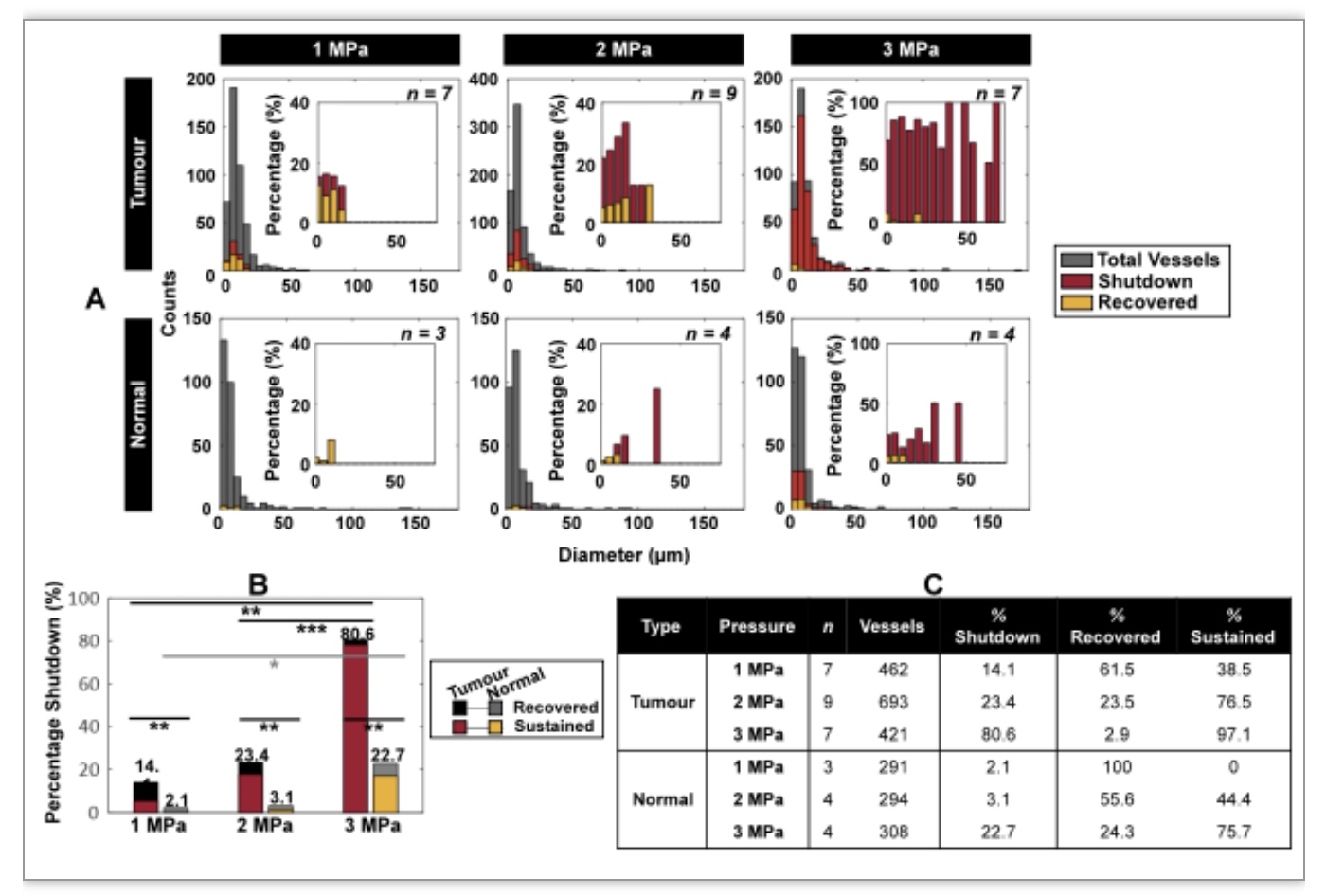
在治疗过程中最明显的血管效应是局部破环(focal disruption),在这篇文章中也被引述为渗漏(leakage),常常伴随着之后的血流停止。渗漏和血流停止都首发于小直径血管, 随着超声强度的增强逐渐影响到更大更多的血管;血流恢复则首发于低压强和小直径血管。同样的规律对正常血管受用,但相比于受肿瘤影响的血管整体发生率要低 (图2)。
图2 肿瘤血管和正常血管在超声抗血管治疗下的血流停止和恢复
(图源:Zhao X et al., Theranostics, 2023)
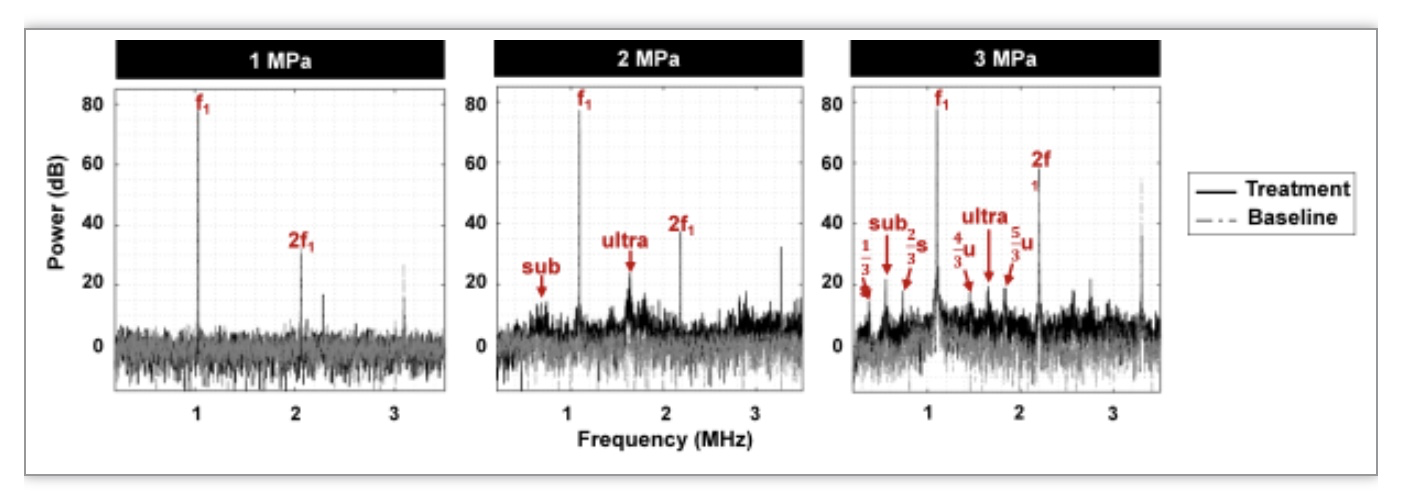
在治疗过程中声信号被检测,其空化信号于血管停止相关联。随着超声能量的增加,收集的空化信号显示出更高的宽带噪声(broadband noise)和明显的次谐波和超谐波 (sub- and ultra-harmonics)及其相关的三阶峰值(图3)。
(图源:Zhao X et al., Theranostics, 2023)
综上所述,这项研究创新性的通过治疗前后注射两种不同荧光染料,将多光子显微镜下观察到的超声血管摧毁术下的血管现象与其独特的空化特征相结合,有助于促进对此项治疗的微观机制的理解,对建立有效的特定治疗方案和控制系统具有重要意义。