非酒精性脂肪肝(nonalcoholic fatty liver disease,NAFLD)是慢性肝病的最主要原因之一。非酒精性脂肪肝可发展为非酒精性脂肪肝炎(nonalcoholic steatohepatitis,NASH),大约40%的NASH患者不可避免地出现严重的并发症,如纤维化、肝硬化和肝癌 [1,2]。NAFLD和NASH并非两种不同的疾病,而是以渐进式炎症反应为特征的一个连续体。然而,这种渐进式纤维化发展的病因在很大程度上仍未研究清楚。目前还没有一种药物被美国食品和药物管理局(FDA)或欧洲药品管理局(EMA)批准用于治疗NASH。
有人认为CD4+辅助T细胞在NAFLD向NASH的发展过程中发挥了作用,但哪种T细胞极化状态是这种纤维化发展的特征仍不清楚。先前的研究一般基于少量预选的细胞因子对CD4+T细胞进行分类。因此,这些研究没有完全描述人类CD4+T细胞生物学的复杂性和它们在NASH中的潜在含义。此外,越来越多的证据表明,肠道微生物群不仅可能影响肝内T细胞的功能,而且在肝脏疾病(包括NASH)的发病机制中起着关键作用[3]。有人提出了肠道和肝脏之间的联系,即肠道-肝脏轴,是由NAFLD发展到NASH的原因。然而在同一患者队列中分析免疫系统和组织特异性微生物群组成的研究仍有待进行。CD4+T细胞在肠道-肝脏轴中的作用也值得更深入的研究。
该研究结合单细胞RNA测序(scRNA-seq)、多参数流式细胞仪分析以及肝脏和肠道样本的微生物组测序,首次提供了专注于NAFLD和NASH患者肝脏浸润性CD4+ T细胞的单细胞图谱并描述了患者肝脏和肠道的微生物组成。该单细胞图谱显示NASH的特点是有一群产生多细胞因子的CD4+T细胞。在这些细胞中,只有那些具有Th17极化状态的细胞在晚期纤维化患者中富集。同时,细菌在NASH患者的肠道中富集,并与产生多细胞因子的CD4+T细胞的频率相关。

为了详细描述NAFLD和NASH患者肝脏的CD4+T细胞,研究者们对分离自3名NAFLD(4421个细胞)和3名NASH患者(6435个细胞)的CD45RA-CD4+记忆T细胞进行了单细胞测序。
通过无监督的聚类分析和对比已有的肝脏细胞测序数据及流式数据,研究者鉴定了8个T细胞类群(图1左上)。常见的一些T细胞表面受体,转录因子和细胞因子的基因表达情况为各个类群的注释提供了更好的参照(图1右上)。在NASH患者的肝脏中发现的CD4+T细胞具有较低的组织驻留性转录特征,并表达一些通常由肠道T细胞表达的趋化因子的基因,暗示了可能的肠道-肝脏轴特征 。由于CD4+T细胞主要通过细胞因子执行调控功能,研究者比较了几种核心炎症细胞因子在NAFLD和NASH患者中的表达,分析了数据集中的细胞因子分泌细胞的频率。尽管患者样本数量比较少,但与NAFLD相比,NASH患者的CD4+T细胞共同表达TNF、IFNG、IL17A和IL10的细胞比例显得更高(图1下)。在NASH患者中发现的不同的CD4+T细胞群有一个整体的促炎性转录组特征,例如,共同表达多种促炎性细胞因子。
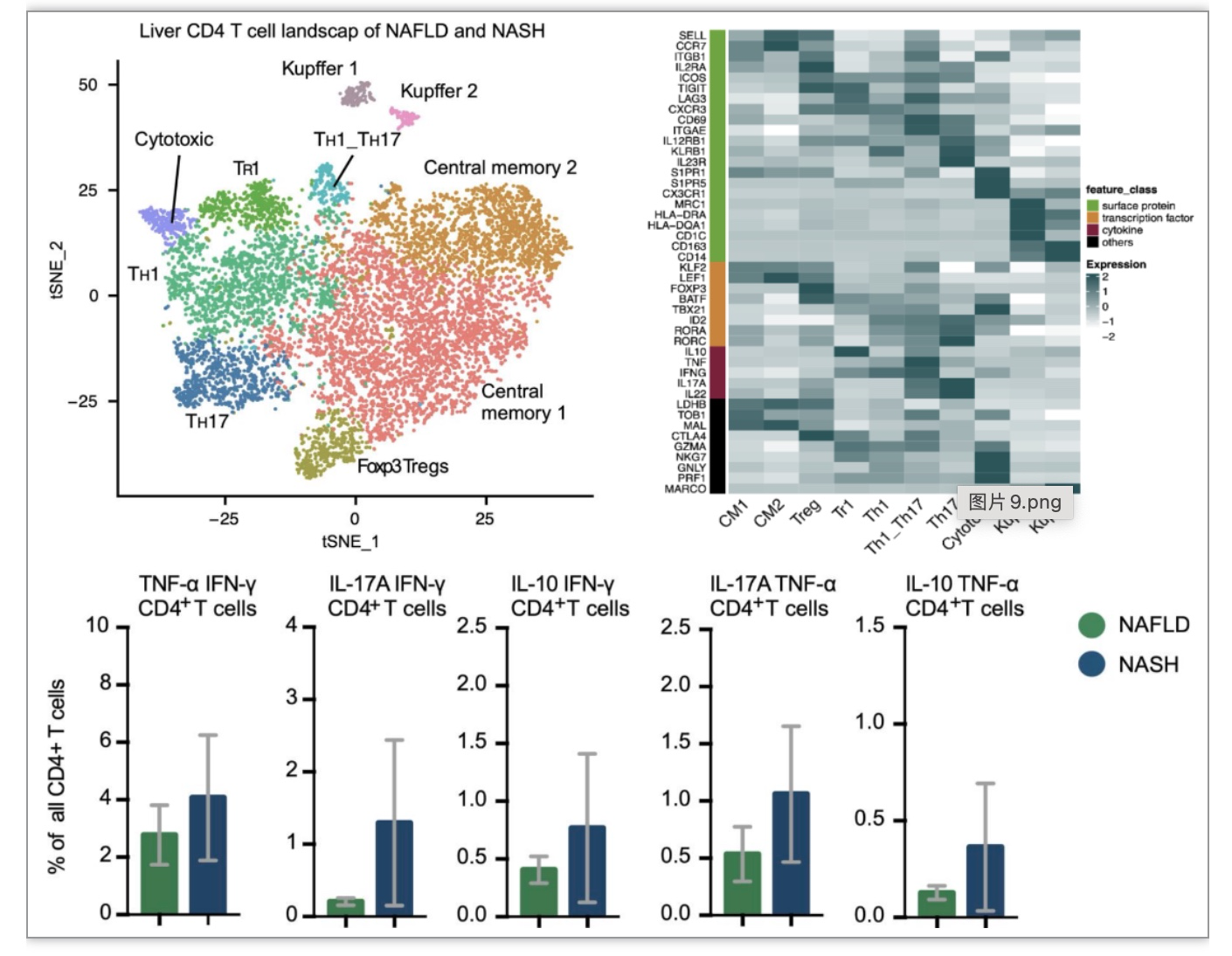
为了验证NASH患者肝脏能够产生多种细胞因子的CD4+T细胞频率比NAFLD患者高的现象,研究者又扩大了样本数量,对从26名NAFLD和39名NASH患者的肝脏中新鲜分离的CD4+T细胞进行了细胞因子FACS染色(图2A)。考虑到许多细胞因子组合可能发生,研究者进行了viSNE分析,以确定其中哪些确实存在于NAFLD或NASH患者的肝脏中(图2B)。研究者发现,与NAFLD患者相比,NASH的肝脏中产生多种因子的CD4+T细胞群明显富集(图2C)。
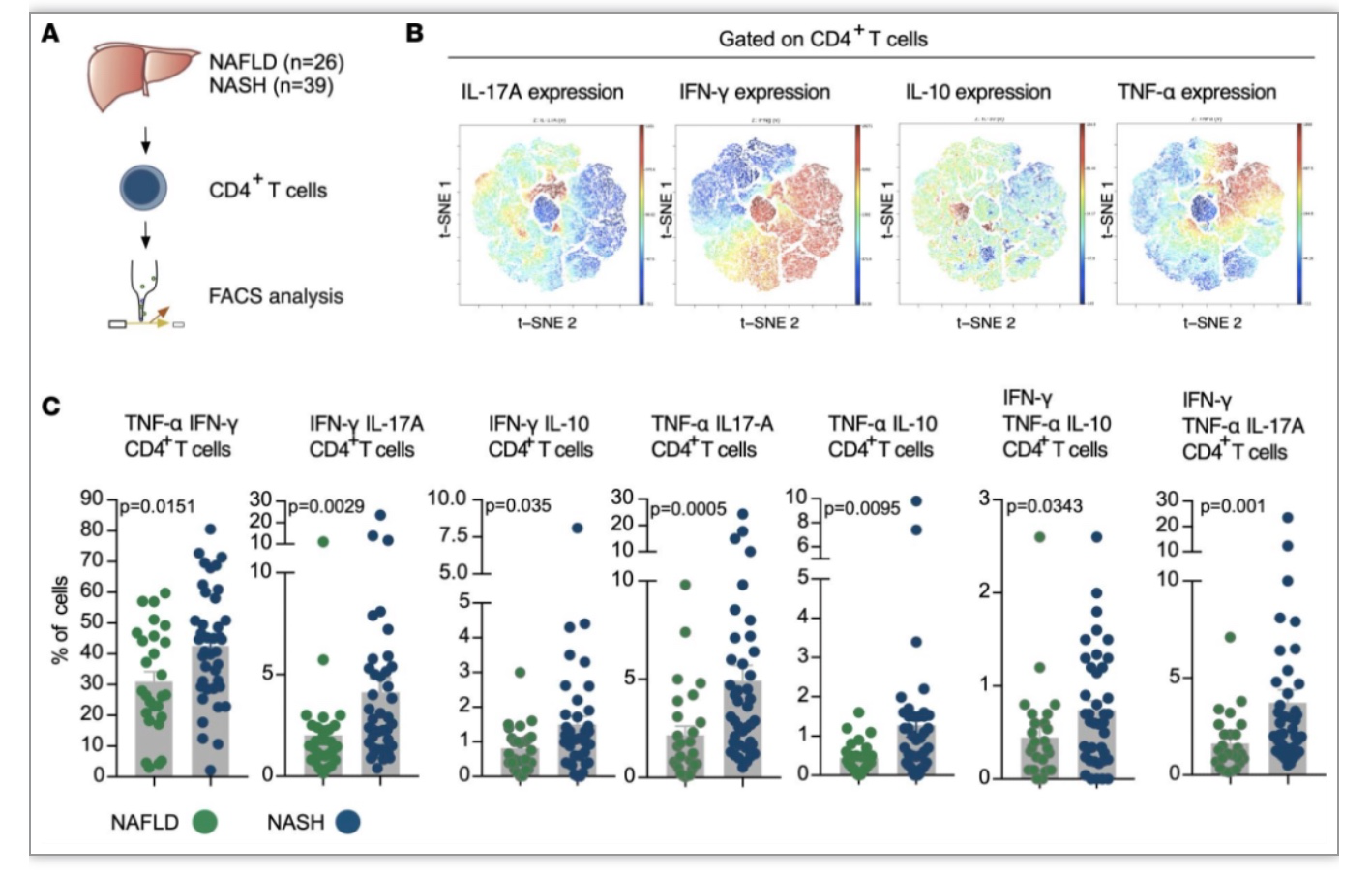
图2. NAFLD和NASH患者肝脏CD4+T细胞的细胞因子流式分析。
(图源:Woestemeier A, et al., JCI Insight, 2023)
接下来,研究者想知道肝脏产生多因子的CD4+T细胞的频率是否与NASH患者的纤维化评分相关。在不同的产生多因子的CD4+T细胞中,研究者发现,与没有纤维化的NASH患者相比,主要产生IL-17A的CD4+T细胞(即具有Th17极化状态的CD4+T细胞)在肝脏中明显富集(图3 左)。此外,为了进一步证实研究者在不同患者群中的发现,研究者使用了一个已发表的NASH患者Bulk RNA测序数据集 [4],并发现IL17A和纤维化标记基因COL1A1的表达之间有显著的正相关性(图3 右)。研究者接下来还通过体外实验发现IL-17A可以激活成纤维细胞。
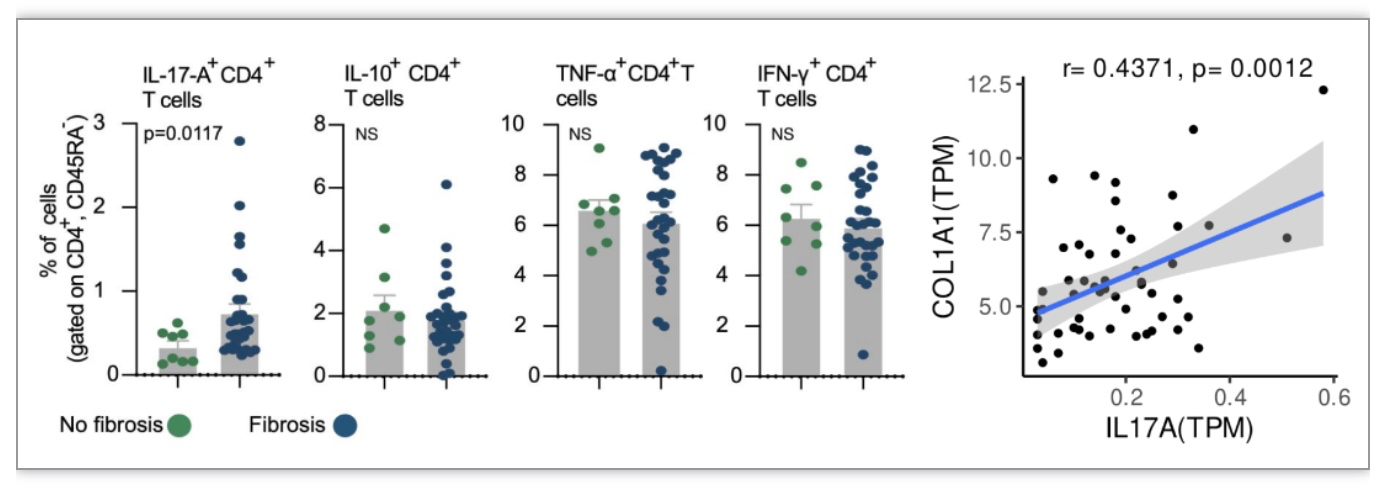
图3. NASH患者肝脏CD4+T细胞的细胞因子和纤维化程度相关性
(图源:Woestemeier A, et al., JCI Insight, 2023)
考虑到CD4+T细胞功能与肠道微生物群之间的已知联系 [5],研究者假说肝脏-肠道轴可能是肝脏T细胞过度激活的原因。为了支持这一点,研究者测试了(16s rDNA测序)NAFLD和NASH患者的肝脏(n = 50)和小肠(n = 19)微生物组(图4 左上)。研究者分析了配对的肝脏和小肠样本,发现一些细菌同时存在于患者的小肠和肝脏中(图4下)。肝脏组织中的细菌在NAFLD和NASH之间的属种丰度没有明显差异,然而在NASH患者的小肠中,Bacteroides明显富集(图4 右上)。该结果与以前通过对NASH患者的粪便进行测序所发表的结果一致 [6]。研究者希望能在以后的研究中进一步探索肠道细菌和肝脏CD4+T细胞激活的潜在相关性,为肝脏-肠道轴提供更多证据支持。
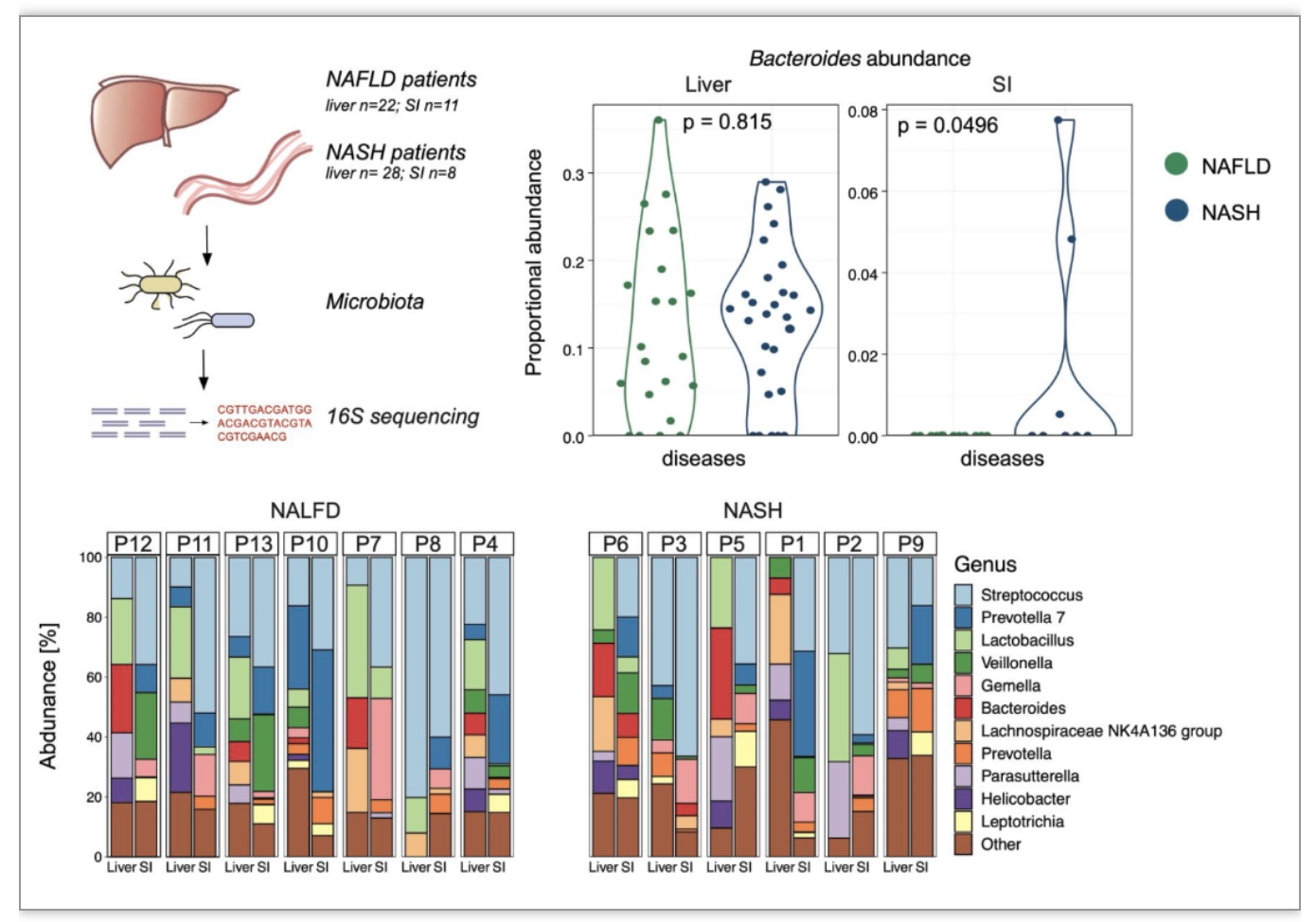
图4. NAFLD和NASH患者的小肠和肝脏微生物组分析
(图源:Woestemeier A, et al., JCI Insight, 2023)

