新型冠状病毒病(SARS-CoV-2)引起的感染在全世界范围内持续、大规模流行,已经造成了数亿人感染和数百万人死亡。作为单链RNA病毒,SARS-CoV-2一直处于快速变异的状态,先后出现了B.1.1.7 (Alpha)、B.1.351 (Beta)、P.1 (Gamma)、B.1.617.2 (Delta)和B. 1.1.529 (Omicron)等5种受关注的变异株(Variant of Concern, VOC)[1, 2]。这些变异株包含多种多样的突变位点,使病毒极易发生免疫逃逸从而给疫苗和中和抗体的有效性带来了极大的挑战。
针对病毒变异问题,研究人员筛选了靶向刺突蛋白(Spike, S)保守表位的中和抗体,但关键结合位点的突变仍可能导致活性丧失。在这一基础之上,研究人员又提出了将多种中和抗体联合应用的策略。然而,不管是靶向保守表位的抗体还是抗体组合,其广谱性的评价主要是基于现有的病毒,而病毒又处于快速突变之中,难以评估这些抗体或抗体组合对未来可能出现的SARS-CoV-2变异毒株的有效性。因此,开发一种可充分评估中和抗体广谱性的方法对SARS-CoV-2的治疗有积极意义。
为了评价这一模型的可靠性,作者首先从早期建立的SARS-CoV-2中和抗体库中筛选了靶向保守表位的抗体[3]。采用竞争ELISA法,作者绘制抗体表位信息,并将这些抗体分为了三组(图1a)。然后,作者以能否与SARS-CoV-1交叉结合及中和作为反映抗体保守活性的指标(图1b-c)。位于第1组的7G10、8G4、9E12、9D11、8C12、9A6等抗体对SARS-CoV-1具有较高的中和活性。作者还发现第1组和第3组抗体具有良好的ACE2竞争能力(图1d)。最后,作者从不同表位群选出了9E12、9D11、8G4、11F7、10D4、7B9、2G1这几个候选抗体,并构建了抗体组合。考虑到抗体组合在现实生产中的复杂性,作者还利用自主开发的BAPTS双抗平台设计了7B9-9D11, 10D4-8G4和10D4-11F7共3个双特异性抗体。
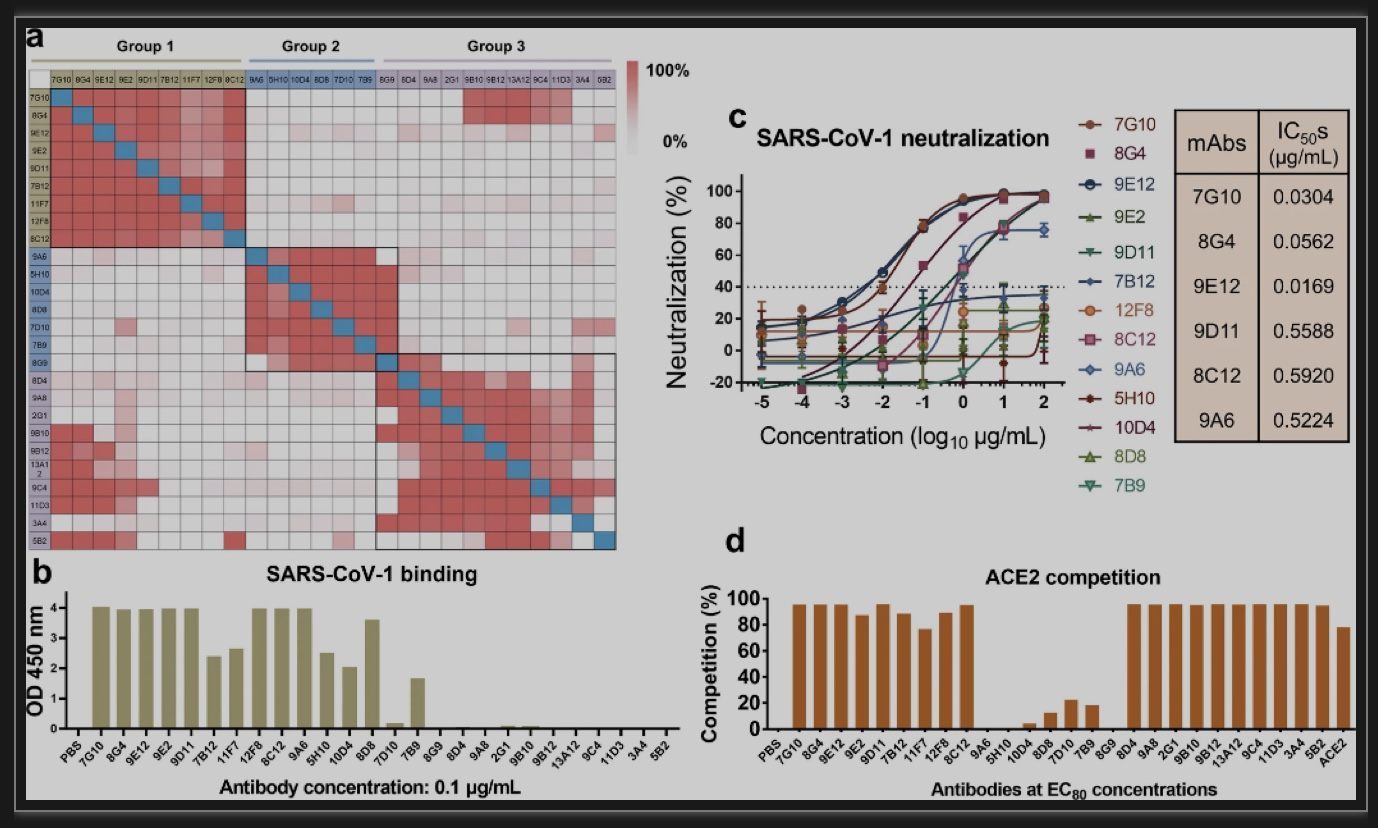
图1 从SARS-CoV-2中和抗体库中筛选保守表位抗体
(图源:Ma H, et al., Acta Pharmacol Sin, 2023)
VSV-SARS-CoV-2病毒可自我复制,并在复制过程中产生随机突变。根据这一特性,作者推测中和抗体的长期作用可能导致特定的、逃逸抗体中和的突变被选择性地保留下来,广谱性良好的抗体则难以发现逃逸突变。于是作者将VSV-SARS-CoV-2病毒在中和抗体存在的情况下进行长期传代,并通过观察病毒突破所需要的传代次数来初步判断抗体是否具有广谱中和能力(图2a)。对照抗体REGN10933在第3代就被病毒突破,保守性较好的单抗9E12可坚持到第9代,对于抗体组合,7B9-9D11+2G1可坚持到第30代,9E12+10D4+2G1可坚持超过33代不被突破(图2b)。这初步表明了具有保守表位的抗体,特别是抗体组合可大大增加对病毒变异的耐受性。
病毒的传播能力与其复制速度有关。随后,作者测试了这些突变病毒的复制速度,发现大多数病毒的复制速度相较于野生型WA1/2020病毒有所下降(图2c)。这提示尽管有些病毒突破了广谱中和抗体的保护,但却是以牺牲传播能力为代价,在现实世界中大流行的可能性较小。针对表现出良好耐受能力的两个抗体组合9E12+10D4+2G1和7B9-9D11+2G1,作者通过表面等离子体共振发现组合中的所有抗体都可以同时结合到S蛋白上,具有较高的开发价值(图2d)。
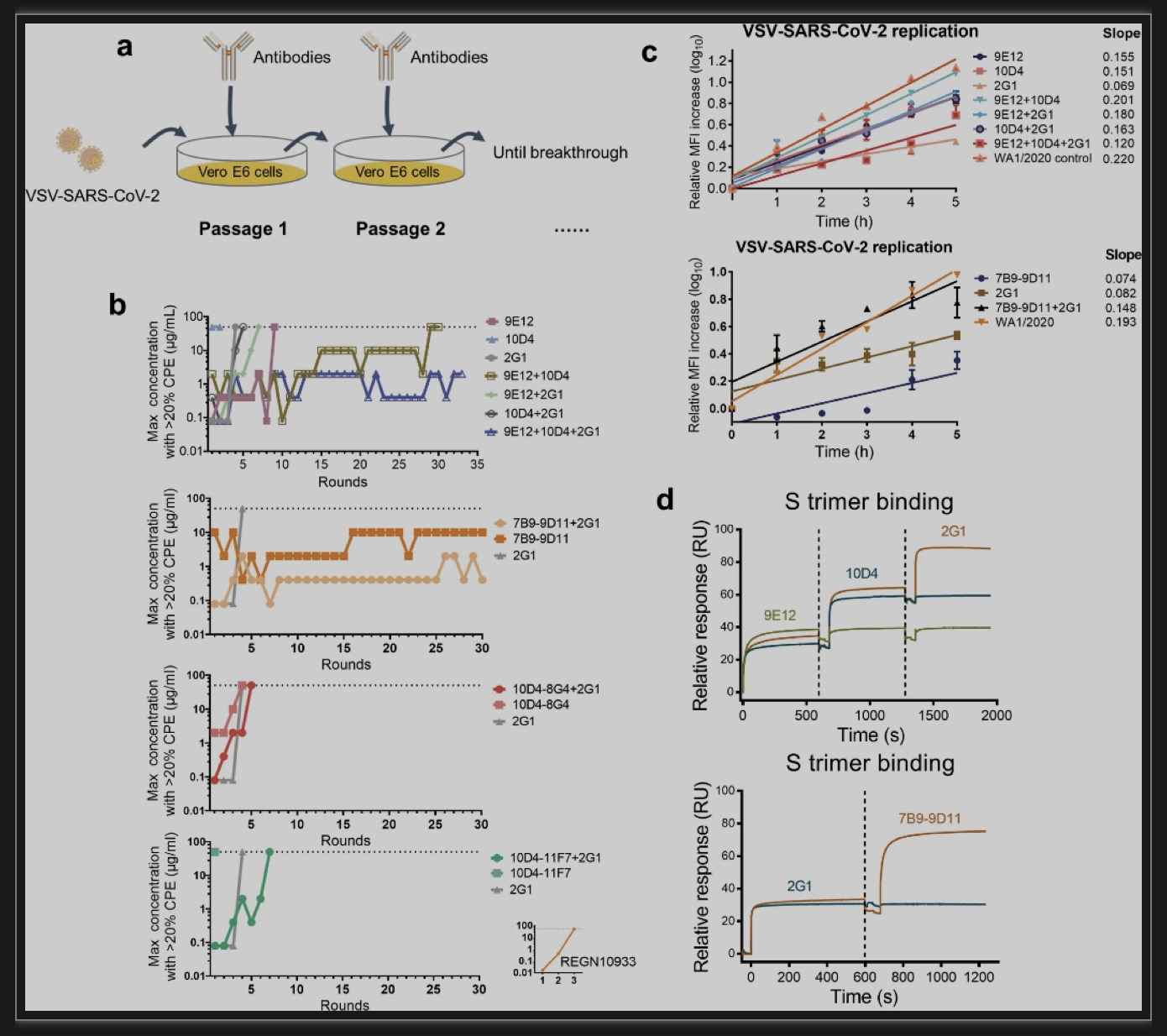
图2 通过长期传代评价抗体组合保护细胞免受VSV-SARS-CoV-2感染的能力
(图源:Ma H, et al.,Acta Pharmacol Sin, 2023)
病毒的S蛋白与细胞表面ACE2分子结合是病毒感染宿主的关键步骤。作者使用重组ACE2蛋白评估了这些突变病毒的ACE2敏感性,结果发现突变病毒的ACE2敏感性没有增加,反而在一些抗体组合中有所降低(图3)。由此作者推测在前面观察到的病毒复制速度下降可能是由于这些病毒突变之后ACE2亲和力降低。

图3 突破抗体保护的突变病毒的ACE2敏感性
(图源:Ma H, et al.,Acta Pharmacol Sin, 2023)
随后作者对这些突变病毒进行了深度测序,以确定病毒的逃逸位点。广谱性稍差的抗体10D4和2G1分别使病毒产生了一个突变,而广谱性较好的抗体9E12 则产生了三个突变,抗体组合产生的突变数量则更多(图4)。这表明病毒突破广谱性越强的抗体所需要产生的突变数量可能越多。
值得注意的是,抗体组合的突变位点并不是对应的单抗的简单叠加。这可能意味着SARS-CoV-2病毒逃逸抗体保护的突变方式远不止一种。此外,这些突变大多没有在已知的主要毒株中发现。这提示,即使一个抗体可以中和目前的所有,仍然可能有未知的突变方式逃逸其保护,基于现有突变株设计的抗体及组合仍需充分探索其广谱活性。

图4 深度测序鉴定突变病毒的逃逸位点
(图源:Ma H, et al.,Acta Pharmacol Sin, 2023)
使用SARS-CoV-2假病毒系统,作者测试了9E12+10D4+2G1和7B9-9D11+2G1两个广谱性较好的抗体组合对主要毒株的中和活性。结果显示,9E12+10D4+2G1和7B9-9D11+2G1均可以中和包括Omicron (BA.1)、SARS-CoV-1在内的所有主要毒株(图5)。这证实了作者开发出来的用于评价中和抗体广谱性的模型的可靠性。

图5 VSV-SARS-CoV-2模型筛选出的广谱抗体组合对主要SARS-CoV-2突变株的中和活性
(图源:Ma H, et al.,Acta Pharmacol Sin, 2023)

