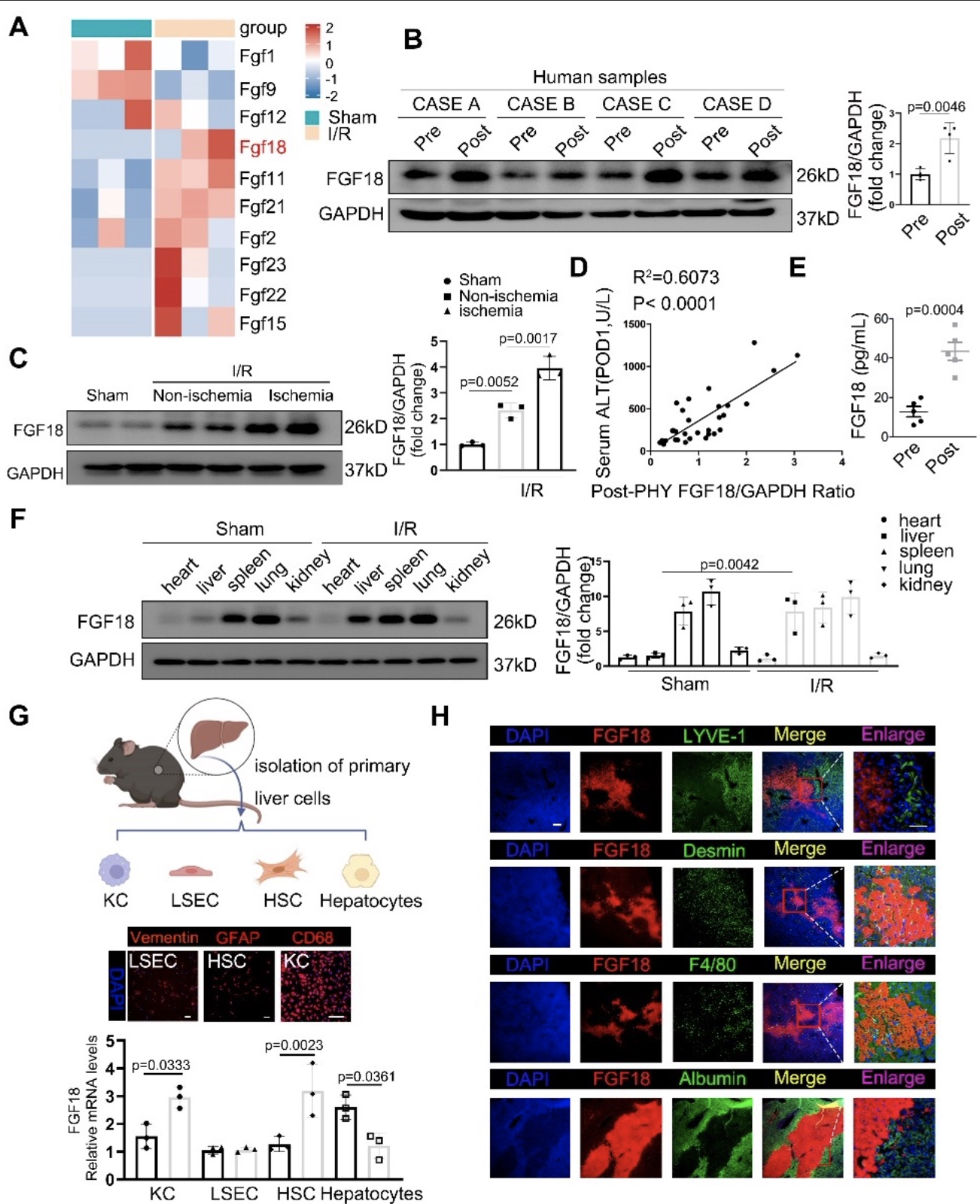
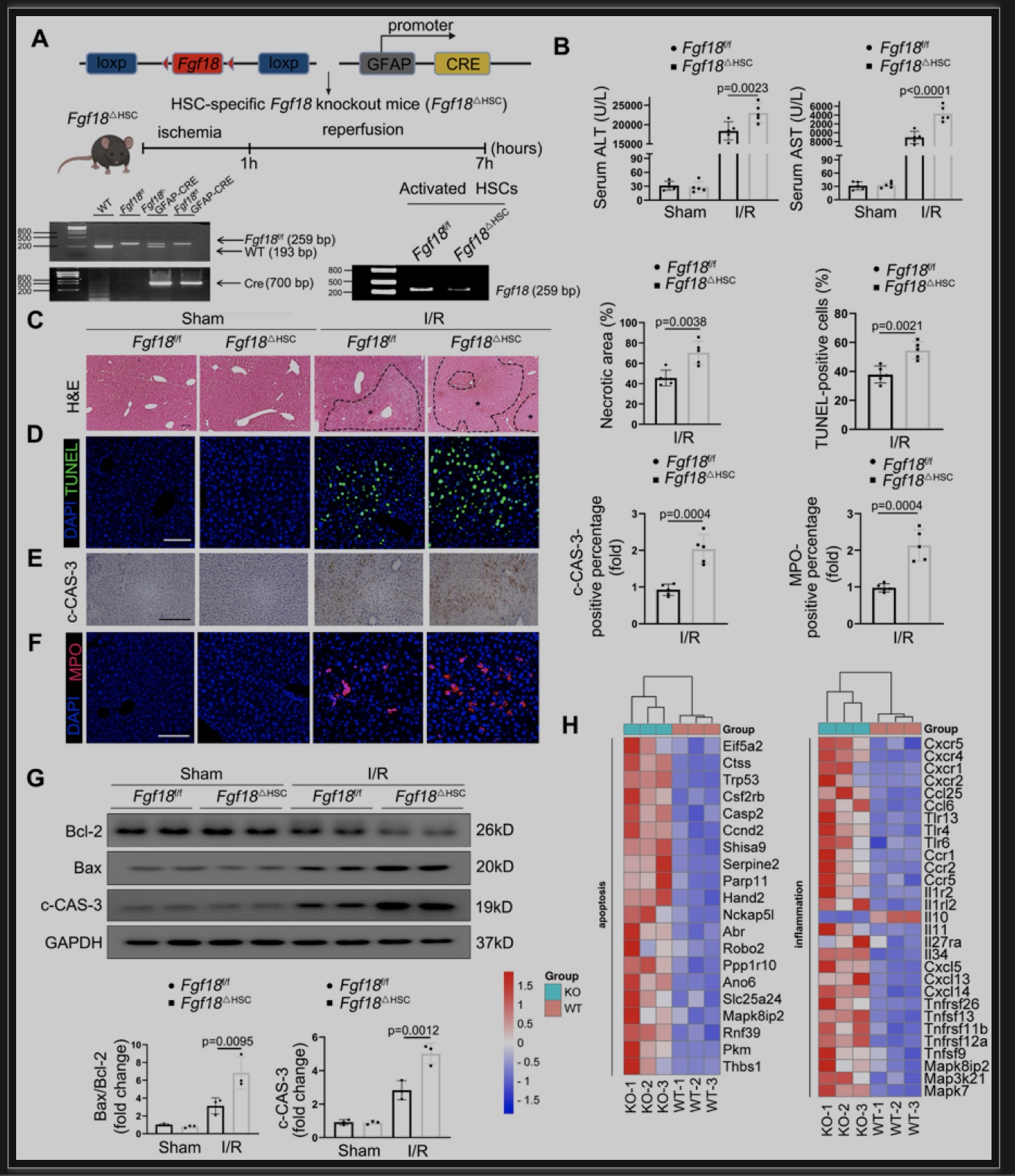
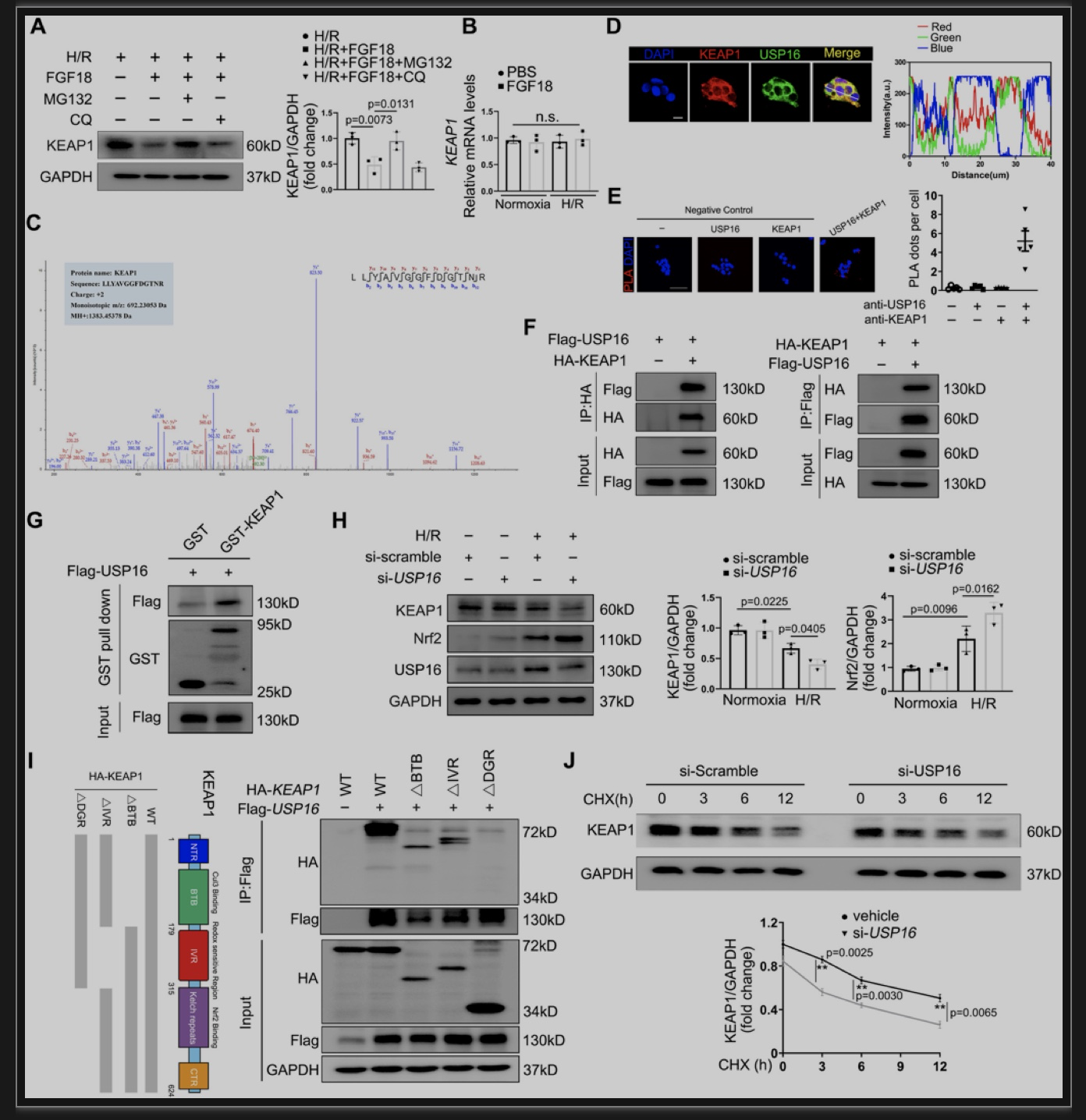
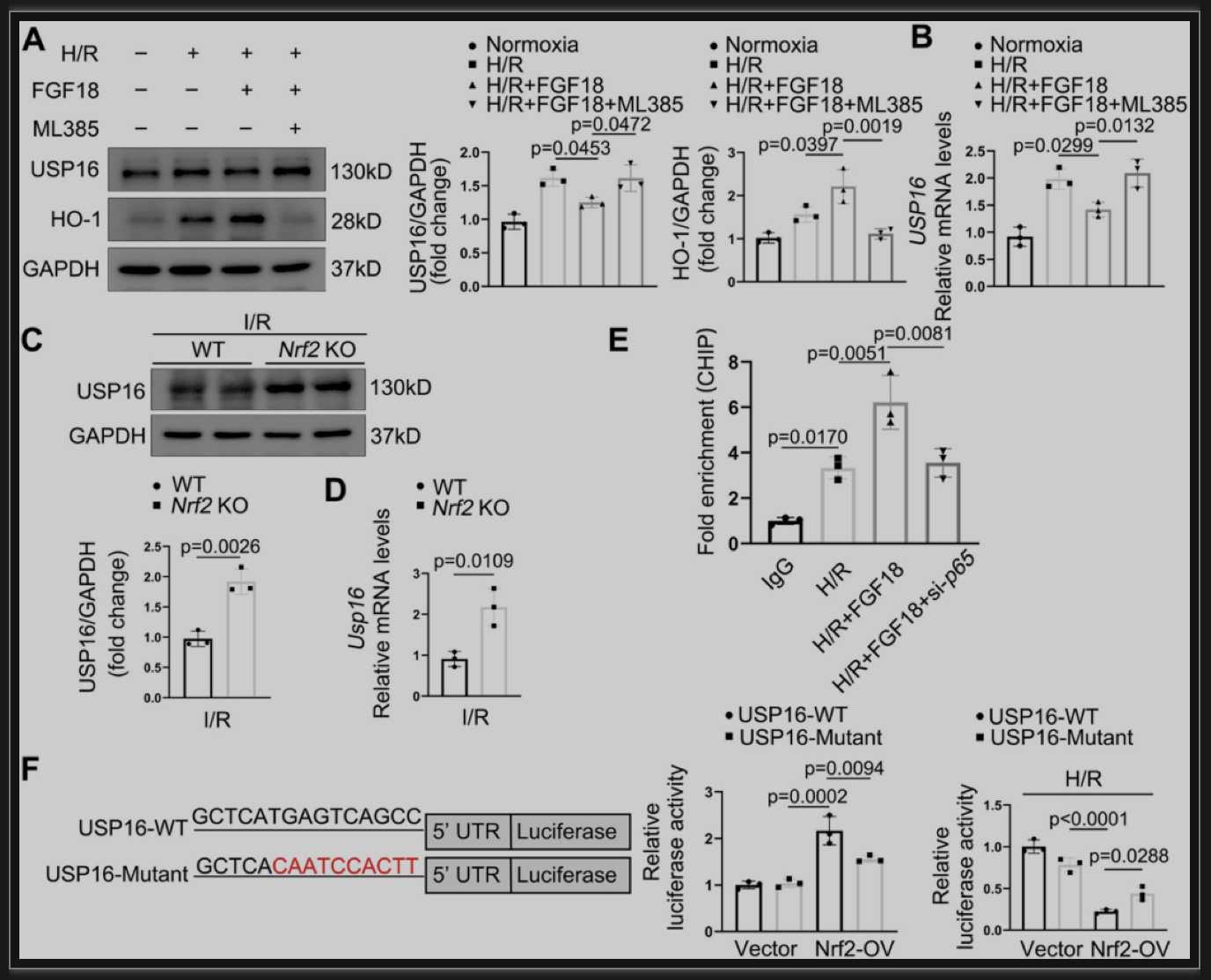
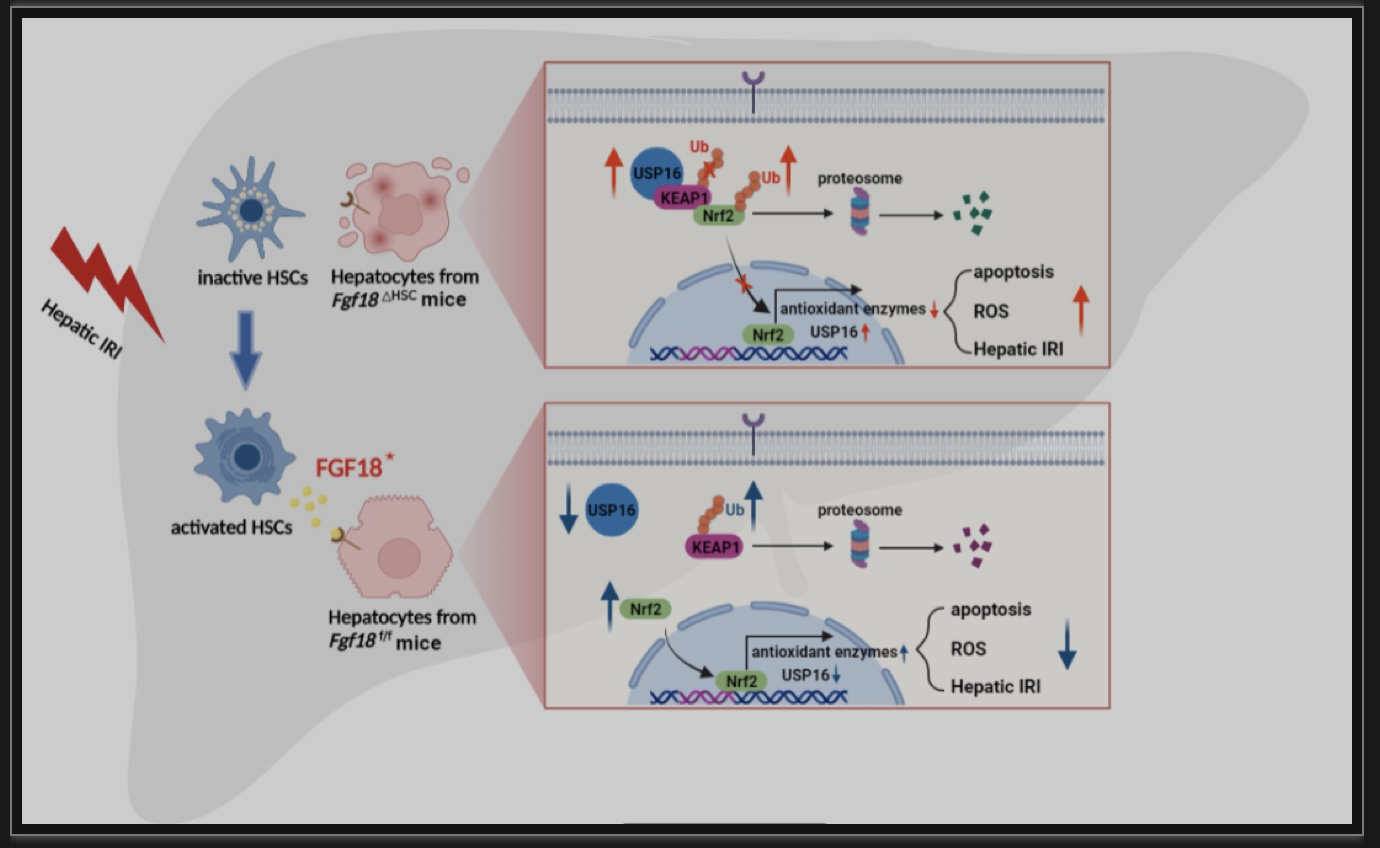
综上所述,本项研究的结果证实,FGF18在肝缺血再灌注过程中扮演关键作用,其可显著改善肝缺血再灌注过程中的损伤,主要体现在通过降低氧化应激以及炎症水平,最终减少肝实质细胞的凋亡。作者通过实验发现在缺血再灌注过程中,肝星状细胞可分泌FGF18并作用于肝实质细胞,从而保护肝实质细胞。从机制上来讲,FGF18的保护作用主要是通过下调USP16的表达,从而增加了KEAP1的泛素化修饰水平,进而激活Nrf2信号并最终改善肝脏缺血再灌注损伤。此外,作者发现FGF18对USP16调控作用是通过Nrf2和USP16的负反馈调控来实现的。因此靶向FGF18/USP16/KEAP1信号通路可作为临床上改善肝脏缺血再灌注损伤和相关病理过程的一种新策略。

