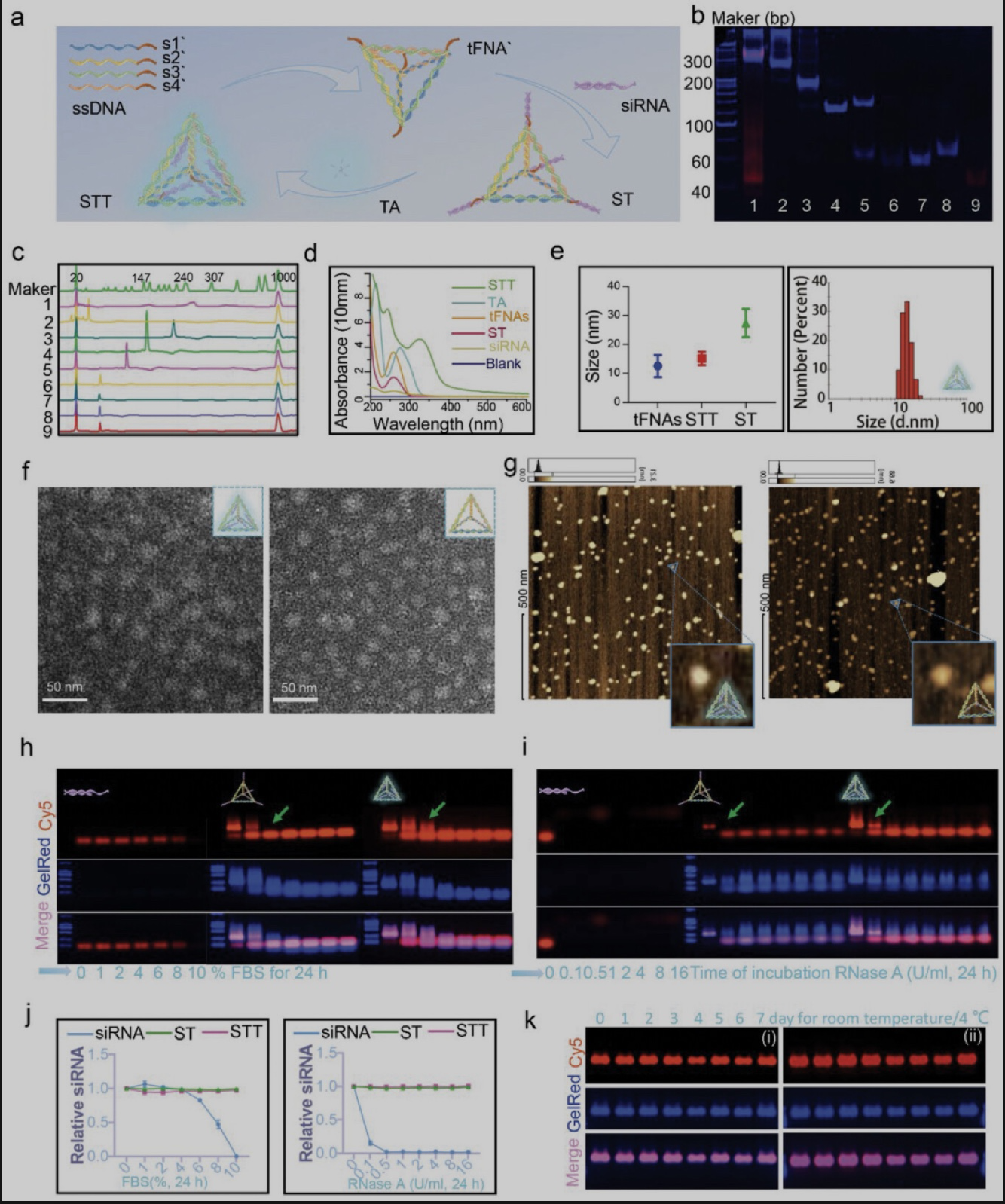
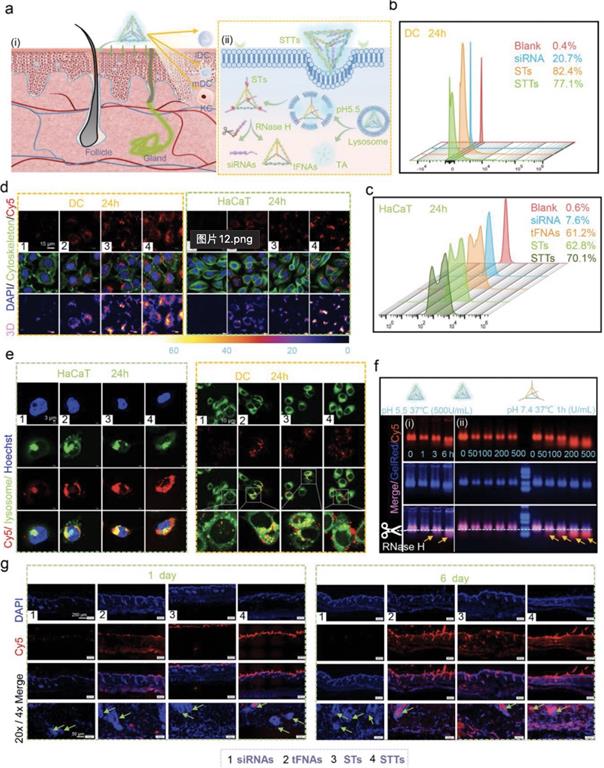
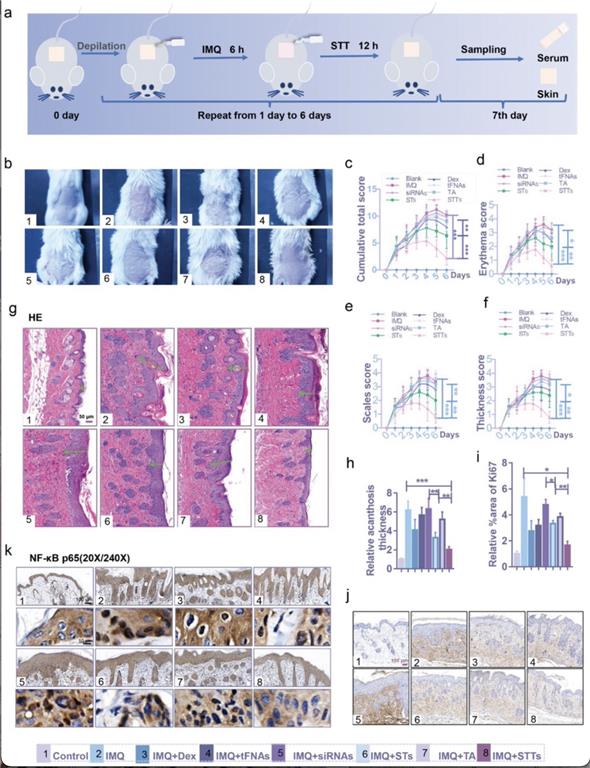
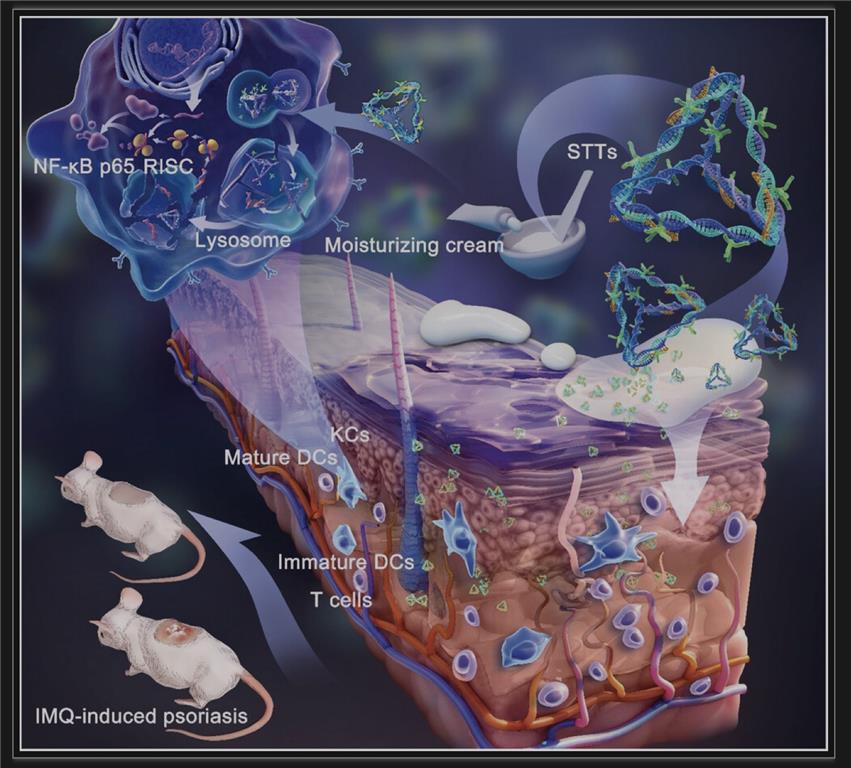
透皮基因疗法对于由皮肤屏障破坏和免疫紊乱引起的疾病非常有前途。作者最后介绍道,作为一种透皮RNAi药物,STT不仅具有良好的透皮和细胞摄取效率,而且确保了siRNA递送过程中的稳定性。STT特异性地沉默和抑制NF-κB信号的传递并抑制DC的成熟,从而影响关键细胞因子TNF-α和IL-23 / IL-17表达的变化,最终减少KCs的增殖。STT治疗牛皮癣基本上涉及皮肤的先天性和后天免疫力,在维持皮肤的免疫稳态方面起着强大的作用。STT的出现为疫苗接种、伤口愈合以及皮肤癌和其他皮肤病的治疗提供了新的前景。但是,该研究仍然有一些不足,文中揭示STT对于免疫相关的影响仅仅涉及到DC,关于进一步的T 细胞的变化分型还应做更深入的探讨。

