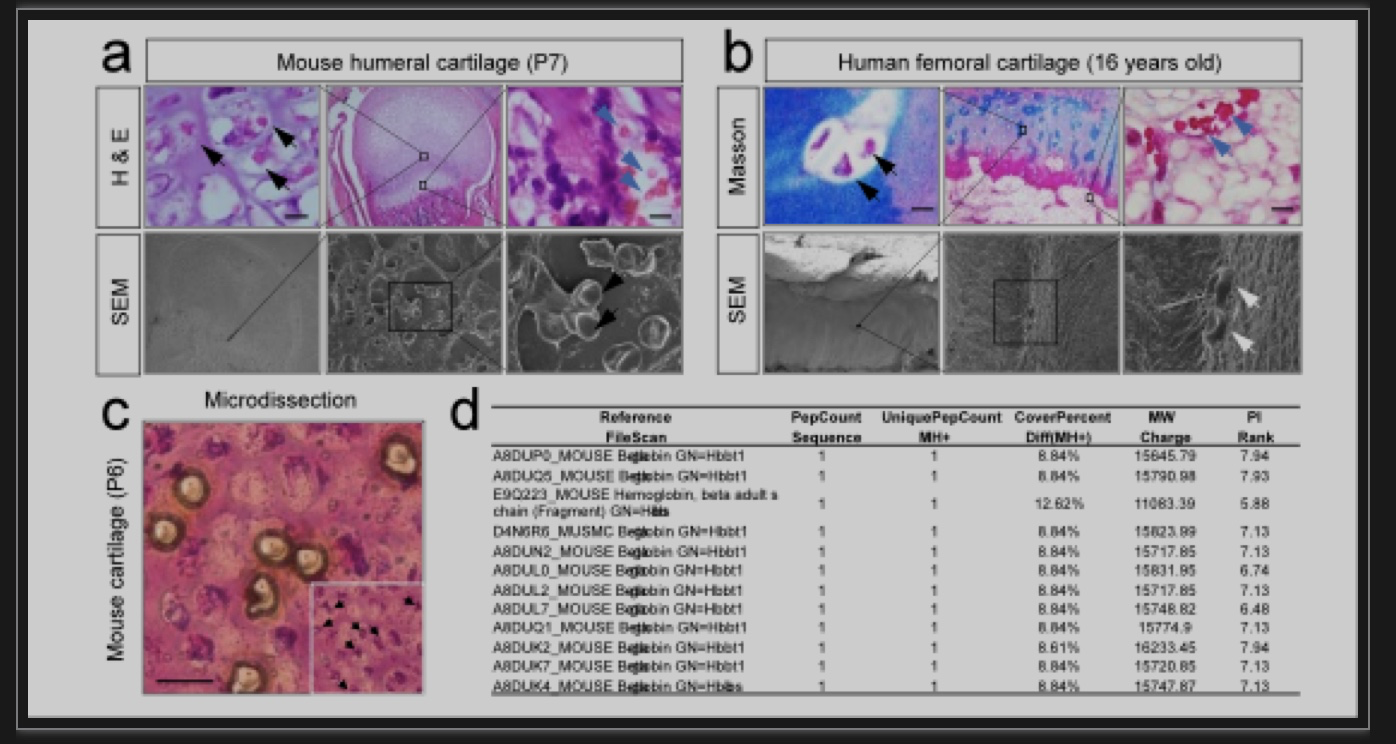
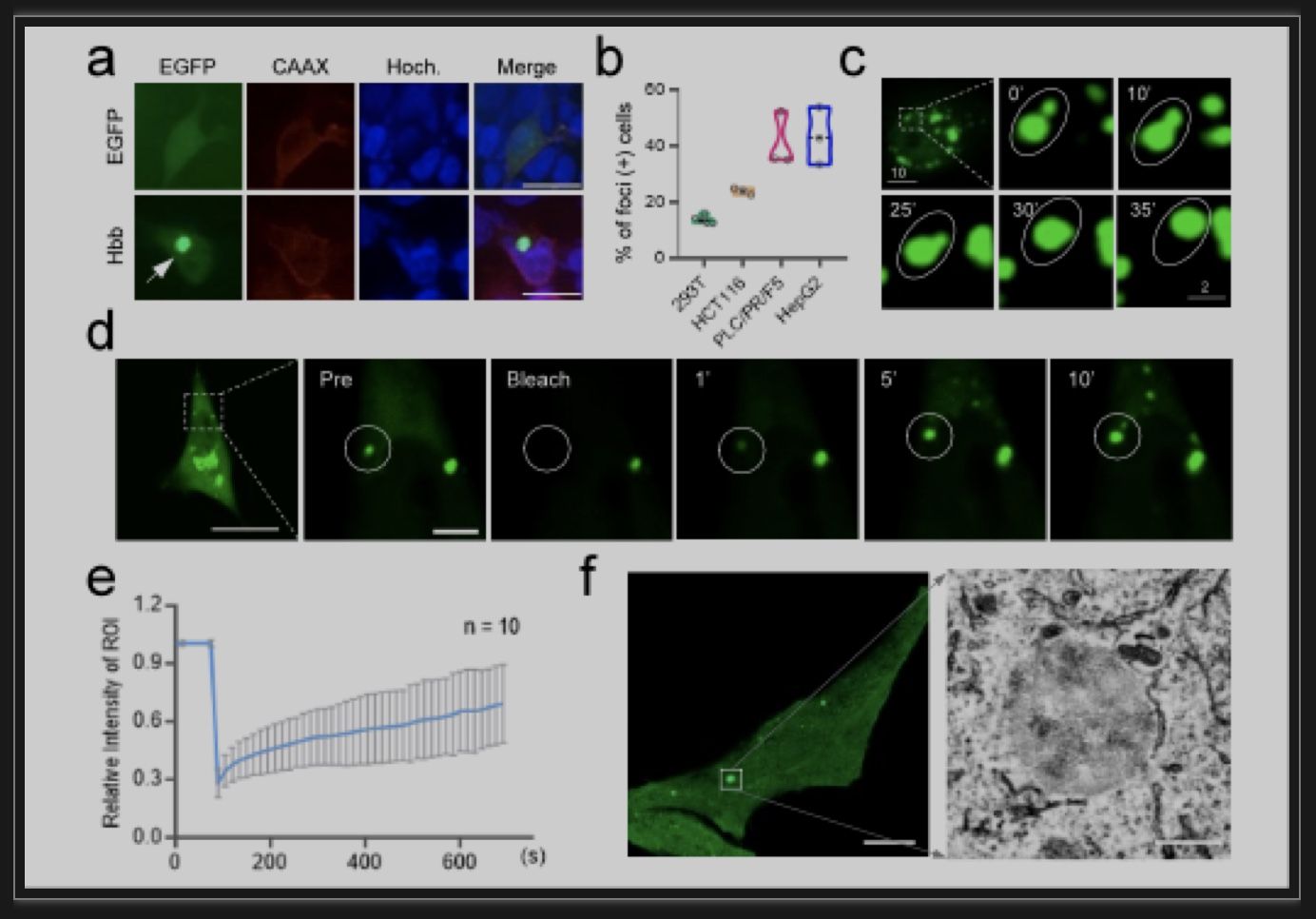
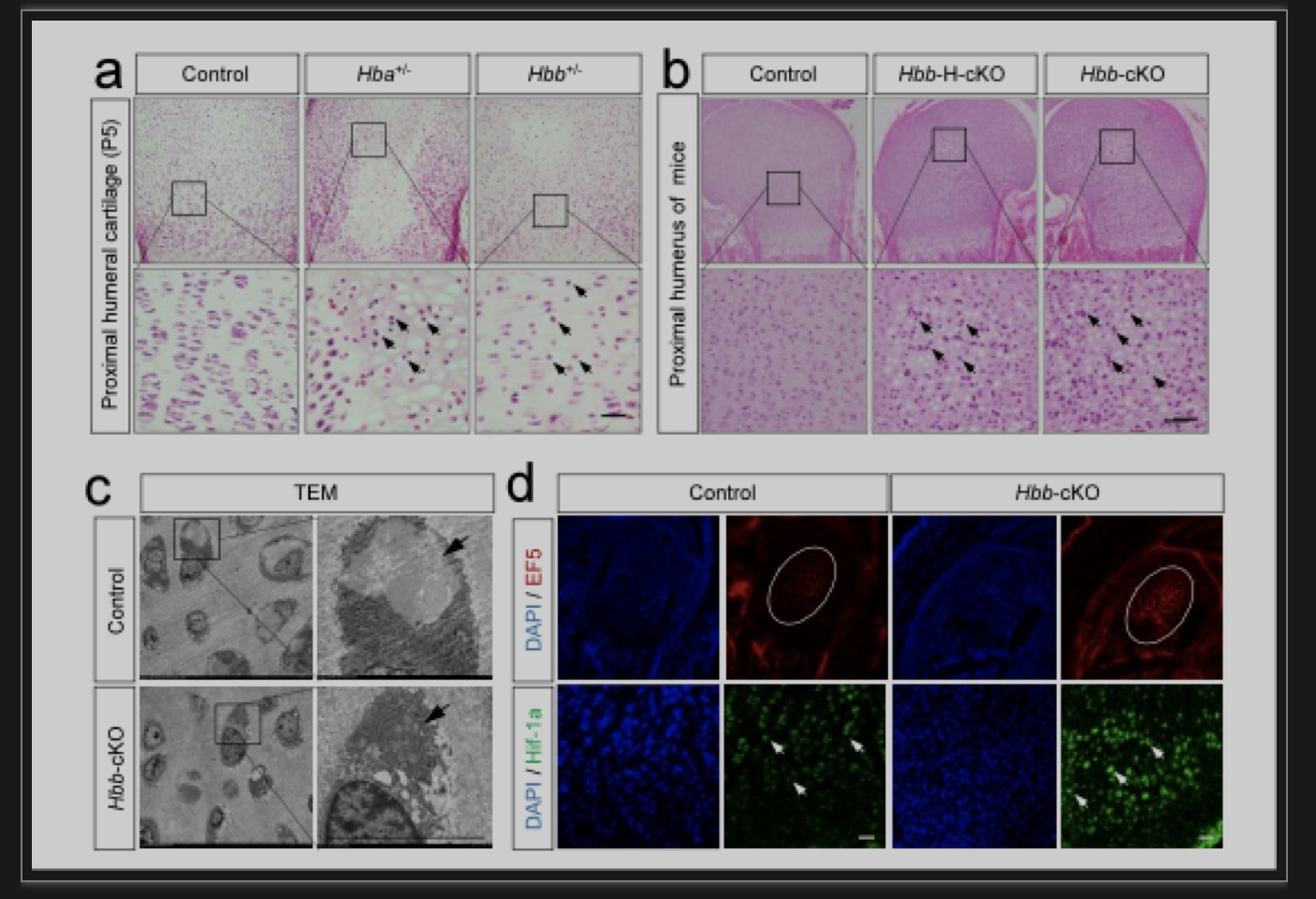
本研究阐明了软骨细胞维持细胞内氧稳态,适应缺氧环境的新机制,首次揭示了红细胞外血红蛋白在正常组织中发挥的重要生物学功能,而且发现了血红蛋白表达调控的新机制。与这些发现一致的是,地中海贫血综合征患者通常患有关节疼痛[10],贫血在患有软骨相关疾病的患者中也很常见,如类风湿性关节炎(RA,约30%至70%)[11,12]和软骨发育不全(约73%)[13]。此外,血红蛋白较低的RA患者表现出更严重的关节疾病[14],治疗贫血能显著缓解关节症状[15]。这提示软骨细胞中的血红蛋白可能在疾病过程中发挥着重要作用。另外,研究者发现了血红蛋白的液液相分离特性,首次发现了通过液液相分离机制血红蛋白可以形成具有生物学功能新的细胞结构-Hedy。当然血红蛋白在软骨中的亚基结合方式以及其他辅因子是否参与结构构成在此项研究中并未深入探讨,而且软骨细胞中的血红蛋白为何具有更强的氧气结合力,这与Hedy的形成是否有关?接受何种机制调节?这些问题仍有待进一步研究。

