

文章结论与讨论,启发与展望
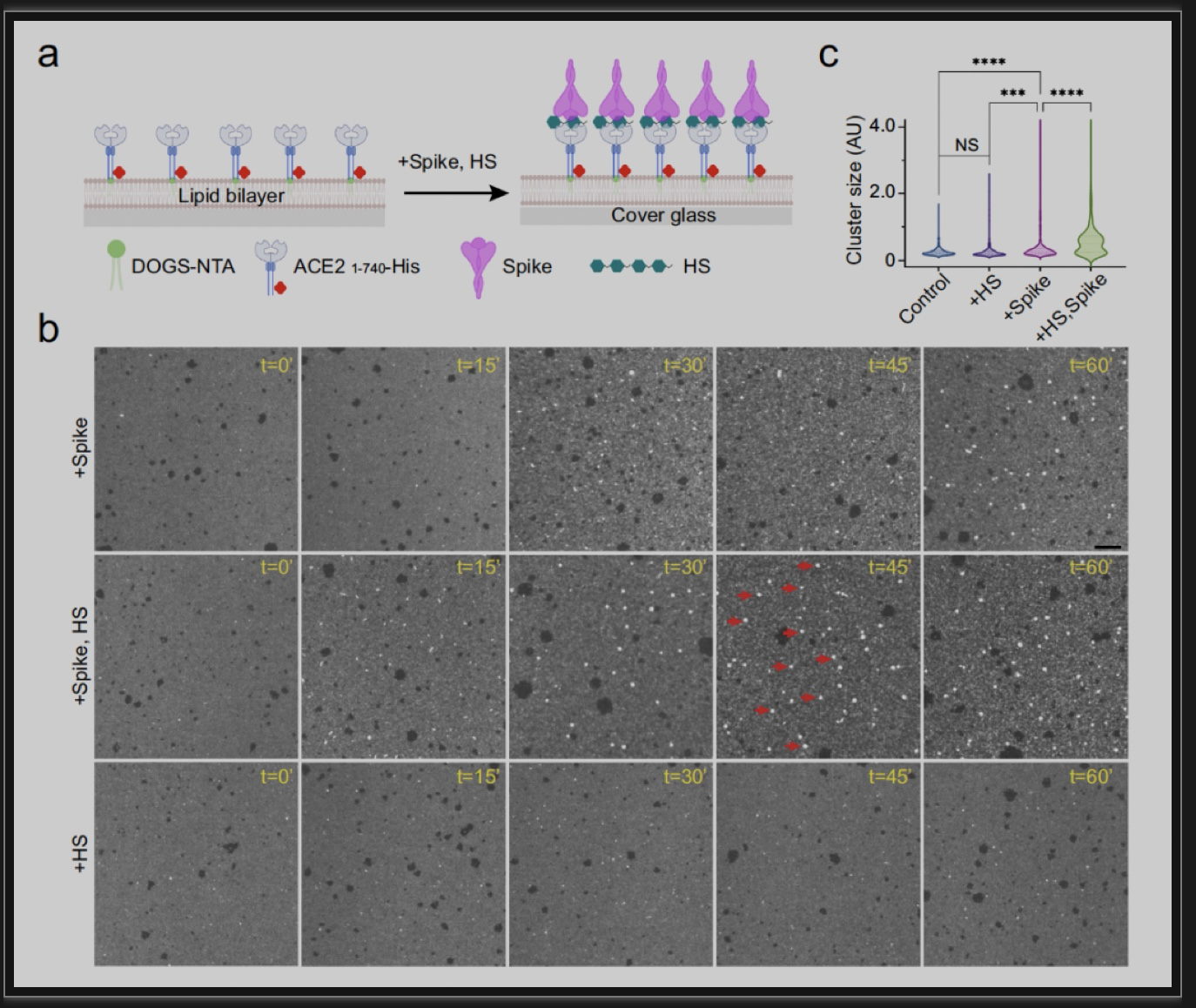
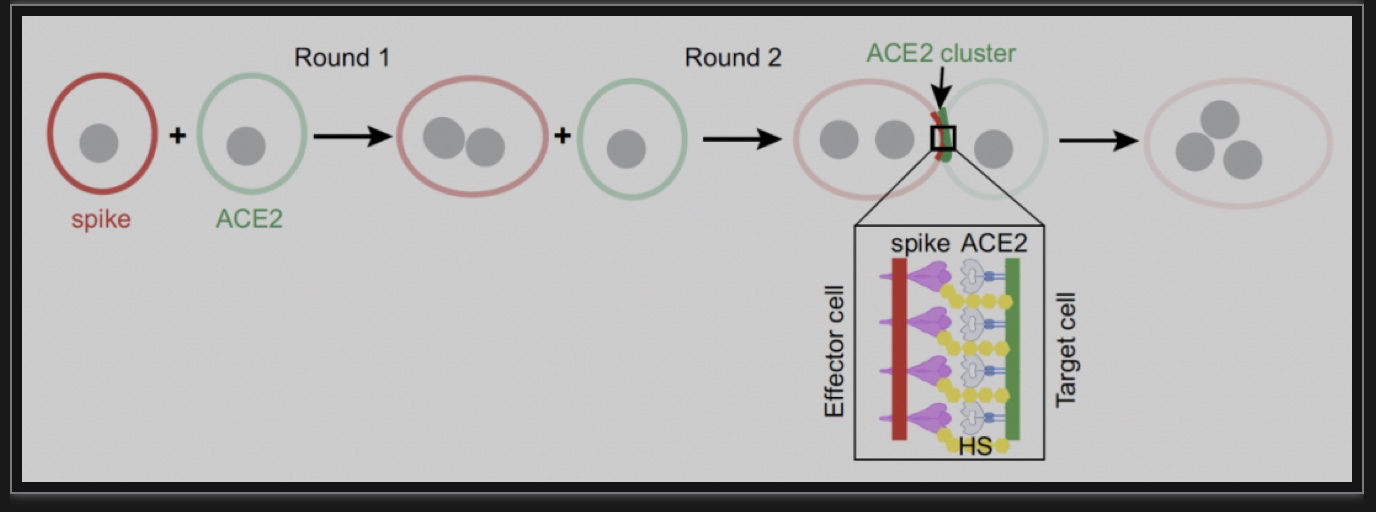
团队及其合作者的研究表明HS 可以直接参与刺突蛋白和 ACE2 的结合反应,协助诱导ACE2发生构象变化,从而允许保守的连接区域引发ACE2 的聚集。 由于聚集的 ACE2 可以与相对膜上的刺突结合,这些多价蛋白相互作用也因此聚集了刺突,同时将两个细胞膜偶联在一起形成突触样结构,进而促进膜融合。 虽然关于HS 是如何促进 ACE2 超聚体的机理仍有待阐明,该团队的发现可以很好的解释刺突蛋白如何在低表面浓度下仍可以有效促进细胞融合(图 4)。




文章结论与讨论,启发与展望
团队及其合作者的研究表明HS 可以直接参与刺突蛋白和 ACE2 的结合反应,协助诱导ACE2发生构象变化,从而允许保守的连接区域引发ACE2 的聚集。 由于聚集的 ACE2 可以与相对膜上的刺突结合,这些多价蛋白相互作用也因此聚集了刺突,同时将两个细胞膜偶联在一起形成突触样结构,进而促进膜融合。 虽然关于HS 是如何促进 ACE2 超聚体的机理仍有待阐明,该团队的发现可以很好的解释刺突蛋白如何在低表面浓度下仍可以有效促进细胞融合(图 4)。