封面故事:封面设计灵感来源于中国古典四大名著之一的《西游记》。当孙悟空(NKs)识破美丽的小女孩是由一心想吃唐僧肉的白骨精(CTCs)所变,并要尝试将其杀死时,白骨精会通过假装楚楚可怜唤起唐僧(血小板)的悲悯之心来保护她,猪八戒(HLA-E)也被唐僧误导,以致最后阻碍了对白骨精的制服(图1)。

图1 Cancer Cell封面文章
肿瘤细胞的转移扩散是癌症相关死亡的主要原因。从原发灶肿瘤脱落的循环肿瘤细胞(Circulating tumor cells, CTCs)被认为是肿瘤远端转移的“种子”[1-3]。阐明肿瘤细胞转移扩散的潜在机制,开发针对肿瘤转移“种子”细胞的新型治疗策略对抑制肿瘤转移具有重要意义。近年来,随着人们对肿瘤免疫逃逸的认知,免疫检查点阻断已经彻底改变了多种癌症的治疗模式[4-6]。目前,实体肿瘤原发或转移灶肿瘤微环境中肿瘤细胞与不同类型的免疫细胞之间的免疫检查点分子已经得到了广泛的研究。由于血液循环是肿瘤细胞从原发灶向远端转移的主要途径[7-9],研究CTCs与血液中免疫细胞之间的相互作用可能提供一种通过激活宿主免疫系统来阻断转移的策略。然而,目前关于CTCs在血液中如何逃脱宿主免疫监视的机制尚不清楚,也缺乏有效的抑制CTCs转移扩散的治疗方案。发现了CTCs与NK细胞间新的免疫检查点分子对HLA-E:CD94-NKG2A,阐明了CTCs逃避宿主免疫监视的新机制,进而提出靶向免疫检查点HLA-E:CD94-NKG2A抑制肿瘤转移的治疗策略。

为了研究CTCs的转移机制,团队以胰腺导管癌(pancreatic ductal adenocarcinoma, PDAC)肝转移为模型,利用单细胞转录组测序技术刻画了PDAC原发灶肿瘤、CTCs和肝转移灶肿瘤微环境的转录普特征,基于CellPhoneDB分析了原发灶肿瘤细胞、CTCs和转移灶肿瘤细胞与免疫细胞间的相互作用,鉴定出CTCs与NK细胞间特异性的免疫检查点分子对HLA-E:CD94-NKG2A。并通过体内外实验,证明了利用anti-NKG2A的阻断抗体或者shHLA-E阻断该免疫检查点分子对的结合可有效的抑制肿瘤转移,表明HLA-E:CD94-NKG2A是CTCs与NK细胞间的一个新型的免疫检查点分子对(图2)。
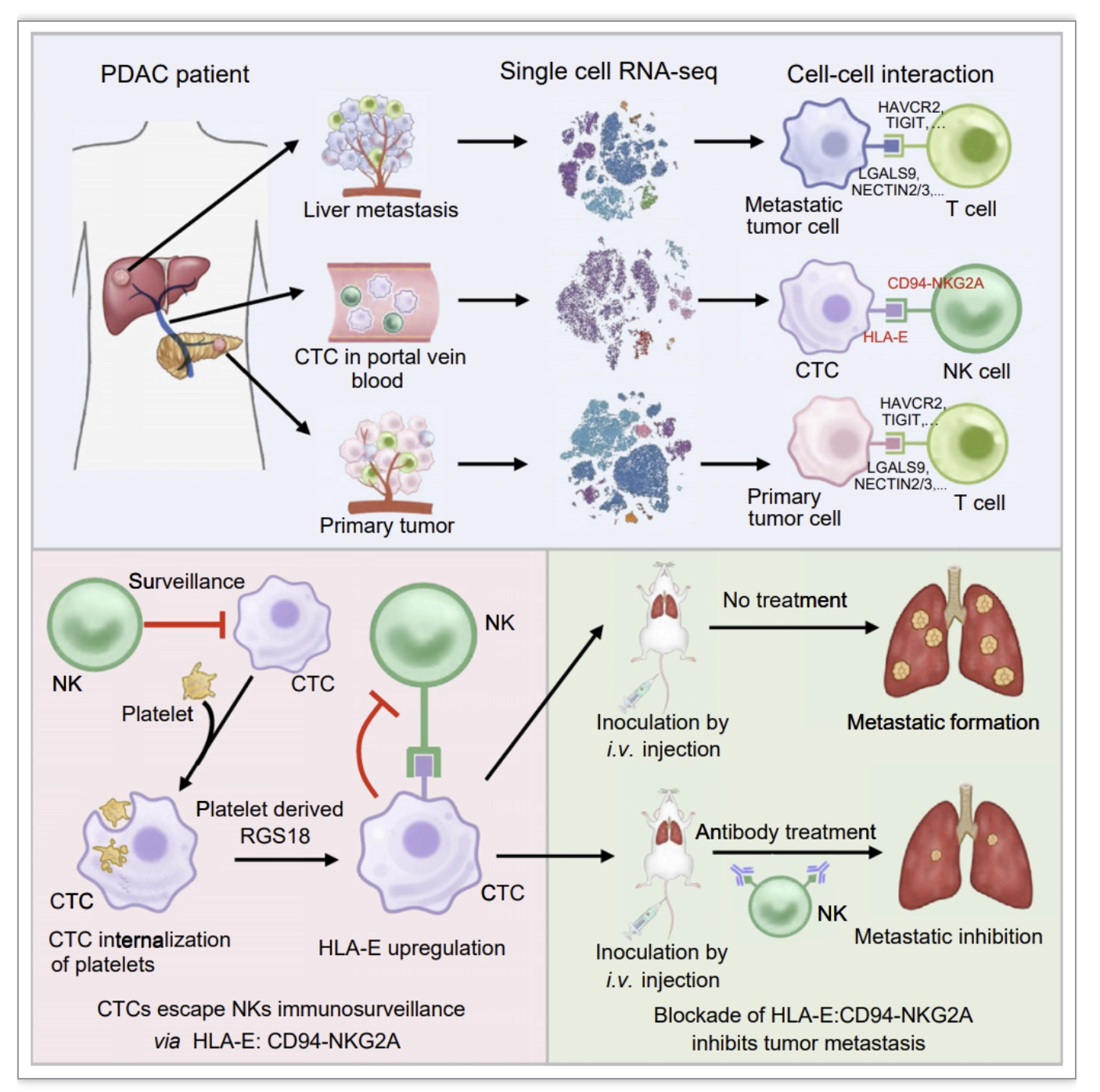
图2 文章整体设计思路
(图源:Liu X, et al ., Cancer Cell. 2023)
首先,基于CellPhoneDB数据库,研究者们对肿瘤细胞与不同类型免疫细胞之间的相互作用进行探索。结果发现,在原发或转移病灶的肿瘤微环境中,肿瘤细胞与多种类型免疫细胞发生相互作用,如CD8+T细胞、巨噬细胞、NK细胞等。而CTCs主要通过其表面的HLA-E分子与NK细胞上的CD94-NKG2A分子发生特异性的相互作用。
值得注意的是,无论是原发或转移病灶肿瘤微环境中还是血液环境中,大多数NK细胞都表达CD94-NKG2A,但HLA-E在CTCs上的表达水平要远高于实体病灶中的肿瘤细胞(图3)。
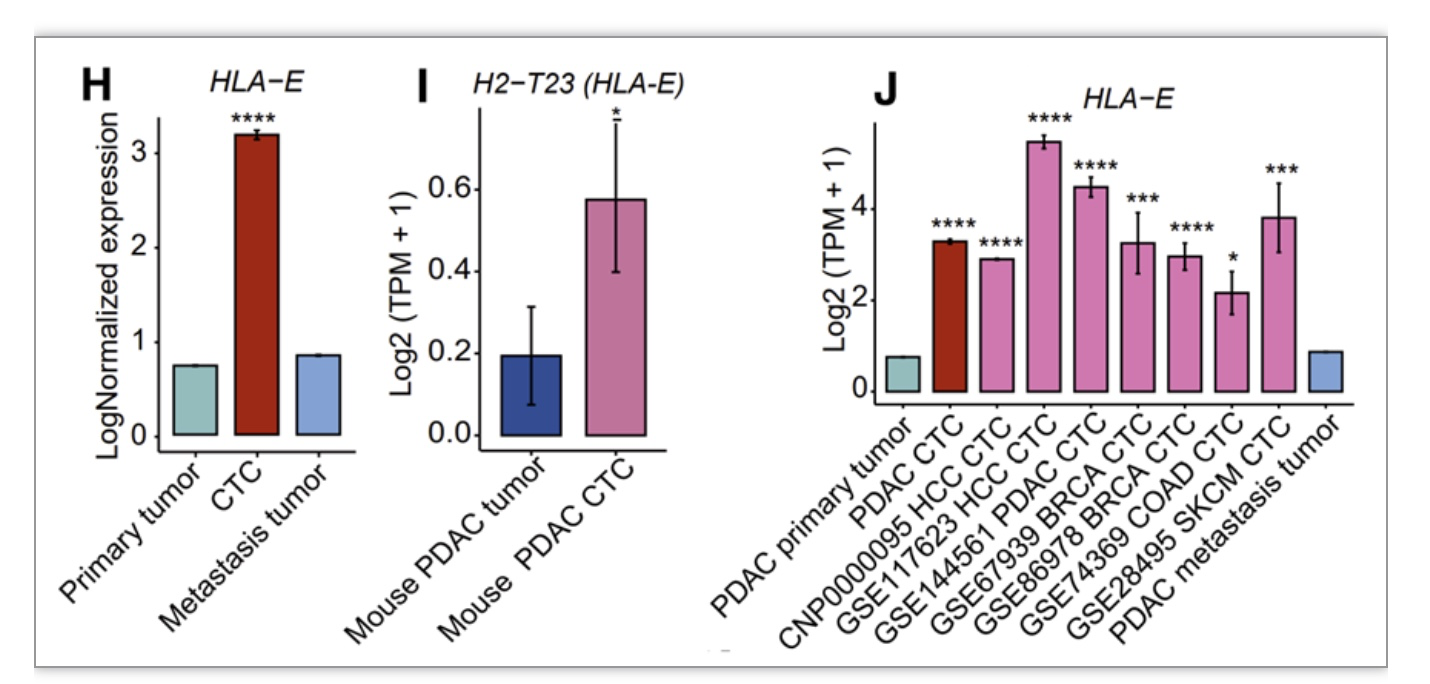
图3 鉴定出CTCs特异的免疫检查点HLA-E: CD94-NKG2A
(图源:Liu X, et al ., Cancer Cell. 2023)
接下来,研究者们利用体外实验和体内动物实验验证表明,使用抗NKG2A抗体治疗或使用遗传学手段敲低HLA-E的表达来阻断CTCs和NK细胞的结合和互作能够显著抑制PDAC肿瘤转移,并显著提高发生肺转移的PDAC小鼠在接种肿瘤后第27天的总生存率(图4)。
另外,阻断HLA-E:CD94-NKG2A之间的互作,其抗肿瘤效果仅局限于在血液循环中流动的CTCs,那些已经成功转移阵地、定植在新器官的肿瘤细胞不受影响。
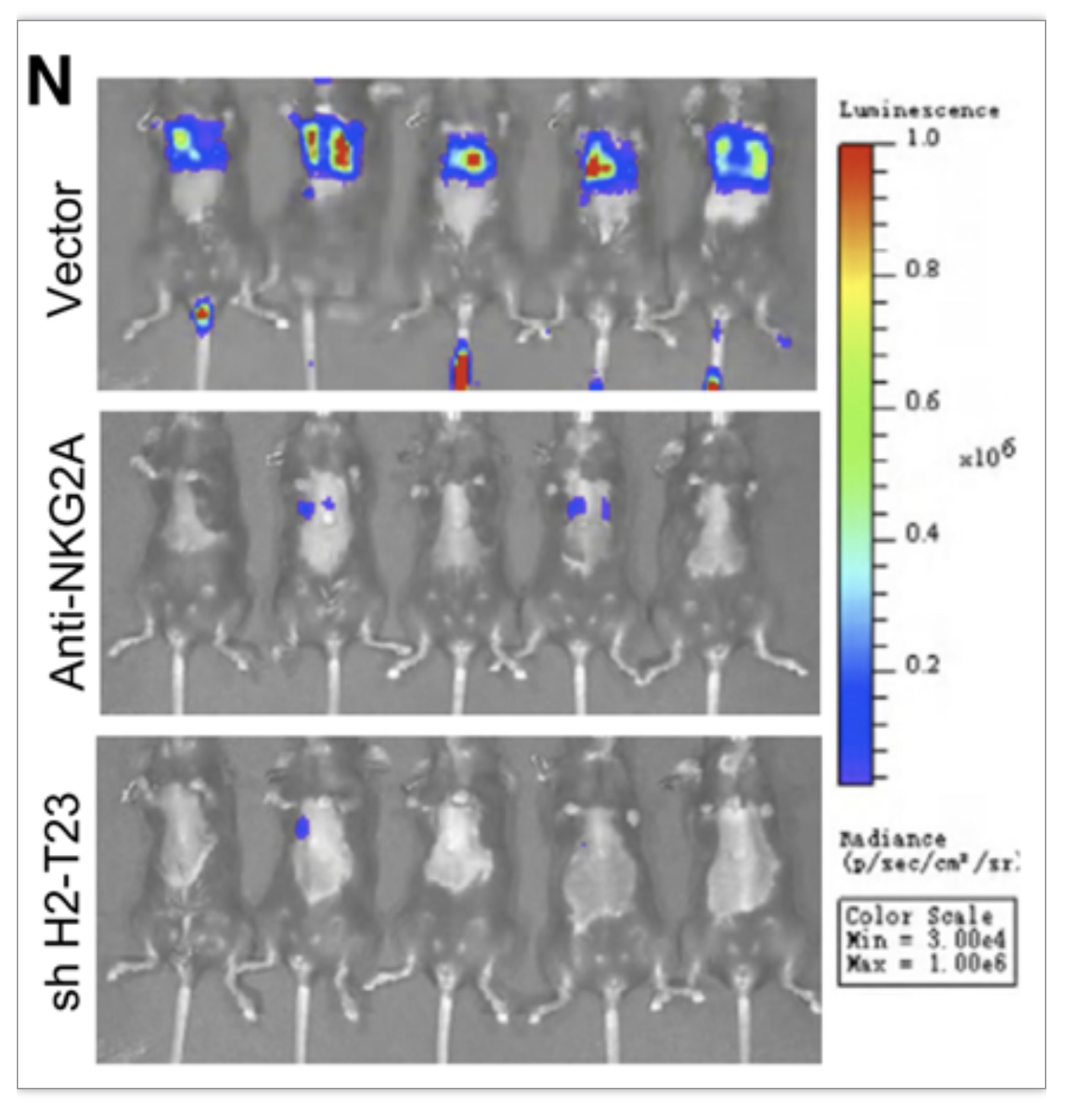
图4 阻断免疫检查点HLA-E:CD94-NKG2A抑制小鼠肺转移的形成
(图源:Liu X, et al ., Cancer Cell. 2023)
进一步的分子机制研究发现,血小板来源RGS18通过AKT-GSK3β-CREB信号通路驱动CTCs中HLA-E的表达上调。通常认为,血小板通过黏附在CTC表面形成物理屏障,保护CTCs抵御免疫毒性细胞的攻击。有趣的是,该研究发现CTCs可以内吞血小板,并获得RGS18基因,从而帮助CTCs逃避NK细胞的免疫监视(图5)。这一发现颠覆了以往人们认为血小板黏附在CTC表面保护CTCs的认知[10-12],为研究血小板促进肿瘤转移提供了新的思路。
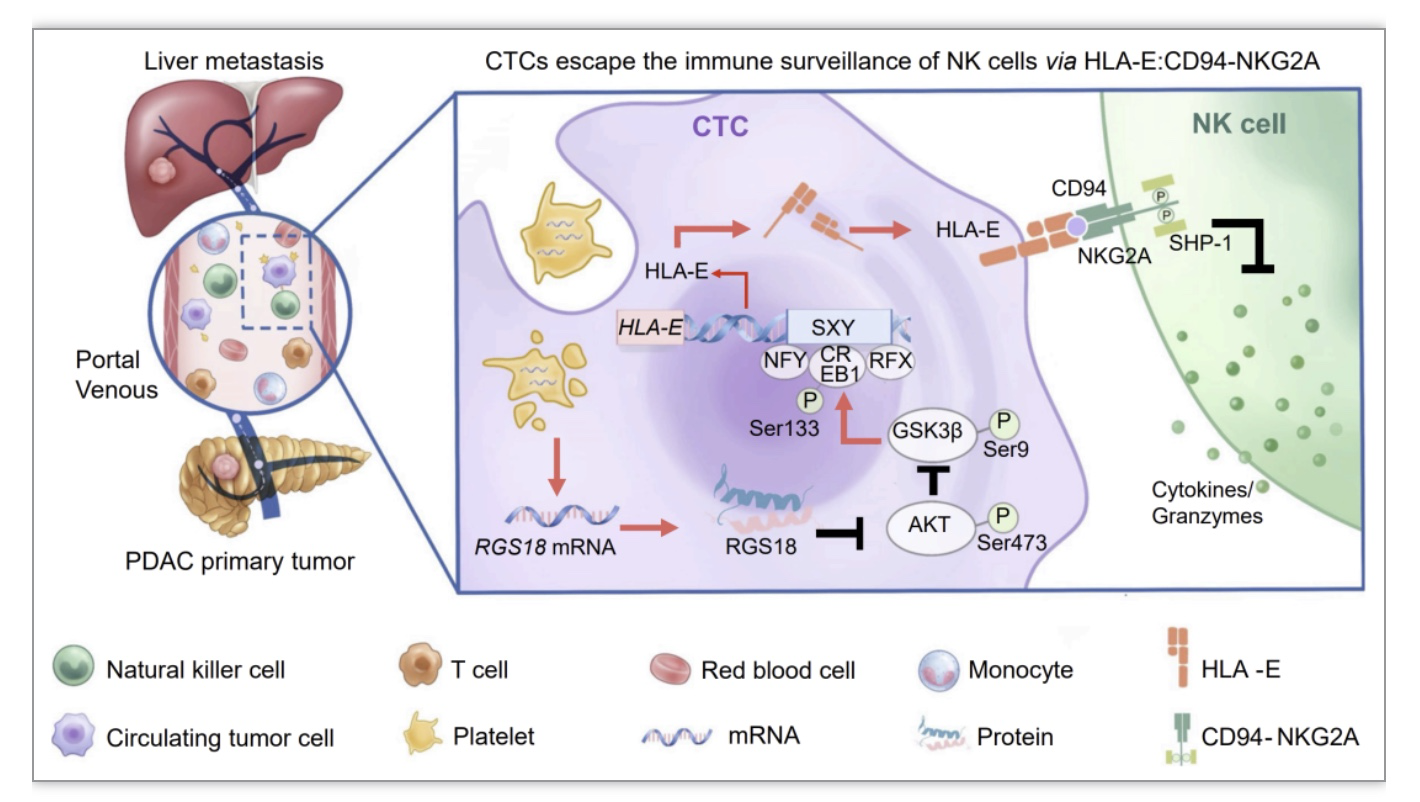
图5 血小板来源的RGS18通过AKT-GSK3β-CREB信号通路轴促进HLA-E的表达并介导CTCs逃避NK细胞免疫监视
(图源:Liu X, et al ., Cancer Cell. 2023)

