骨关节炎(Osteoarthritis, OA)是最常见的关节炎之一,可累及包括颞下颌关节、四肢关节在内的人体所有滑膜关节。该病以关节软骨的破坏为主,引起疼痛和活动障碍,严重影响患者的生活质量。目前,临床上尚缺少有效预防、阻止或修复关节软骨破坏的方法,根本原因之一是对关节软骨形成的机制尚未完全了解。因此,阐释关节软骨形成的机制,特别是关节软骨干细胞的来源及分化机制,对理解OA的发病过程、开发该病有效的治疗药物及方法至关重要,也是领域内亟需解决的前沿基础科学问题。该研究首次发现NFATc1在关节软骨干细胞中表达,并结合干细胞体内示踪等技术,在空间位置上进一步明确了关节发育早期软骨干细胞的来源,同时鉴定NFATc1是调控关节软骨细胞分化的关键转录因子。长期以来, NFATc1在肌骨骼系统中被认为是调控破骨细胞分化和功能的关键基因,实验室以往报道了NFATc1促进软骨细胞分化(与本研究结论不同),因此,该项发现对以往相关认知具有颠覆性,已被选为“eLife digest”做重点推介。该论文通过eLife传统peer-review过程发表。

该项研究承接葛献鹏教授在哈佛医学院博士后研究期间的创新性发现:NFATc1和NFATc2通过相互补偿的机制在韧带及其附丽点处的干细胞中抑制多发性骨软骨瘤的形成,NFATc1和NFATc2双基因敲除小鼠能够模拟人类多发性骨软骨瘤的病理变化和临床表现,且NFAT基因删减的剂量能够决定骨软骨瘤的数量和大小,并以此提出了骨软骨瘤发病的新机制(Ge et al., JCI Insight 2016, 杂志特色论文)[2]。在此基础上,葛献鹏课题组结合多个基因编辑小鼠模型、干细胞体内示踪、体外培养鉴定和高通量转录组学等技术,进一步研究发现NFATc1在关节软骨干细胞中表达,且NFATc1表达的干细胞在关节发育早期位于关节原基的侧翼,从而在空间位置上进一步明确了关节软骨干细胞的来源。研究还发现,NFATc1随着关节软骨细胞的分化和成熟表达逐渐降低,在干细胞中删减NFATc1足以引起自发性软骨分化,而高表达NFATc1则抑制软骨细胞分化。机制上,作者发现NFATc1负调控软骨特征性基因Col2a1的转录(图1&2)。
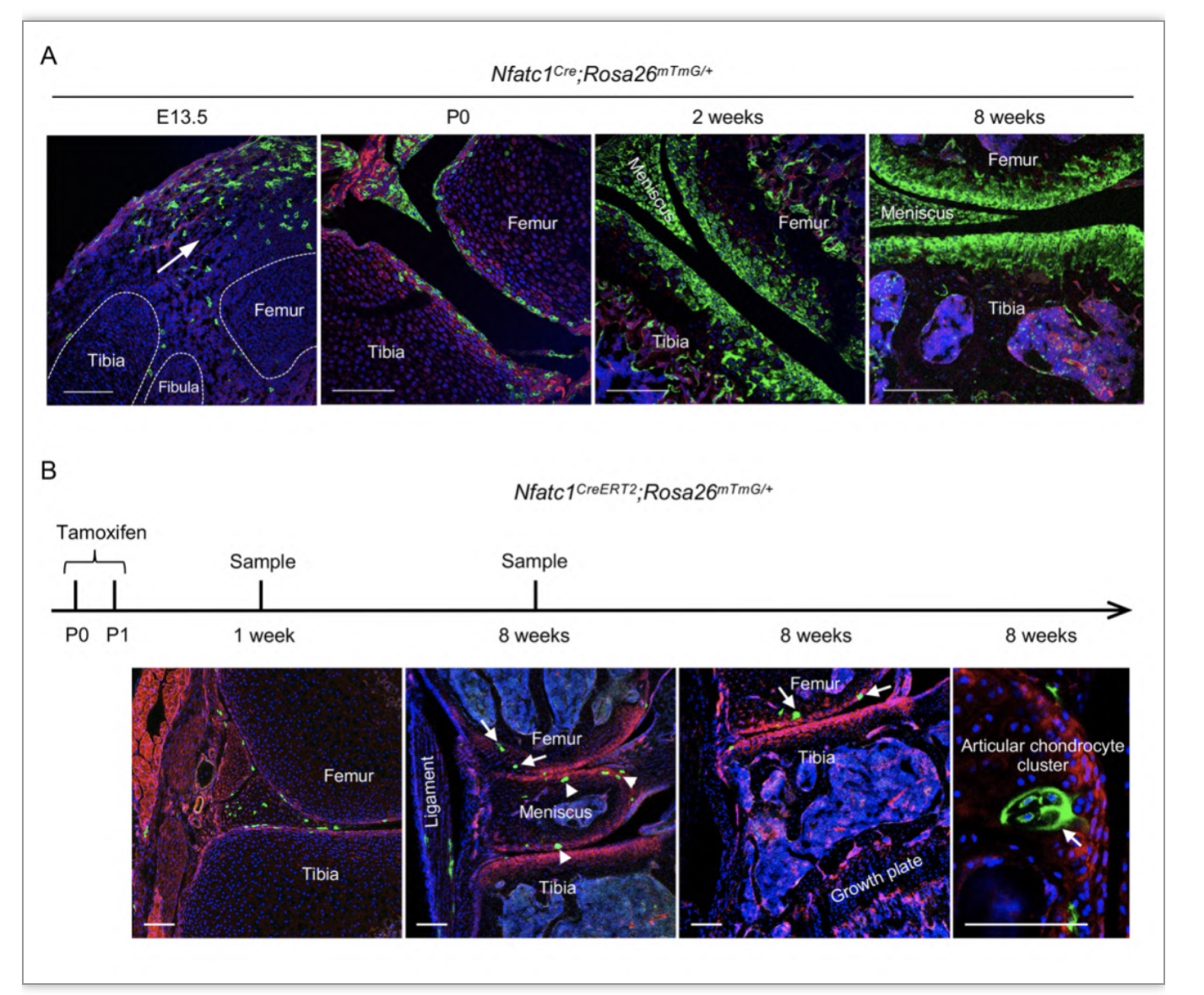
图1. NFATc1+ 的干细胞形成关节软骨细胞
(图源:Zhang F, Wang Y, et al., eLife, 2023)
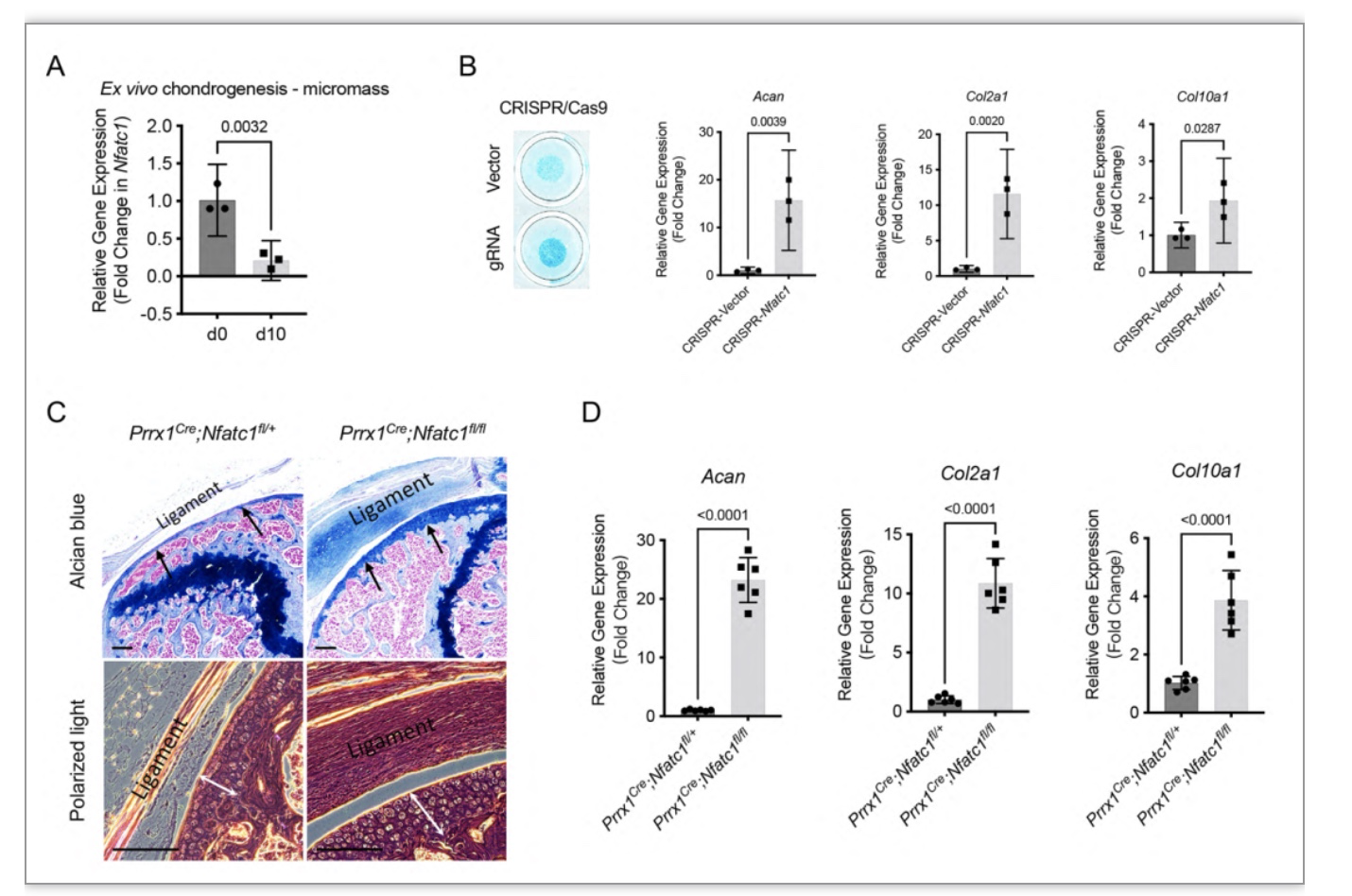
图2. NFATc1调控关节软骨细胞分化
(图源:Zhang F, Wang Y, et al., eLife, 2023)
综上所述,该研究鉴定NFATc1是标记关节软骨干细胞的重要分子,以此进一步明确了关节软骨干细胞的早期来源,同时发现NFATc1是决定关节软骨细胞分化的关键基因,调控NFATc1单个基因足以诱导软骨细胞分化,这些创新性发现对理解OA的发病机制及治疗均具有重要意义。同时,葛献鹏课题组于2023年1月在Cell出版社综合性期刊Heliyon发表研究论文,报道了NFATC1在人和小鼠骨膜干细胞中高表达[3]。这些系列研究鉴定了一类以NFATC1为分子特征的新型骨骼干细胞,对此类干细胞的进一步深入探索,将有助于理解包括OA在内的骨骼疾病的发病机制,可用于开发新型治疗方法和药物。

