随着电离辐射在生产生活中的广泛应用,辐射暴露的风险日益增加。在受到辐射短期内出现的病症为辐射的早期效应,如急性皮肤损伤、急性放射病等。在数月或几年后出现的病症为辐射急性损伤的远期效应,其涉及全身多个组织器官的慢性损伤,器官功能出现紊乱,机体衰老进程加速[1]。
辐射引起的造血系统损伤是影响受照人员健康状况的重要因素,其中骨髓持久性抑制是临床肿瘤放疗后最常见的毒副作用之一,也是辐射急性损伤远期效应的主要表现之一,临床尚无有效治疗手段[2]。辐射引起的骨髓持久性抑制与造血干细胞(hematopoietic stem cells,HSCs)衰老密切相关。与年轻造血干细胞相比,衰老的造血干细胞发生了表型和功能的改变,包括自我更新能力降低、髓系分化偏移和重建造血能力减弱,最终导致造血功能衰竭[3,4]。目前造血辐射远期损伤的防治研究仍是亟待解决的问题。
烟酰胺核糖(nicotinamide riboside,NR)是一类天然的维生素B3衍生物,在细胞内可以显著提高烟酰胺腺嘌呤二核苷酸(NAD+)水平,已在多个器官组织中报道具有抗细胞衰老、抗氧化应激和维持线粒体稳态等作用,有研究发现烟酰胺核糖可通过改善线粒体功能恢复造血干细胞的功能[5]。然而,NR对辐射诱导早衰小鼠造血系统远期损伤的作用尚不清楚。
该研究在证实电离辐射会对造血系统造成远期损伤,并加速小鼠的衰老进程的基础上,通过补充NR抑制了早衰小鼠HSC衰老和髓系分化偏移,从而缓解了受照小鼠造血系统辐射远期损伤。
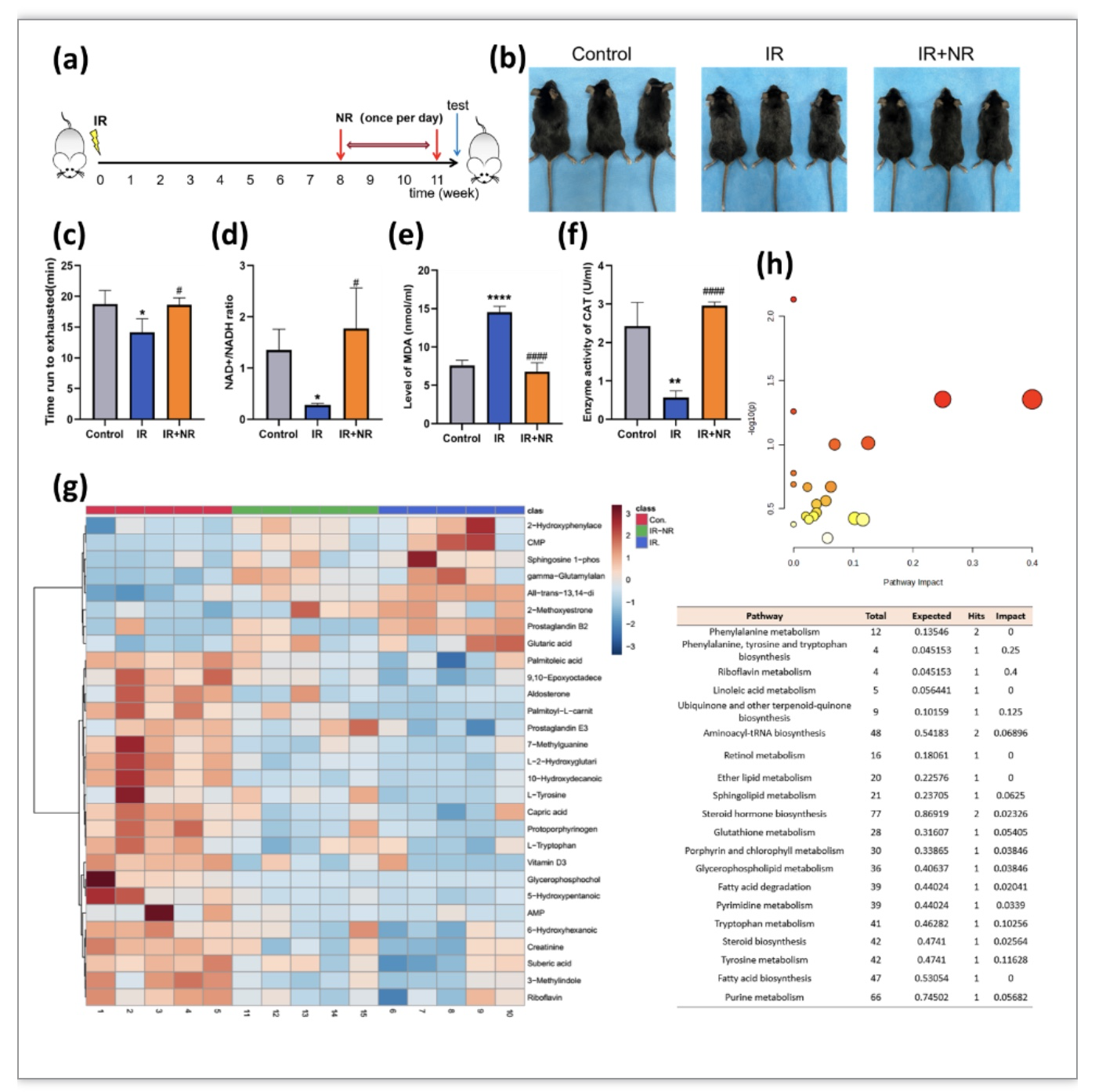
为了证实电离辐射是否会诱导小鼠早衰,以及评估NR对电离辐射诱导早衰小鼠是否具有改善作用,研究人员对小鼠进行6Gy全身照射,在照射8周后给予小鼠400mg/kg/d 的NR溶液,连续给药三周,在照射11周后对小鼠进行观察和评估(图1)。结果显示,照射组小鼠的毛发粗糙暗淡,毛色变为灰白色,运动耐力减弱,血清中NAD+/NADH比率显著降低,氧化损伤加重。给予NR可以改善辐射导致的小鼠早衰表型。随后研究人员通过液相色谱-质谱联用(LC-MS)对小鼠血清进行代谢组学分析,发现差异代谢物主要富集在核黄素代谢、氨基酸生物合成及代谢、嘌呤代谢和谷胱甘肽代谢等通路,这提示NR的治疗作用可能是通过调控氧化磷酸化和氨基酸代谢过程实现。
图1 NR减轻辐射诱导的小鼠早衰表型
为了进一步分析NR对辐射造成的远期造血损伤的作用,研究人员在小鼠6Gy全身照射11周后分离小鼠股骨,获取骨髓单侧股骨有核细胞(BMNCs)进行计数,并使用流式细胞仪分析各组小鼠骨髓成熟造血细胞的比例(图2a-d)。结果表明,照射可引起小鼠骨髓有核细胞数下降。流式分析结果显示,与对照组比较,照射组小鼠骨髓中T淋巴细胞和B淋巴细胞比例降低,髓系细胞显著比例升高,NR可以显著降低骨髓中髓系细胞比例。随后研究人员通过流式细胞术对小鼠骨髓中LSK(Lin-Scal+c-Kit+)和其他未成熟造血细胞进行分析(图2e-g)。结果显示,接受照射小鼠骨髓中LSK水平显著降低,而NR可以使LSK水平显著升高。此外,造血干细胞来源的其他祖细胞群体的比例也发生改变。其中共同淋系祖细胞(CLP)的减少和粒细胞-巨噬细胞祖细胞(GMP)的增加表明骨髓发生髓系-淋系细胞谱系偏倚,NR在祖细胞水平上可有效改善辐射诱导早衰小鼠造血系统的损伤,恢复骨髓细胞中髓系-淋系细胞的平衡。活性氧检测结果表明NR可抑制LSK中ROS水平。
图2 NR改善辐射诱导早衰小鼠骨髓造血细胞的分化水平
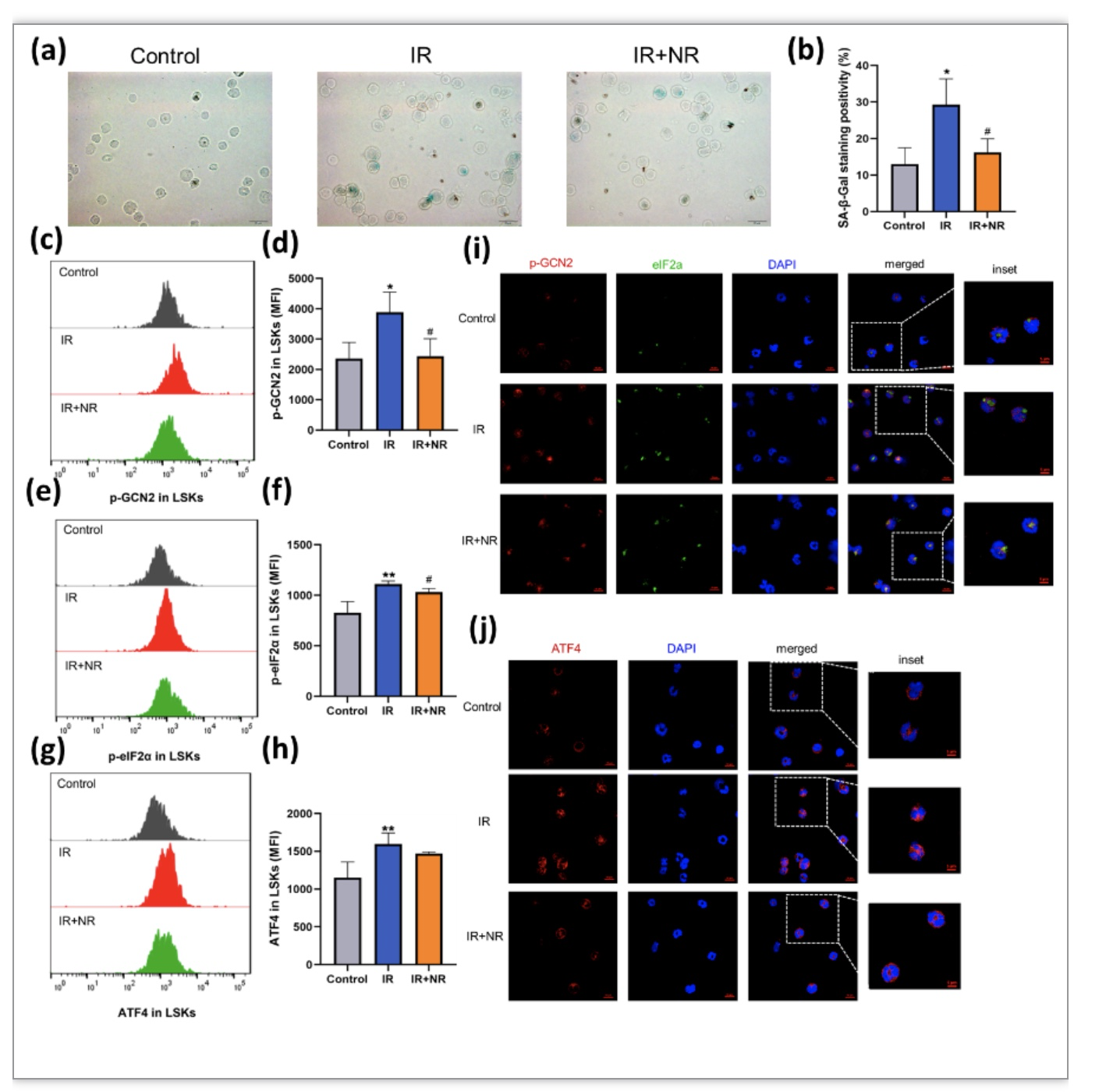
随后研究人员发现辐射诱导早衰小鼠中LSK发生衰老,初步探究其机制发现LSK衰老可能与GCN2/eIF2α/ATF4通路的过度活化相关,给予NR可以部分抑制该通路的活化,减缓LSK衰老(图3)。
图3 NR可以降低LSK衰老水平
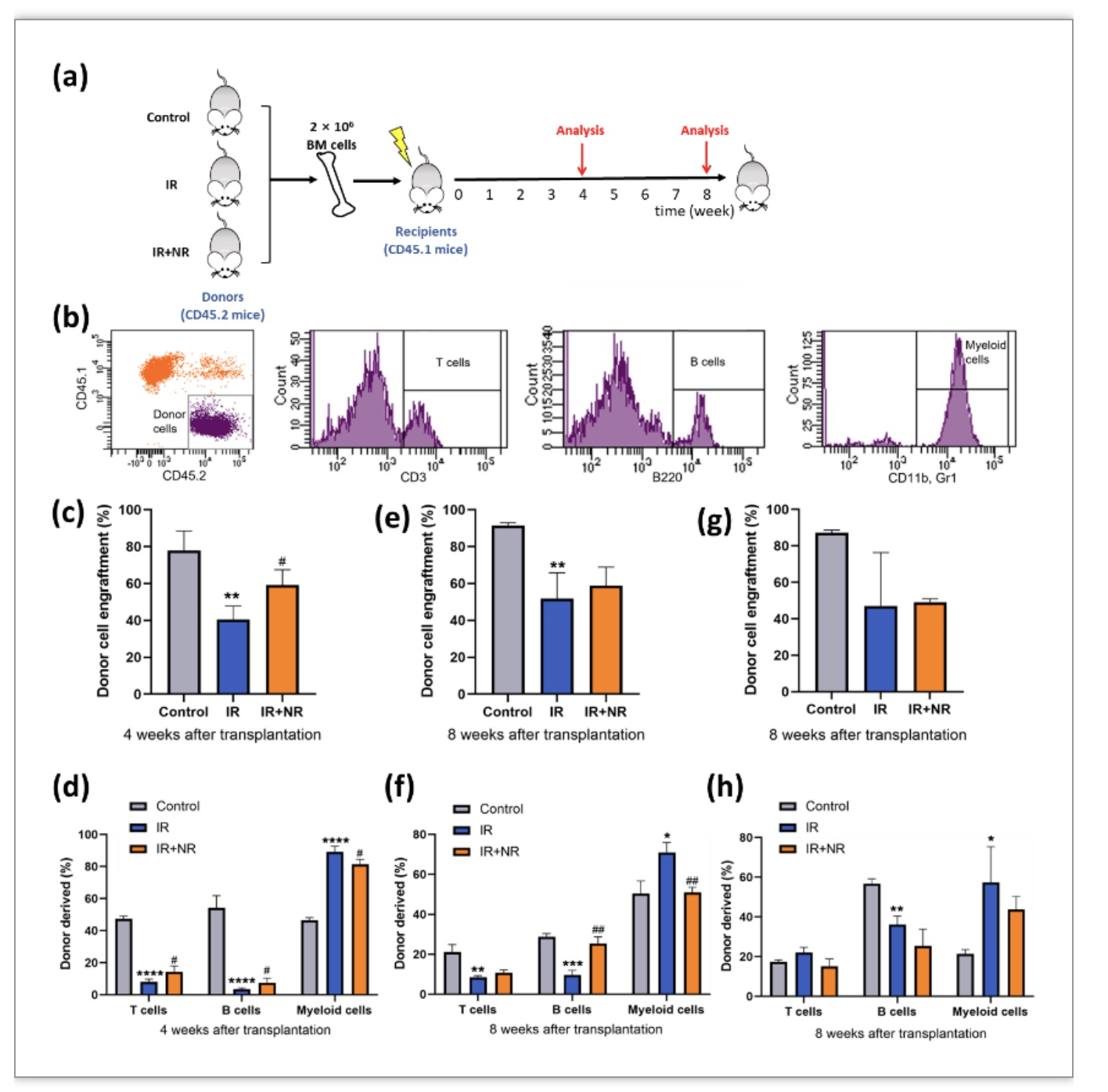
最后研究人员通过竞争性移植实验评估了HSC的造血重建功能(图4)。外周血检测结果显示移植4周后NR可以显著提高辐射诱导的早衰小鼠HSC的多系移植和造血重建功能,然而NR对HSC的作用在移植8周后并没有得到进一步提升,这表明NR可以在短期内提高HSC的造血重建能力。
图4 NR部分提高HSC的多系移植和造血重建能力
电离辐射造成的远期损伤会严重影响受照人员和接受放疗后癌症幸存者的健康状况,诱发多种慢性疾病,加速机体衰老进程。然而目前针对电离辐射的远期效应及其诱导的早衰研究还相对缺乏,也很少有相关研究报道有效的解决方案。该研究在成功建立辐射诱导早衰小鼠模型的基础上,发现了烟酰胺核糖对辐射诱导细胞和早衰小鼠造血系统的治疗作用,并对其潜在机制进行了探讨。同时,该研究尚存在一定的局限性。首先对机制的探讨不够深入,仍需通过体外细胞实验或基因分子技术进行深入探究。其次,长期以来科学界普遍认为DNA的变化是导致衰老的最主要原因,由于DNA累积基因突变等导致的错误变化,从而影响基因活性,造成细胞功能失常。然而最近的一项研究表明,表观遗传分子的退化也是衰老发生的主要因素[6],因此进一步研究表观遗传分子在辐射诱导HSCs衰老中的作用也是未来的工作方向。