自然杀伤细胞(Natural killer cells,NK细胞)是免疫监视感染细胞和肿瘤细胞的关键效应细胞。NK细胞的功能由多种激活和抑制性受体调控,这些受体识别靶细胞或抗原递呈细胞上各自的配体。NK细胞的缺陷和功能失调与各种癌症增加的发病率、进展和转移有关[1]。新型的免疫检查点分子已被发现在肿瘤微环境中介导NK细胞的功能障碍,因此探索NK细胞相关的免疫检查点的治疗潜力意义重大。
TIGIT是最近几年最热门的免疫检查点之一[2],表达在T 细胞和NK细胞, 主要配体是肿瘤细胞的PVR。目前全世界有100多个阻断TIGIT的临床试验在进行中。大药企巨资进入TIGIT赛道, 仅2021年TIGIT抗体重磅交易就有葛兰素史克、百时美施贵宝、阿斯利康、吉利德等, 交易金额超过60亿美元。但今年罗氏药厂二个大的三期临床试验失败,给TIGIT赛道蒙上了阴影。
“Blockade of the immunosuppressive KIR2DL5-PVR pathway elicits potent human NK cell-mediated anti-tumor immunity”,该研究揭示了人NK细胞受体KIR2DL5通过与肿瘤细胞表面PVR配体结合介导肿瘤免疫逃逸的功能及其分子机制, 发现KIR2DL5和TIGIT二个受体可同时非竞赛性结合PVR。KIR2DL5/PVR通路存在于人,但小鼠缺失。臧教授团队自主开发的KIR2DL5特异性单克隆抗体可阻断KIR2DL5/PVR这一新的NK细胞免疫检查点通路,从而显著增强NK细胞在体外以及体内杀伤肿瘤细胞的能力。

杀伤细胞免疫球蛋白样受体家族(KIR)调节NK细胞功能,大部分KIR成员通过识别人类白细胞抗原(HLA)I类分子来调节NK活性,使NK细胞通过"缺失自我机制 "杀死感染细胞和肿瘤细胞。去年臧星星教授团队报道KIR家族成员KIR3DL3的配体不是HLA I类分子[3], 而是他们在2013年发现的B7家族成员 HHLA2 [4]。KIR2DL5是臧教授团队近期研究的另一个KIR家族成员。最新研究提示KIR2DL5是继TIGIT, CD226,和CD96后又一发现的PVR的受体。研究人员通过竞争性实验发现KIR2DL5与其他三个受体结合PVR不同位点,提示其功能机制的独特性。进一步探索KIR2DL5的等位基因多态性影响其与PVR的相互作用,KIR2DL5 D0结构域中97位甘氨酸被丝氨酸替换(G97S)明显增强PVR-Ig与KIR2DL5的结合。这些结果表明,KIR2DL5的等位基因多态性影响了抗体识别以及它与PVR的结合能力。
作者发现KIR2DL5蛋白存在于多种先天性和适应性免疫细胞表面,主要表达在具有杀伤性能力的更为成熟的CD56dimCD16+NK细胞亚群。细胞毒性实验发现KIR2DL5的存在极大地抑制了NK对PVR+肿瘤细胞的细胞溶解活性,通过CRISPR/Cas9敲除肿瘤细胞中的PVR后,肿瘤细胞对NK细胞杀伤变得更为敏感(图1)。KIR2DL5与PVR结合促进NK细胞与肿瘤细胞间抑制性免疫突触的形成从而抑制NK细胞的功能。作者进一步研究发现抗KIR2DL5单克隆抗体F8B30能够有效阻断KIR2DL5-PVR相互作用,并显著增强KIR2DL5+原代NK细胞对PVR+肿瘤的杀伤作用(图1)。这些结果表明,KIR2DL5抑制NK细胞的功能并通过与肿瘤细胞上的PVR结合促进肿瘤免疫逃逸。
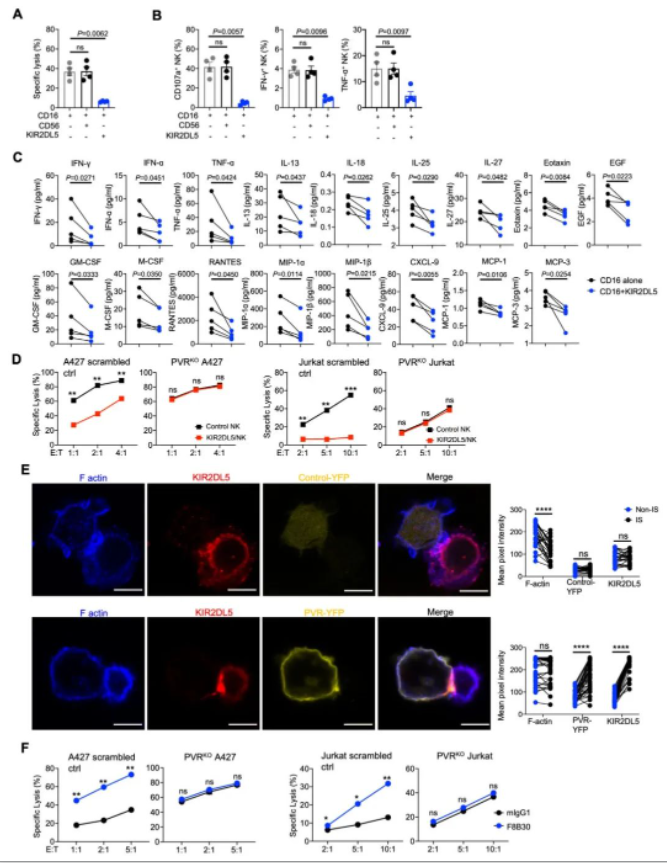
图1 KIR2DL5抑制NK细胞功能并介导PVR阳性肿瘤的免疫抵抗
(图源:Ren et al., JCI , 2022)
为了进一步探究KIR2DL5抑制NK细胞功能的作用机制,作者将KIR2DL5胞内功能结域基于免疫受体酪氨酸的抑制基序(immunoreceptor tyrosine-based inhibitory motif,ITIM)和基于免疫受体酪氨酸的开关基序(immunoreceptor tyrosine-based switch motif,ITSM)或两者的酪氨酸残基突变为苯丙氨酸,免疫沉淀试验和细胞毒性实验提示ITIM或ITSM的酪氨酸突变均影响蛋白酪氨酸磷酸酶SHP-1的募集,而SHP-2的募集仅被ITIM的酪氨酸突变所影响。功能上,ITIM和ITSM突变影响KIR2DL5+NK细胞靶向PVR+肿瘤细胞的细胞毒性作用。进一步研究表明KIR2DL5通过招募SHP-1和SHP-2抑制下游Vav1/ERK1/2/p90RSK/NF-κB信号通路,从而抑制NK细胞的激活。这些数据揭示了KIR2DL5抑制NK细胞功能的分子机制。
作者发现多种PVR+癌症,如膀胱癌、肾癌、乳腺癌等肿瘤组织中存在KIR2DL5阳性免疫细胞, 表明KIR2DL5与PVR相互作用可能通过影响肿瘤微环境中的免疫细胞功能从而实现免疫逃避。作者采用多种小鼠人源化肿瘤模型,包括实体瘤肺癌模型和血液肿瘤急性T淋巴细胞白血病模型,进一步验证了体内阻断KIR2DL5-PVR通路能明显抑制肿瘤生长并延长了小鼠的总体生存期(图2)。这些数据表明KIR2DL5-PVR可作为肿瘤免疫疗法的潜在靶点,通过阻断该通路可激活NK细胞功能,增强NK细胞的抗肿瘤免疫反应。
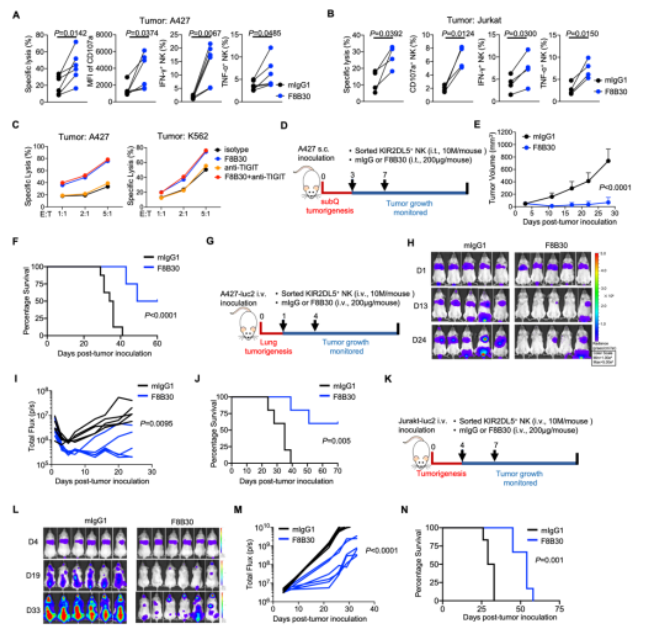
图2 体内阻断KIR2DL5显著增强基于NK细胞的抗肿瘤免疫反应
(图源:Ren et al., JCI , 2022)

图3 KIR2DL5特异性单克隆抗体阻断KIR2DL5-PVR通路并增强NK细胞肿瘤杀伤能力
(图源:Ren et al., J Clin Invest, 2022)

