皮肤瘙痒是慢性肾病,尤其是终末期患者常见的皮肤病症之一,称为慢性肾脏病相关性瘙痒(Chronic kidney disease-associated pruritus,CKD-aP),也称尿毒症瘙痒[1]。过去几十年来,CKD在全球范围内变得越来越严重,已成为一个严重的公共卫生问题;在CKD患者中大约30-85%的患者表现出不同程度的瘙痒症状,约40%的CKD患者长期遭受皮肤瘙痒的折磨 [2, 3]。CKD-aP会严重影响患者的生活质量,加重患者的负面情绪,增加患者的死亡风险[4-6];由于瘙痒是CKD患者的重要临床表现,因此寻求患者瘙痒背后的物质基础和作用靶标对阐明慢性肾病形成机理和药物治疗均具有一定的意义。相关研究结果阐述了慢性肾脏病瘙痒患者血清和慢性肾病瘙痒模型瘙痒小鼠血清中尿囊素的变化,尿囊素诱导小鼠的行为反应,尿囊素作用的分子靶标及引起细胞反应的下游信号通路。

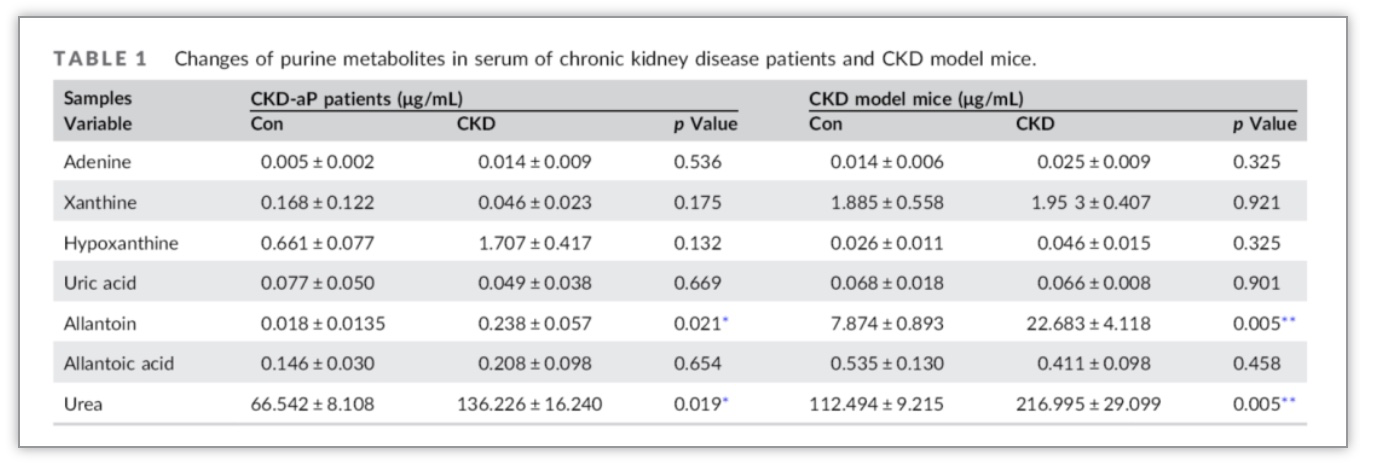
表1 CKD-aP患者及动物模型小鼠血清尿囊素变化
(图源:Yang, Y. et al., Journal of Cellular Physiology, 2003)
为了明确尿囊素参与瘙痒,研究人员利用行为学方法检测了尿囊素诱导的抓挠反应(图1)。实验结果证实小鼠颈背部皮下注射或尾静脉注射尿囊素,均可诱导小鼠明显的抓挠反应(p<0.05)。
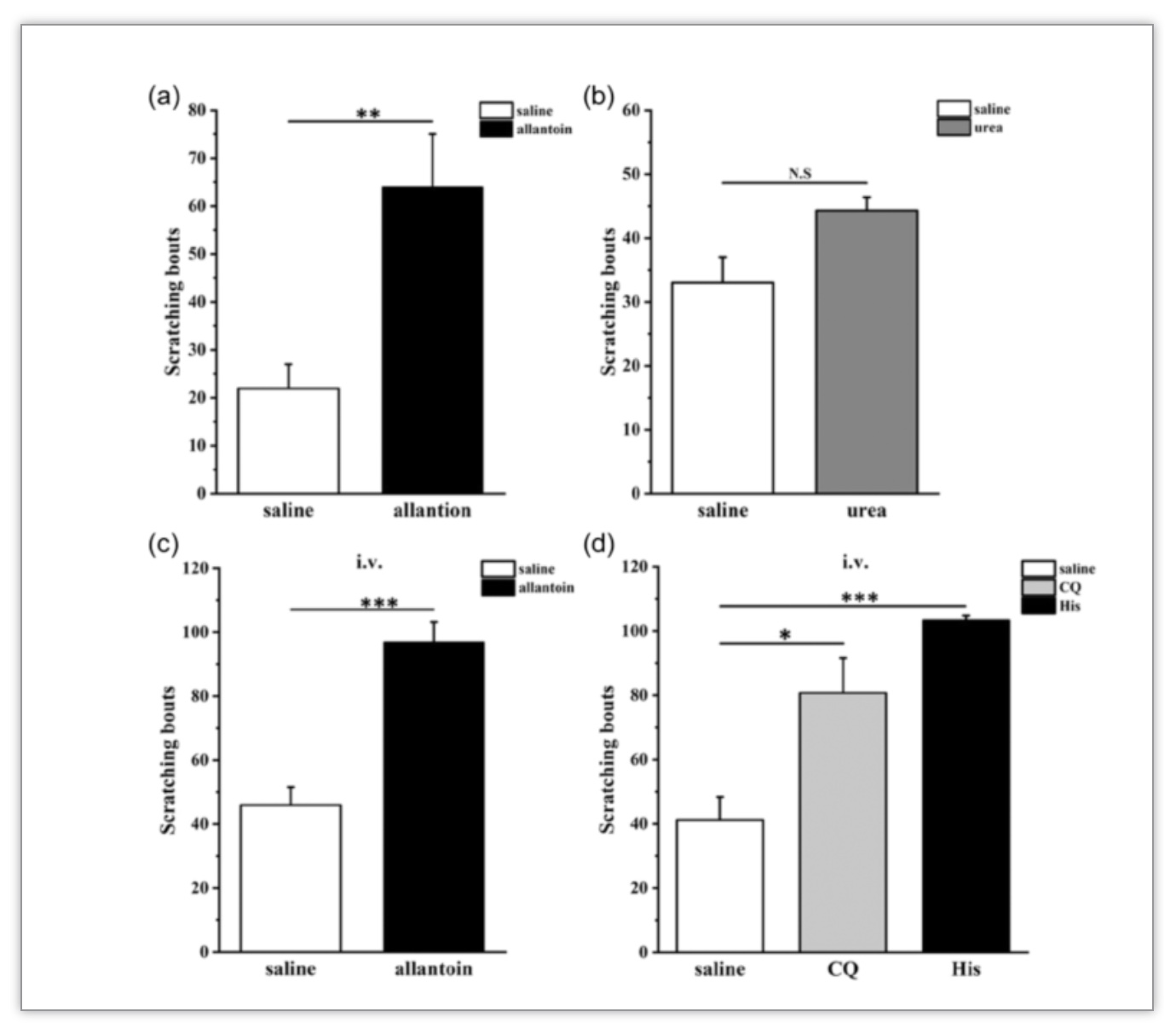
图1 尿囊素诱导小鼠产生明显抓挠行为
(图源:Yang, Y. et al., Journal of Cellular Physiology, 2003)
其次,研究人员检查了慢性肾病模型小鼠肾组织结构的变化,结果表明:模型小鼠表现出典型的肾脏损伤,模型小鼠肾脏出现明显的肾小球萎缩、间质炎性细胞浸润、组织纤维化(图2)。模型小鼠肾脏纤维化和炎性细胞浸润与对照组相比具有显著性差异(p<0.001)。
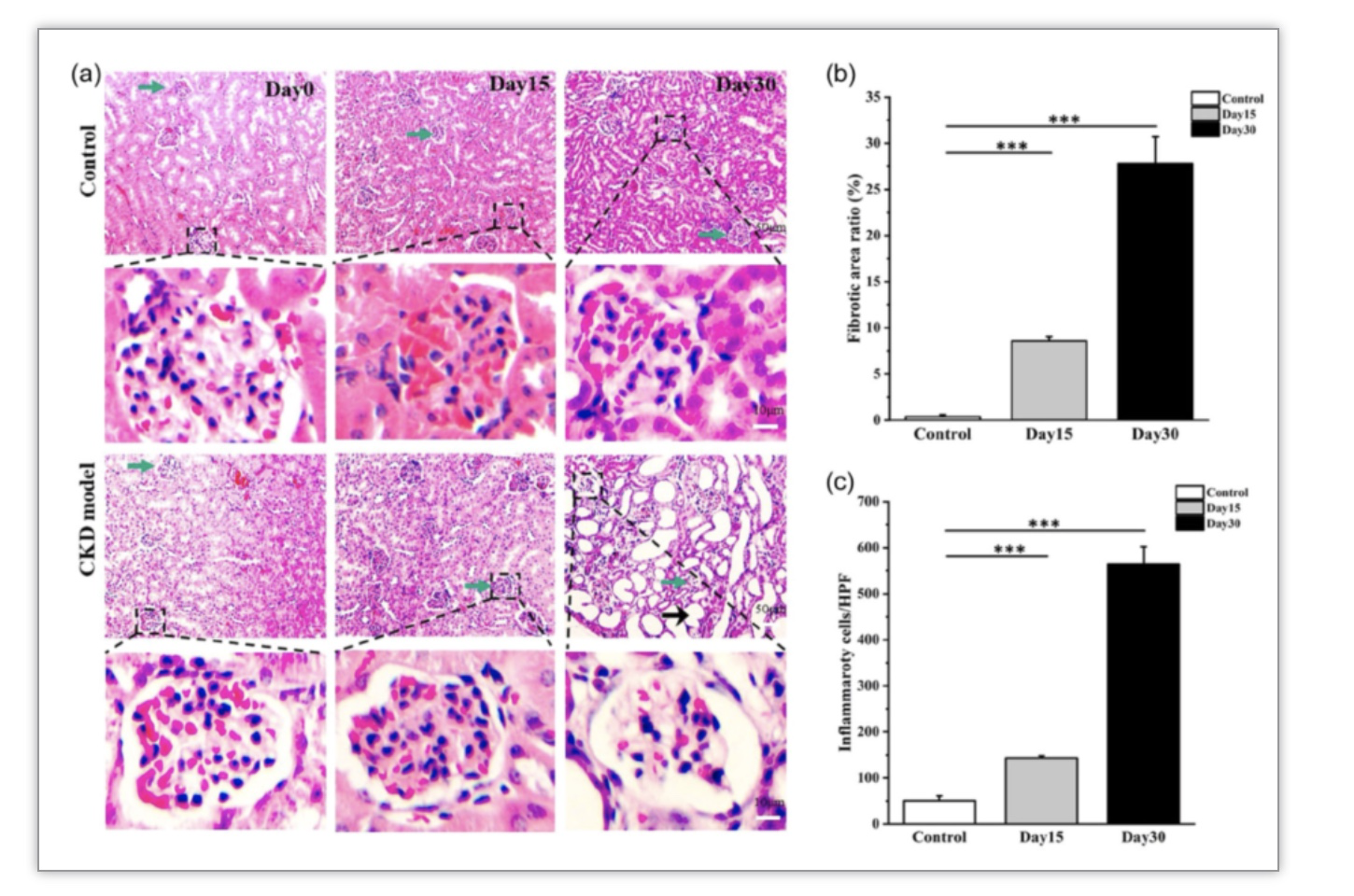
图2模型小鼠表现出典型的肾脏损伤
(图源:Yang, Y. et al., Journal of Cellular Physiology, 2003)
接着,试着寻找尿囊素参与瘙痒的分子机制。研究人员利用钙离子成像、全细胞膜片钳技术和不同基因敲除小鼠仔细分析了尿囊素作用的靶点和引起细胞反应的相关信号通路。结果表明:尿囊素诱导的瘙痒行为在MrgprD KO小鼠和TRPV1 KO小鼠的瘙痒行为明显降低(图3),同时,尿囊素与MrgprD的激动剂剂β-alanine激活相同的DRG神经元,并进一步证明MrgprD下游信号通路中相关的离子通道为TRPV1。
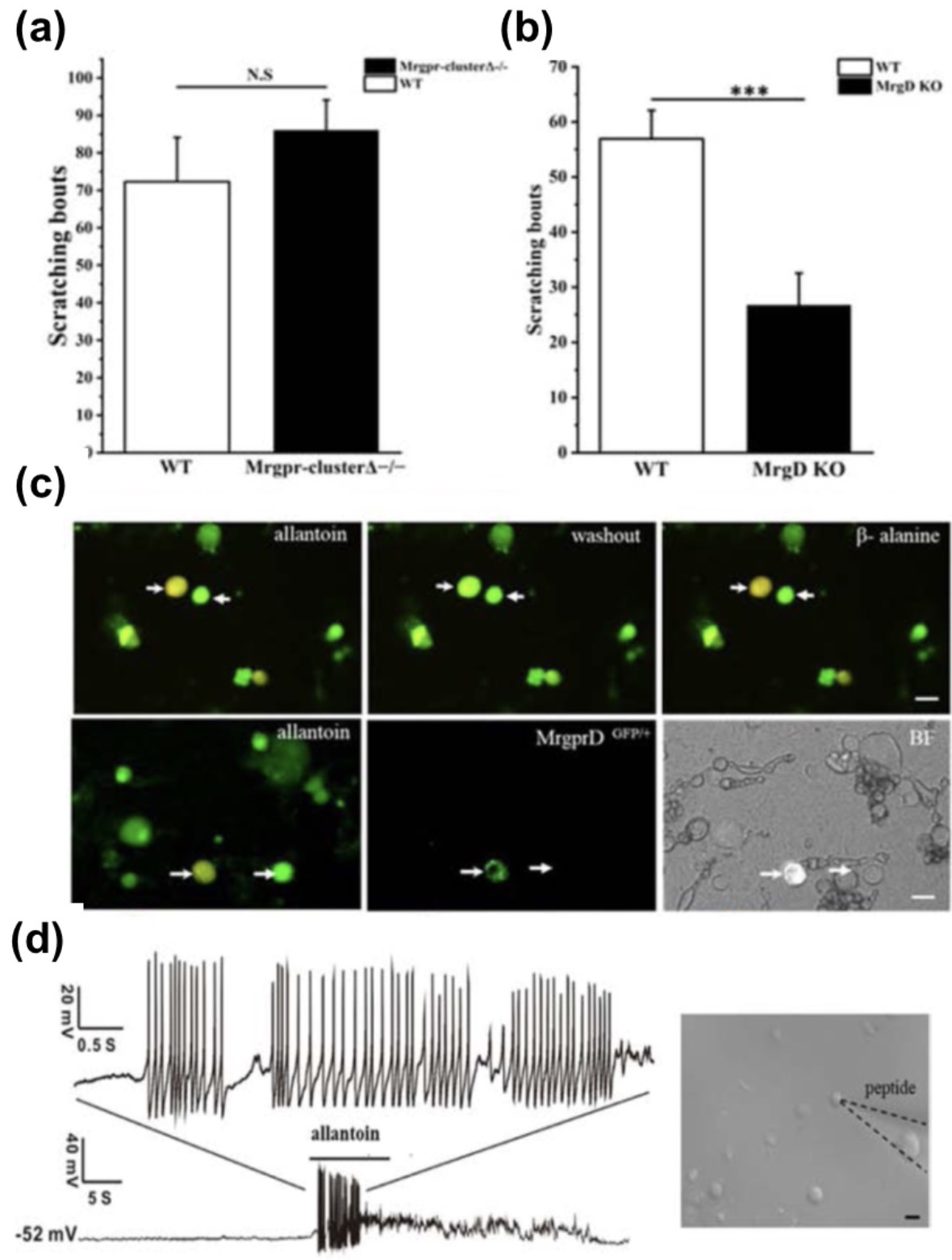
图3 尿囊素可以激活MrgprD阳性神经元
(图源:Yang, Y. et al., Journal of Cellular Physiology, 2003)

