动脉粥样硬化(atherosclerosis,AS)是一种慢性炎症性血管疾病,是冠心病的主要病理基础之一[1]。根据世界卫生组织(WHO)的数据,每年约有700万人死于冠心病[2]。随着人们的生活方式和饮食的变化,AS的发病率每年都在增加。然而,目前主流的治疗方案他汀类降脂药物仅能在临床实践中将冠心病事件减少约40%[3]。
体育活动和运动训练近年来被认为是降低心血管疾病(cardiovascular disease,CVD)风险的有效策略。尤其是,目前有证据支持运动训练和降脂药物的联合疗法优于单一药物疗法[4, 5]。临床试验证明他汀类药物和运动的联合疗法显著改善血脂异常并降低CVD的风险[4]。然而一方面,改善与AS相关的风险因素的最佳锻炼模式尚不清楚,另一方面,联合疗法被国家脂质专家小组建议存在一定患肌病的风险[6]。因此目前需要解决的问题有:1)寻找最佳的运动方式来降低患运动相关疾病的风险;2)寻找治疗AS的潜在靶点,进一步改善与弥补目前疗法的缺陷。
作者分别总结了有氧运动和无氧运动过程中关键的信号因子与信号通路。此外,作者阐述了运动强度,时间对不同信号通路的影响。此篇综述不仅辅助确定最佳运动方式,还为寻找治疗AS的潜在靶点进行展望,对临床实践中AS的预防和治疗提供了新思路。

AS进展过程中,扩血管效应的一氧化氮(NO)的积累减少和反应性降低导致内皮依赖性血管舒张功能障碍。有氧运动上调腺苷酸活化蛋白激酶(AMPK)导致下游级联的激活有效保护内皮功能。一方面,AMPK激活下游内皮型和神经元型一氧化氮合酶(eNOS&nNOS),导致内皮保护产物NO和H2O2的释放。另一方面,AMPK与过氧化物酶体增殖物激活受体d(PPARd)协同作用诱导肝脏和肌肉中耐力基因的转录,从而增加脂肪消耗率(图1)。此外,大量实验表明AMPK活动与运动强度成正比。尤其是在VO2峰值>60%的条件下,AMPK的磷酸化随着运动强度上升的增加幅度明显。然而,运动的持续时间对AMPK的影响似乎只基于极端的运动强度。
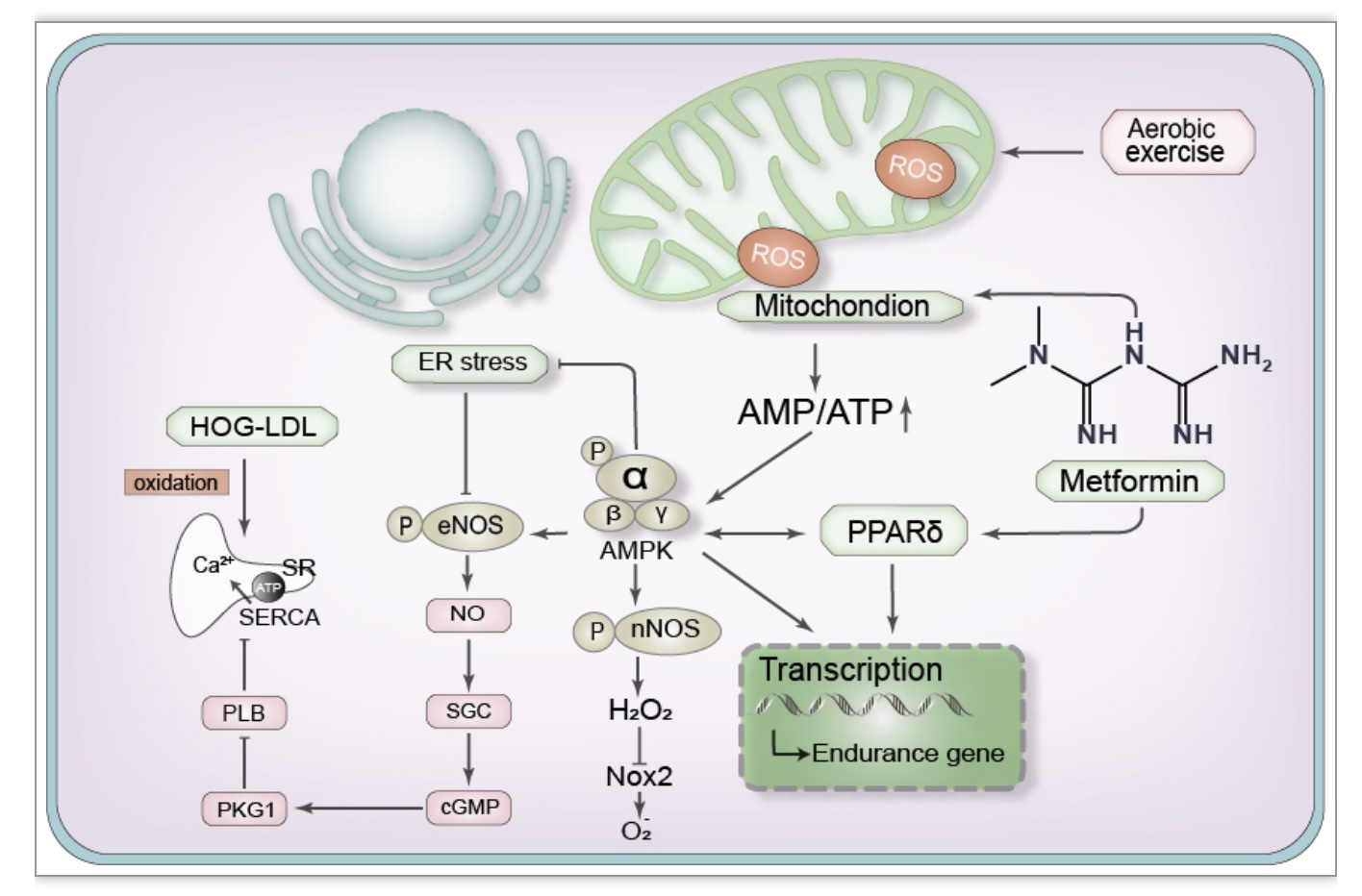
图1 有氧运动通过AMPK信号级联改善内皮功能障碍
(图源:Liu SB, et al., J Cell Physiol, 2023)
Sestrin蛋白(SESNs)通常被用作冠状动脉疾病临床评估的辅助指标。作者主要从SESN蛋白的三种同源物SESN1,SESN2和SESN3相关的信号通路评估有氧运动与AS之间的关系。SESN1诱导的AMPK的激活可以有效抑制哺乳动物雷帕霉素靶蛋白复合体1(mTORC1)。mTORC1的抑制可以阻滞NLRP3炎症体的激活、平滑肌增殖和M1型巨噬细胞促炎因子的释放,从而增加斑块的稳定性。SESN2主要通过上调自噬标志物诱导自噬,从而增加机体的胰岛素敏感性。SESN3通过mTORC2/Akt通路同样增加胰岛素敏感性。胰岛素敏感性的升高以及细胞葡萄糖摄取的增加近一步降低AS的风险(图2)。
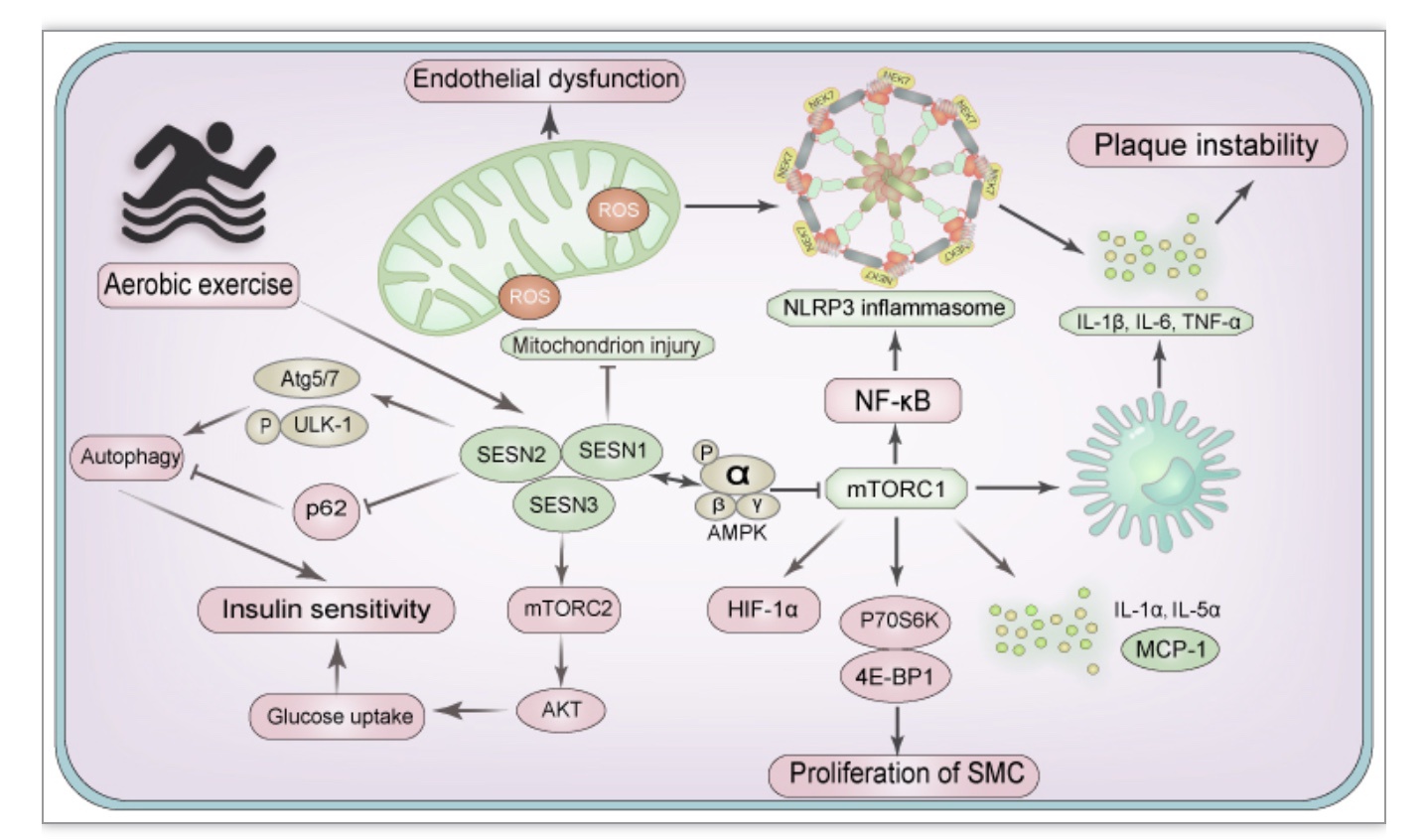
图2 有氧运动中SESNs的信号通路降低动脉粥样硬化风险
(图源:Liu SB, et al., J Cell Physiol, 2023)
有氧运动导致肝脏中成纤维细胞生长因子21(FGF21)敏感性升高,血清浓度先升高后降低。在有氧运动过程中,FGF21水平受到上游信号通路游离脂肪酸(FFA)-过氧化物酶体增殖物激活受体γ(PPARγ)轴的刺激。同时,FGF21下游受体脂联素(adiponectin,ApN)、FGFR1、FGFR2和β-Klotho蛋白(KLB)上调,促进FGF21的作用。此外,FGF21和过氧化物酶体增殖物激活受体γ共激活因子-1α(PGC-1α)相互作用以控制碳水化合物和脂质代谢。FGF21抑制NLRP3炎症小体诱导的各种生理反应,如炎症、细胞焦亡和氧化应激(图3)。
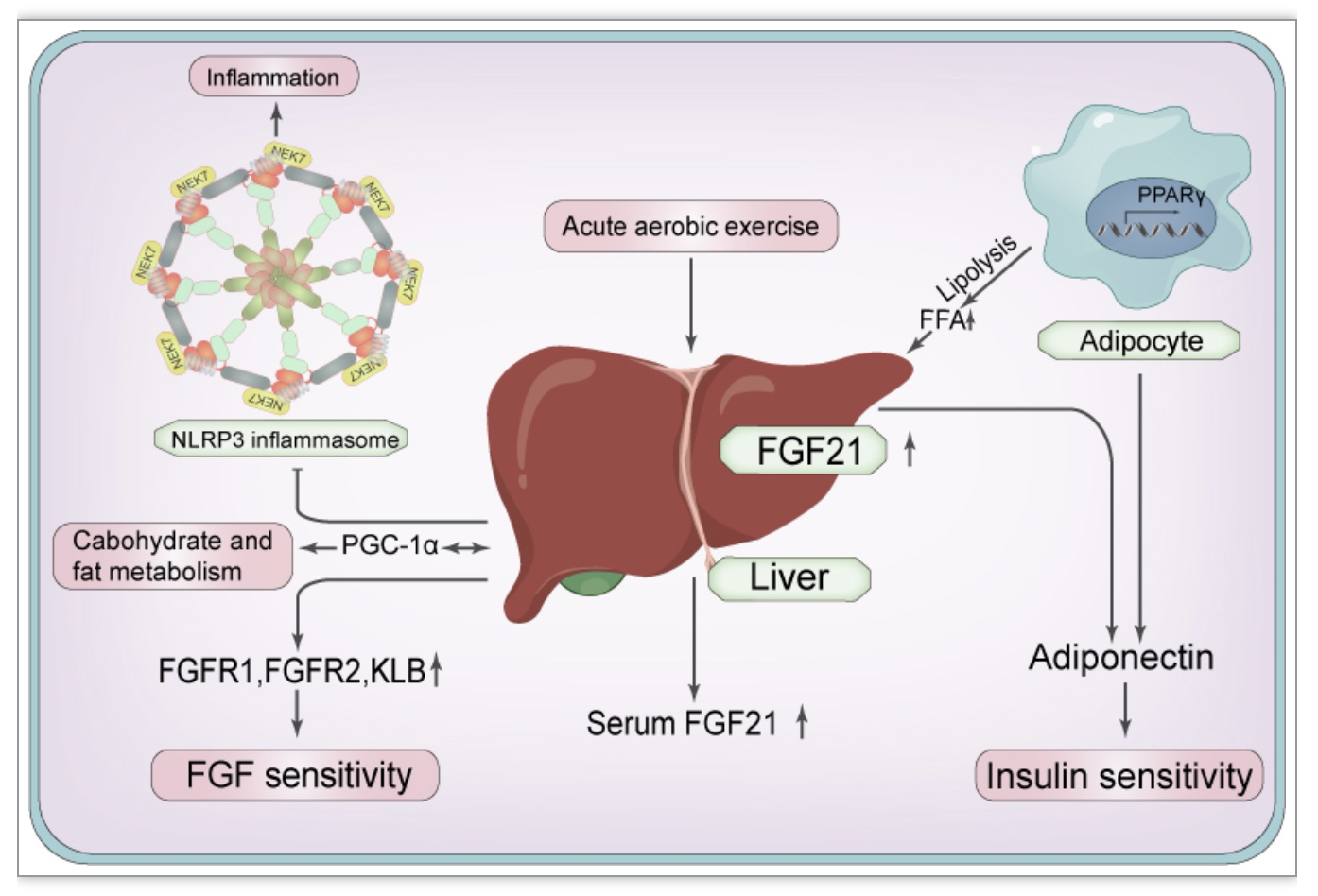
图3 有氧运动诱导的FGF21信号通路降低动脉粥样硬化风险
(图源:Liu SB, et al., J Cell Physiol, 2023)
许多微RNA(microRNA,miR)参与心血管生理和病理变化。作者总结了有氧运动过程中miR-146a、miR-492、miR-20a和miR126四种miRNA的关键信号通路。miR-146a负性调节TLR4-TRAF6炎症信号通路,起到内皮保护的作用;miRNA-492通过靶向抵抗素(resistin)而阻断STAT3-SOCS3-P-选择素(P-selectin)表达,从而改善胰岛素抵抗;miR-20a抑制磷酸酶和紧张素同源物(phosphatase and tensin homolog,PTEN)并激活PI3K/Akt信号通路;miRNA-126通过PI3K/Akt/eNOs轴刺激NO释放起到内皮保护的作用。
无氧运动的效应取决于运动的强度和持续时间。短期无氧运动会刺激内皮信号分子的释放,以进行血管保护。长期无氧运动可能会增加AS的风险,这与动脉粥样硬化斑块中缺氧诱导因子(hypoxia-inducible factor,HIF)的上调有关。HIF是由HIF-1α和HIF-1β组成的异二聚体蛋白,其中HIF-1α对缺氧快速反应,改变细胞的代谢过程,使细胞能够适应缺氧环境。HIF-1α的表达受到巨噬细胞表型或周围细胞环境和信号通路的影响,环境决定了HIF-1α发挥抗AS还是促AS效应。HIF-1α既可以促进THP-1巨噬细胞中载脂蛋白A1(ApoA1)的表达发挥抗AS效应,又可以促进向M1型巨噬细胞的极化发挥促AS的效应。然而,导致HIF-1α发挥不同效应的具体诱导因素需进一步研究。
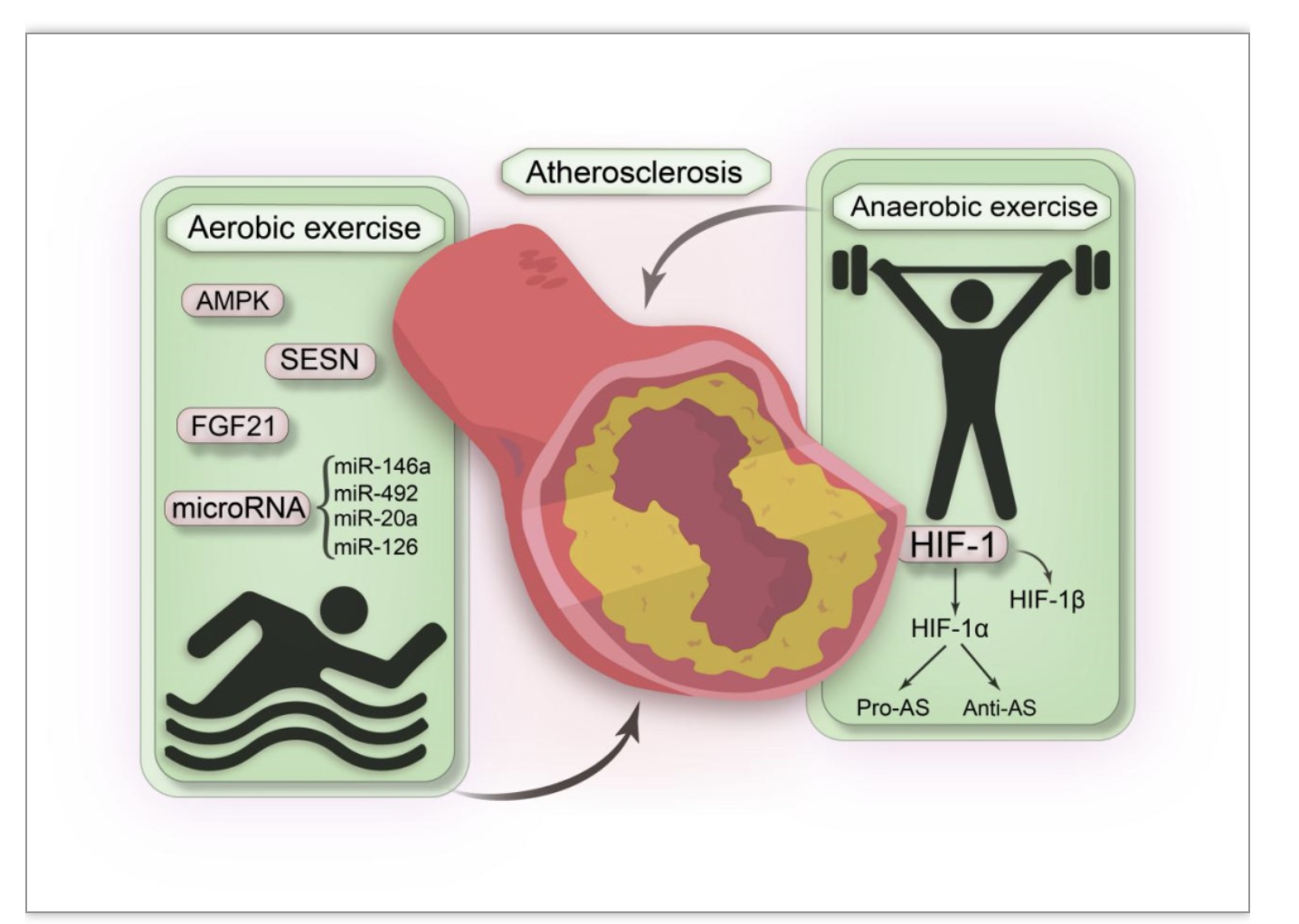
图4 有氧运动和无氧运动过程中的关键因子
(图源:Liu SB, et al., J Cell Physiol, 2023)
综上所述,有氧运动可以通过各种信号通路改善内皮功能以及潜在的危险因素。长期无氧运动可能会增加AS的风险,这与动脉粥样硬化斑块中HIF的上调有关;短期无氧运动可能会刺激内皮信号分子的释放,以进行血管保护。然而,由于研究的有限性,目前最佳的运动方式(强度,持续时间等)仍无法确定。本文总结的关键信号因子可作为未来AS治疗的潜在靶点(图4)。未来的工作将集中在基于动物模型和临床试验寻找AS的潜在治疗靶点。






