活性氧(reactive oxygen species, ROS)是氧气不完全还原时形成的化学物,其主要由细胞呼吸过程中的生化反应产生,并在卵巢健康扮演着双刃剑角色。生理条件下,这些ROS参与卵巢周期的调节,包括减数分裂的恢复、排卵、黄体的维持和消退等过程。然而,当ROS的生成和抗氧化防御系统之间的不平衡会导致卵巢疾病的发展。深入探究ROS参与卵巢疾病的机制,并探索潜在的抗氧化疗法以减轻其影响,这具有重要的临床意义。值得注意的是,几种具有独特ROS调节特性的策略,包括抗氧化药物、激素和间充质干细胞,已经被广泛研究并成为潜在的治疗方案。这里,对ROS影响卵巢疾病的机制及抗氧化疗法的前沿研究进行全面回顾与梳理。作者首先梳理了卵巢内ROS的产生和维持稳态的机制及其在卵巢的生理作用,并强调了ROS在卵巢疾病中的病理机制和潜在的抗氧化治疗策略,最后指明了未来研究方向。

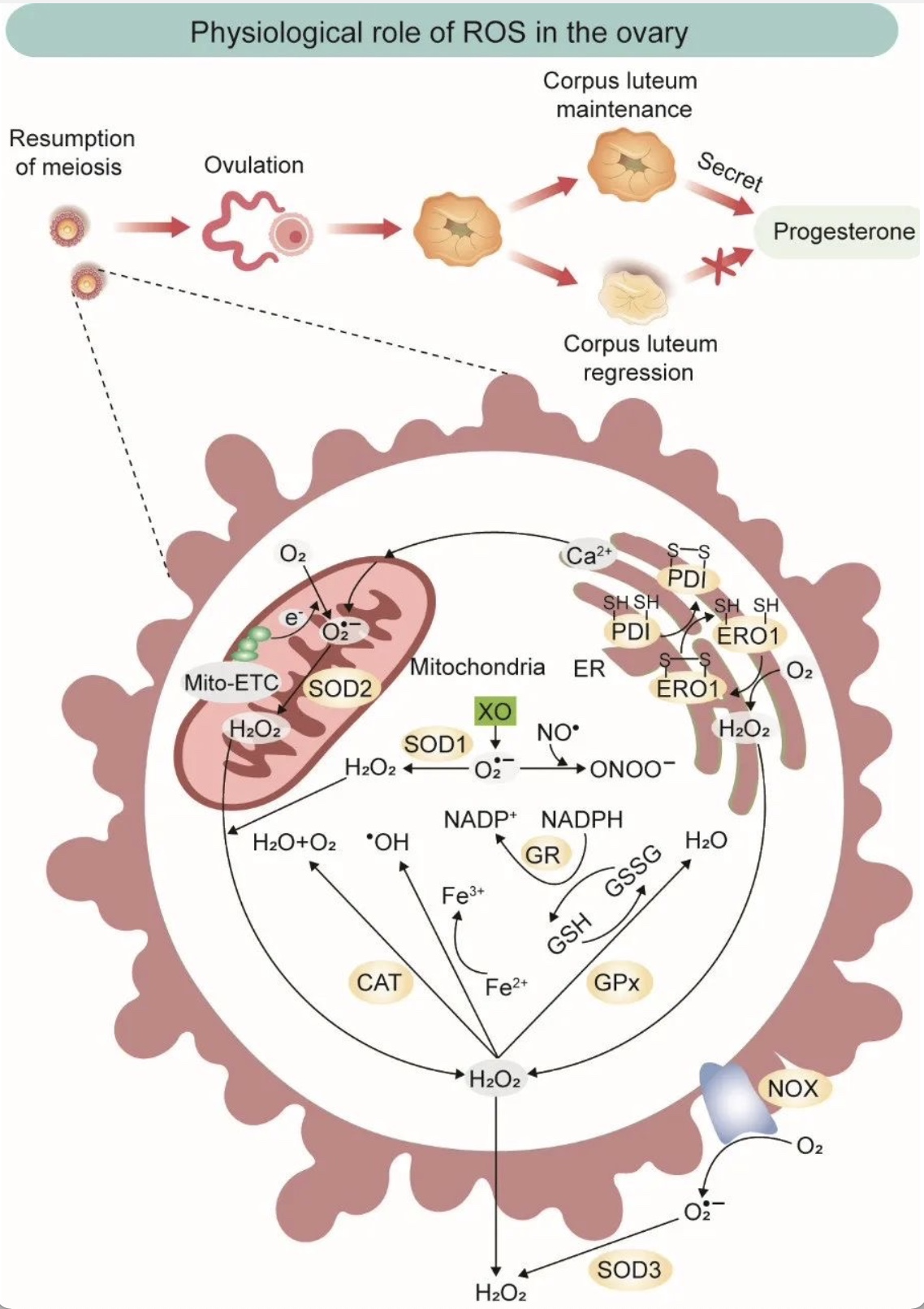
图1. ROS生成示意图
(图源:Liang, et al., Redox biology, 2023)
ROS能调节卵母细胞从生长到受精的多种生理功能,包括减数分裂、排卵、黄体维持和退化等过程。卵巢中氧化应激和抗氧化剂之间的相互作用非常复杂。在减数分裂过程中,ROS和抗氧化剂可以精确地调节卵母细胞减数分裂的停滞和恢复。每个月,只有一个优势卵母细胞完成减数分裂I,这过程中ROS水平增加,抗氧化酶的产生受到抑制。相反,减数分裂II需要抗氧化酶如CAT和SOD的保护。排卵是卵巢的最重要功能之一,排卵前卵巢会产生过量的ROS,促进排卵的发生[4]。排卵后形成的黄体可以产生孕酮。如果排卵后发生受精,孕酮在维持妊娠上发挥重要作用[5]。相反,排卵后未发生受精则需要黄体退化和孕酮水平的下降来为下一个生理周期的卵泡发育提供条件。ROS和抗氧化酶在调节黄体功能中起着重要作用。抗氧化酶SOD表达的增加增强了清除ROS的能力,从而延长了黄体的功能和孕酮的分泌。相反,在SOD活性降低的情况下,ROS会诱导黄体退化。通过这些步骤,ROS和抗氧化酶参与到卵巢周期的控制。

图2. ROS生成与抗氧化防御之间的不平衡
(图源:Liang, et al., Redox biology, 2023)
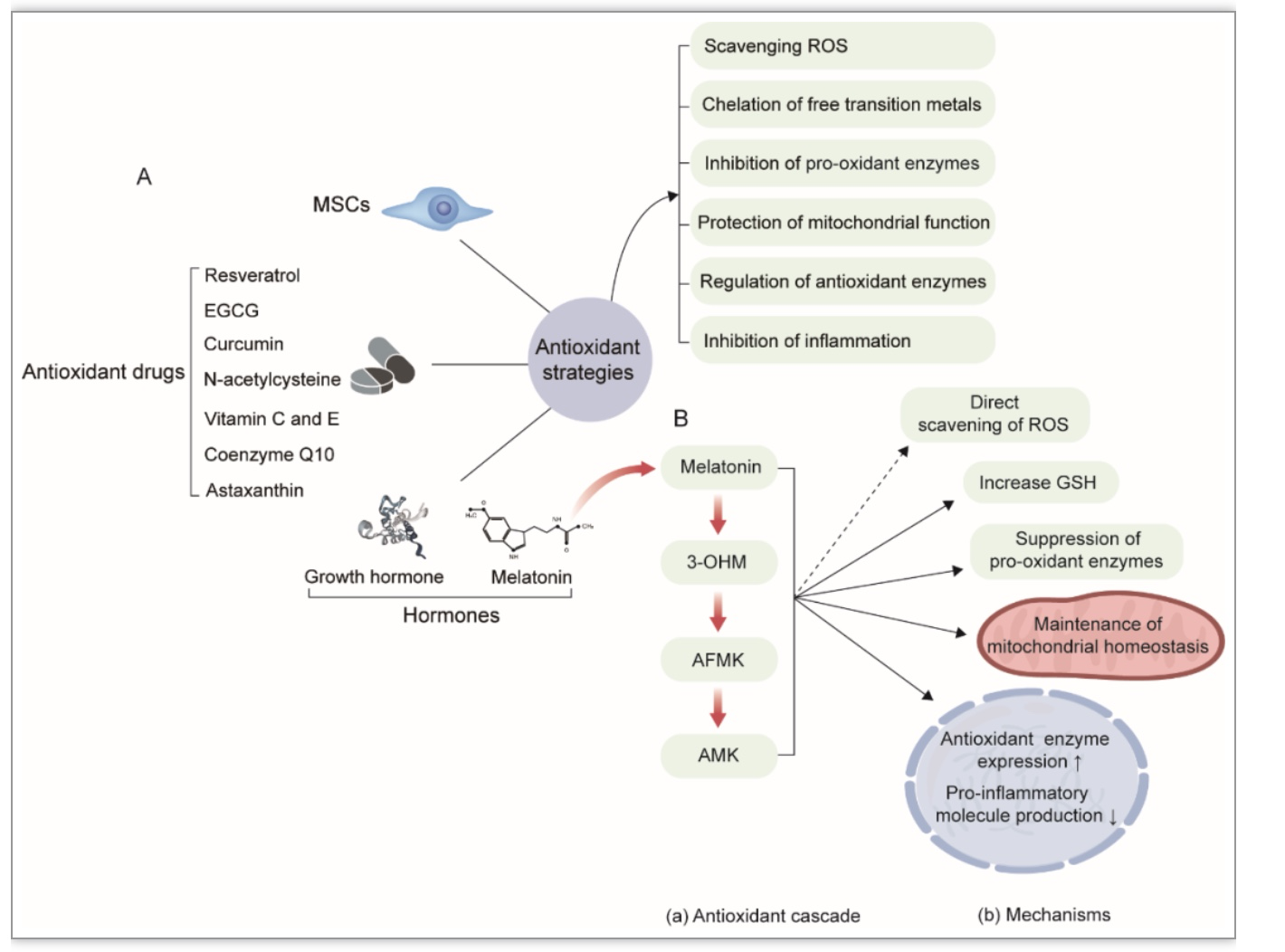
图3. 相关抗氧化机制
(图源:Liang, et al., Redox biology, 2023)
在本文中,作者系统梳理了卵巢内ROS的产生、稳态、生理作用、病理作用及抗氧化策略的前沿研究。这些抗氧化治疗策略在动物和临床试验中展示出光明的应用前景。然而,这些新策略也意味着需要解决新问题。这些抗氧化策略转化为临床应用仍然存在巨大挑战。抗氧化治疗的效果受到ROS在卵巢疾病中发挥作用程度的限制[9]。因此,在应用抗氧化策略之前,有必要确定ROS是否在卵巢疾病的发展中起关键作用。其次,抗氧化策略也存在包括生物利用度低、氧化还原调节能力弱等问题。这些问题的实质性突破将为卵巢疾病的治疗做出重大贡献。

