细胞外囊泡(EVs)可从几乎所有组织和细胞脱落,通过循环体液在细胞间传递信号和效应分子,是医学诊断和治疗的重要来源。目前,EVs主要分为来自核内体的外泌体(30-150 nm),自质膜出芽形成的微囊泡(150-1000 nm),以及凋亡过程中释放的凋亡小体(200-5000 nm)(1, 2)。尽管EV亚群均具脂质双层结构,但包括蛋白质、RNA和代谢物在内的货物会被选择性地包装到EV亚群中,并在胞间通讯中发挥不同的作用。因此,了解EV组成和生物功能的异质性对其发展为临床生物标志物和治疗载体至关重要。
眼泪是可反映内在情绪与疾病的重要载体。诊断学中,作为维持和保护眼健康的流动屏障,泪液也被认为是与血液类似的、可靠的液体活检样本源。更重要的是,泪液分析的价值可以扩展到眼部系统之外。这是由于泪液分享了大量从循环系统中过滤而来的成分,因此携带了众多看似与之无关的其他身体器官的丰富生物信息(3)。然而,虽然已有诸多工作启动了对细胞培养液、血浆和尿液来源EV亚群的分子谱解析,但关于泪液EV及EV亚群的组织学溯源和生物学网络仍有待揭示。

研究者们首先从健康人的泪液样本中分离具备不同粒径范围、蛋白标志物及形貌特征的泪液EV亚群,并将其定义为小尺寸EV(20-100 nm)、中尺寸EV(100-200 nm)和大尺寸EV(200-450 nm)。通过蛋白检测和组学分析,发现所有亚群均富集了具有囊泡介导转运功能的蛋白组分,但外泌体生物发生相关的成分会优先加载至中等尺寸EV,同时,该EV亚群的蛋白组织学来源和生物学功能与视网膜稳态的维持以及炎症调节密切相关。
为全面了解泪液EVs与人体的相互作用网络,研究者们基于HPA数据库(Human Protein Atlas)蛋白溯源分析进一步展示了泪液EV强大的蕴藏力:包括眼/脑/淋巴组织以及神经/血液/免疫细胞在内的多种组织或细胞相关蛋白,可在泪液EV中被检测并呈现一定程度EV亚群选择性(图1)。
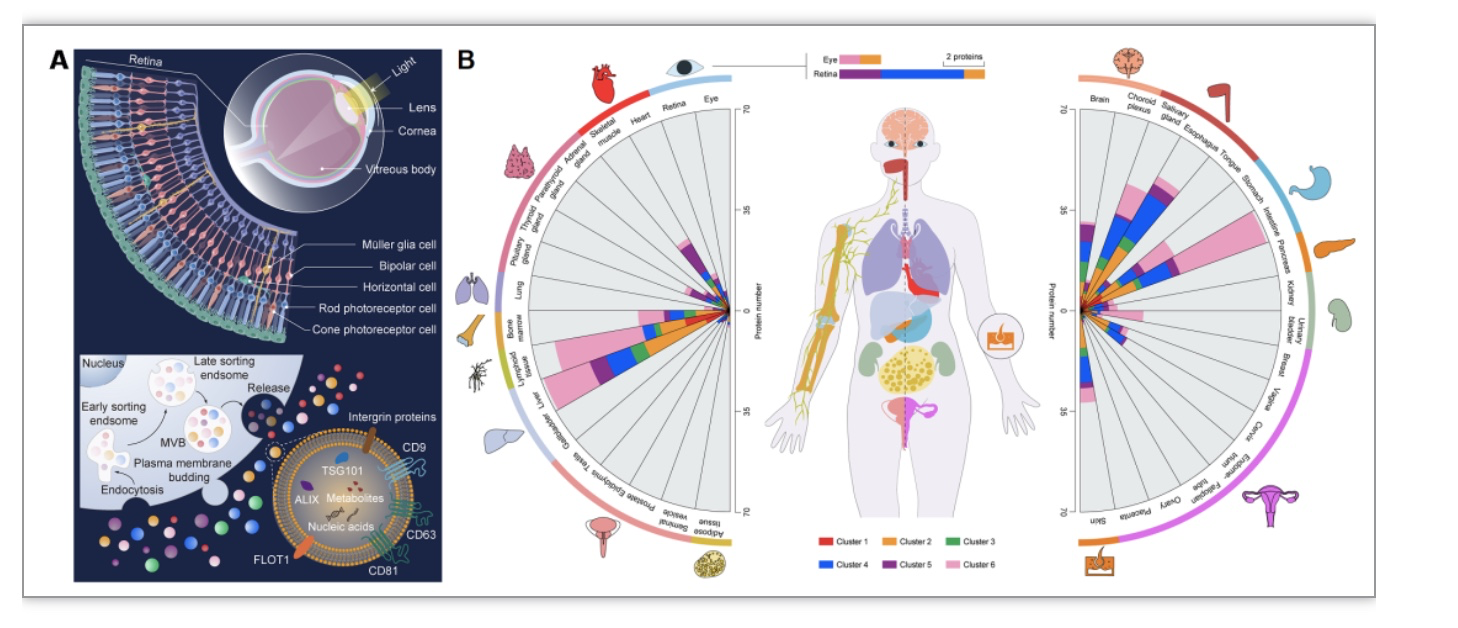
图1泪液EV亚群与组织溯源分析
(图源:Hu, et al., Science advances, 2023)

