膝关节软骨是由少量的软骨细胞和大量的细胞基质组成的透明软骨,且由于其缺乏血管和神经,受损后很难自行恢复[1]。目前临床上的治疗方式并不能很好地恢复正常的软骨结构和重建软骨功能[2,3]。在组织工程领域,水凝胶支架的开发对软骨缺损的修复具备很大优势。近年来,微流控技术、3D打印技术和静电纺丝等技术已广泛应用于软骨组织工程[4,5],但是结合微观和宏观角度以模拟软骨组织解剖学特点的3D打印多尺度复合支架鲜有报导。开发多尺度复合支架用于修复软骨损伤依然是一个很大的挑战。
近日,南方医科大学基础医学院教授课题组合作在iScience上发表了题为“A modular hydrogel bioink containing microsphere-embedded chondrocytes for 3D-printed multiscale composite scaffolds for cartilage repair”的研究。该研究通过集成微流控技术和3D打印技术的新型生物综合策略制备多尺度复合支架;其中,含细胞的水凝胶微球“生物墨水”经过冻存再复苏培养,其内部细胞仍保持较高的生物活力。该复合支架能够精确模拟人体软骨组织的微观环境和宏观环境促进软骨组织再生。

作者团队先前所设计的石英管微流控芯片在制备微球过程中容易发生堵塞,芯片使用寿命有限。因此为了提高芯片的使用寿命和微球的生产率,课题组建立了多通道微流控芯片的模型并通过微型3D打印机制备(图1A, B)。此外,水凝胶微球的粒径会明显影响包裹在微球内部的细胞的活力,因此,控制所制备的微球的粒径显得十分重要。该芯片可通过改变水相溶液和油相溶液的流速比值,可大批量制备粒径可调控的水凝胶微球(图1C)。通过扫描电子显微镜可以观察到微球的表面特征(图1D),微球呈现为尺寸均一且分散性良好的特点。
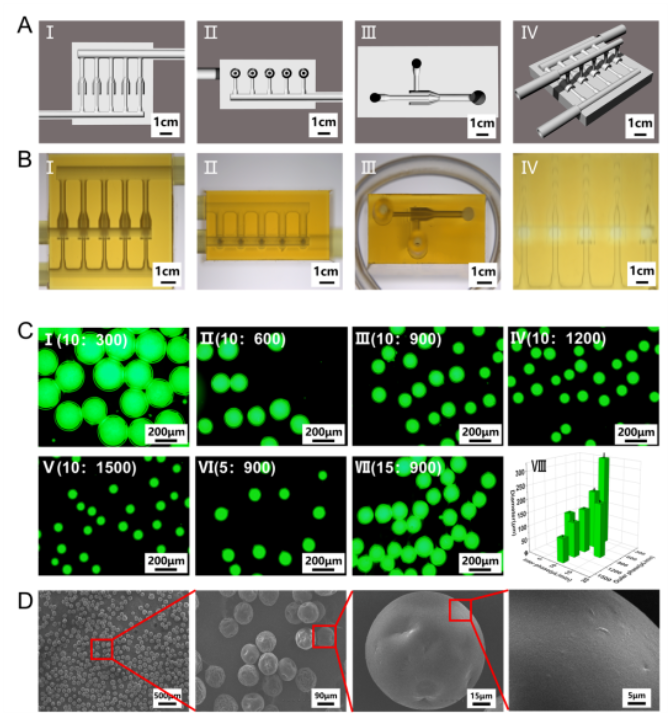
图1. 微流控芯片模型的示意图,以及不同直径的微球的形态分析。
为满足模块化生物墨水用于3D打印的含细胞微球的数量要求,课题组对含有细胞的凝胶微球进行了冻存处理,待使用时再进行复苏处理。课题组探究了冻存再复苏的处理对微球内软骨细胞的生物学行为的影响;其中,含软骨细胞的微球直接进行培养作为对照组,含软骨细胞的微球进行冻存再复苏后培养作为冻存组,分别对这两组样品进行了细胞活力测试、细胞增殖能力测试和蛋白分泌能力测试(图2)。结果发现对照组和冻存组之间的软骨细胞的存活率、细胞增殖能力和蛋白分泌能力没有显著差异,这为后续需要足量的含细胞微球用于制备多尺度复合水凝胶支架做准备提供了保障。
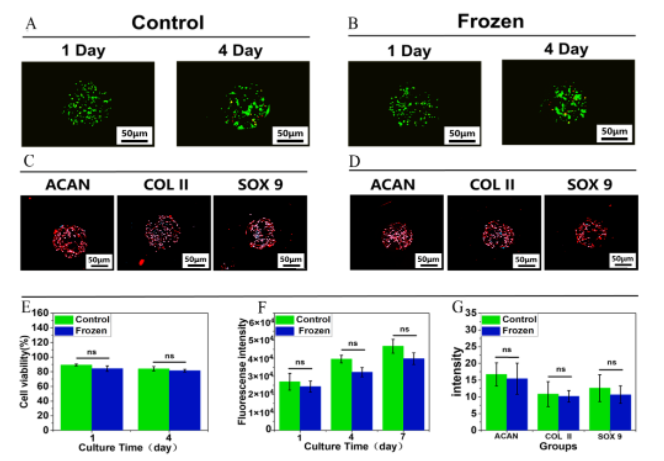
图2. 负载软骨细胞的微球的生物学性能表征。
课题组以混合含细胞微球的水凝胶模块化生物墨水为基础,通过3D打印机制备了负载含细胞微球的多尺度复合支架。该支架不仅可为微球内封装的细胞提供了类似细胞外基质的三维微环境以促进其生长、增殖和分泌蛋白,且可促进组织成熟分化以修复组织损伤和功能重建。为了观察微球在复合支架中的分布,课题组用异硫氰酸荧光素(fluorescein isothiocyanate, FITC)将微球染成绿色,用罗丹明将水凝胶前体溶液染成红色。体显微镜可以观察到微球是散在地分布于复合支架中;此外,结果可以看到复合支架中可负载大量的微球(图3B,C)。微球内的细胞是以一种团聚的形式存在复合支架中(图3D),这也是仿生了人体膝关节软骨的软骨陷窝结构。因此,多功能模块化生物墨水所制备的多尺度复合支架整合了细胞生长的微观环境和宏观环境,使得其在软骨组织损伤修复和再生的医学领域中成为了一种具有巨大潜力的治疗方法。

图3. 多尺度复合支架的表征。
为了进一步确定多尺度复合支架在体内具备促进软骨再生的能力,研究人员将复合支架植埋在裸鼠的皮下组织,并于不同时间进行取材和免疫组织染色(图4)。结果发现,复合支架内的软骨细胞在裸鼠皮下均分泌基质蛋白。此外,支架内的软骨细胞所沉积的一型胶原基质蛋白明显高于二型胶原基质蛋白,这说明了复合支架呈现透明软骨分化趋势而非纤维软骨。因此,多尺度复合支架在软骨组织损伤的临床治疗中具有广阔的应用前景。

图4. 多尺度复合支架的体内软骨再生的研究。

