高达70%因心绞痛症状接受侵入性冠状动脉造影(CAG)的患者并未发现阻塞性冠状动脉疾病,其中很大一部分患者的症状由INOCA造成[1]。最新研究表明,INOCA是一类强异质性疾病,相较无缺血性心脏病的正常人群,主要不良心血管事件(MACEs)和全因死亡风险增加[2],后续卫生经济学负担也大幅上涨[3]。冠脉微循环障碍(CMD)是INOCA主要致病机制,可通过诱发心肌血流量(MBF)和冠脉血流储备(CFR)减低导致MACEs发生。因此精准评估CMD并建立INOCA患者的精准预后体系必要且紧迫。
PET-CT已被证实可精准评估CMD,其衍生的MBF和CFR在INOCA患者中具有较高的预后价值[4],但受限于难以获取的显像药物和昂贵的检查费用,临床实践中很难广泛推广。目前,最新心脏专用机碲锌镉(CZT)-SPECT血流定量技术有望为评估CMD提供新工具。相较于普通碘化钠(NAI)-SPECT,可提供8-10倍灵敏度、2倍空间分辨率[5],且显像药物易获取、检查费用低,已被证实与PET-CT在评估CMD方面具有良好的一致性[6]。但CZT-SPECT血流定量技术在INOCA患者中的预后价值尚未阐明。该研究证实了CZT-SPECT血流定量技术可用于INOCA患者精准预后预测,弥补了SPECT层面上INOCA患者最佳预后阈值的空白,定义了全新的INOCA患者CZT-SPECT预后指标体系,有望为临床医生提供新的诊断策略和预后监测手段,对INOCA患者的诊疗模式遴选具有重要意义。

作者回顾性分析了118例行CZT-SPECT血流定量技术检查的INOCA患者,经过中位随访时间15个月,19例(16.1%)病人发生了MACEs,且 MACEs组的负荷心肌血流量(sMBF)、CFR及部分心肌灌注显像半定量参数均低于非MACEs组。此外涉及CMD的大部分研究仍将PET-CT-CFR<2作为诊断和预后评价的阈值标准,SPECT层面上针对INOCA患者的个性化精准阈值仍属空白。结果表明预测INOCA患者MACEs的最佳阈值为CFR<2.52(敏感性84.2%,特异性77.8%,AUC 0.83,p<0.0001)(图1a),sMBF<3.16(敏感性84.2%,特异性79.8%,AUC 0.86,p<0.0001)(图1b),并且K-M生存曲线提示该阈值具有优秀的危险分层价值,CFR (log-rank=16.92, p<0.0001)(图2a),sMBF (log-rank=28.61, p<0.0001)(图2b),证实了CZT-SPECT血流定量技术在INOCA患者中具有较强的预后价值。

图1. INOCA患者sMBF和CFR预测阈值
(图源:Zhang H, et al., EJNMMI, 2023)
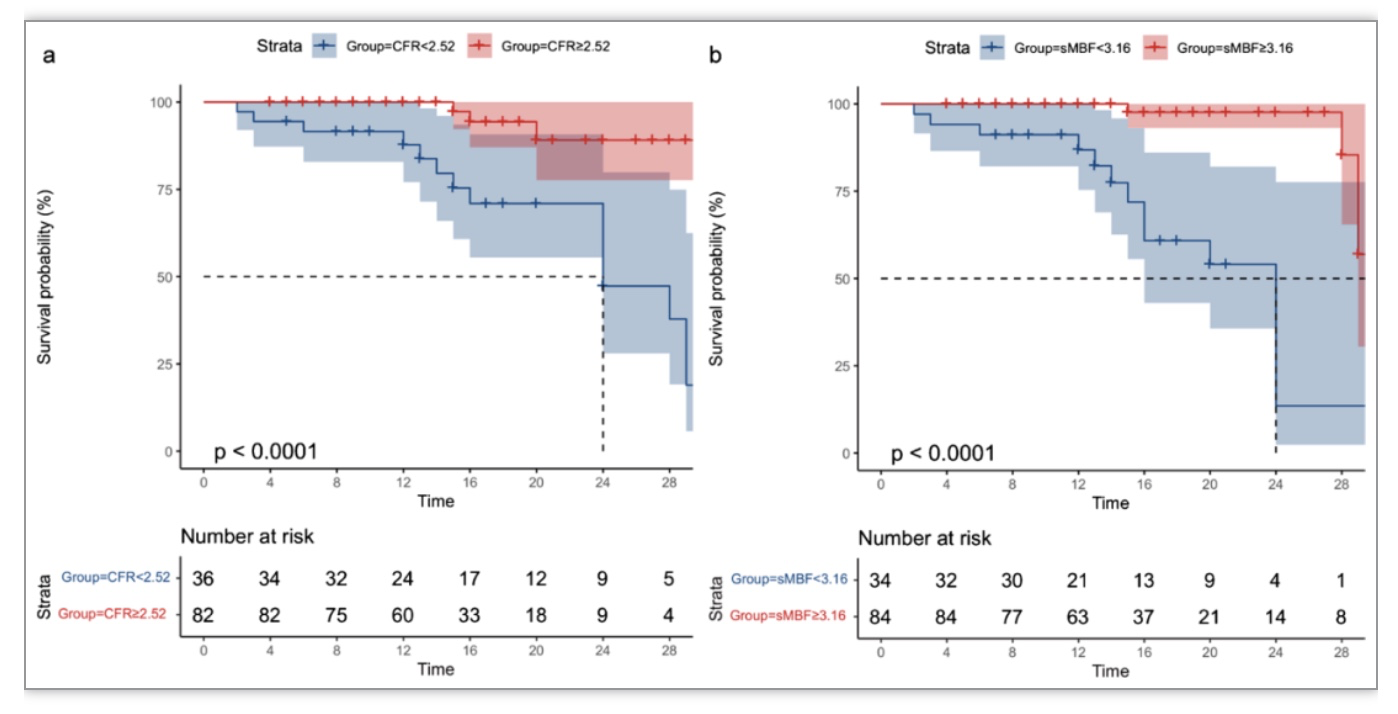
图2. 基于风险阈值的K-M生存曲线
(图源:Zhang H, et al., EJNMMI, 2023)
作者进一步探索了SPECT层面上sMBF和CFR两种指标在预后价值体系中的权重。首先根据sMBF和CFR的一致性,将118例INOCA患者分为四组:第一组(CFR<2.52, sMBF<3.16,n=19, MACEs%=58.0%);第二组(CFR<2.52, sMBF≥3.16, n=17, MACEs%=21.0%);第三组(CFR≥2.52, sMBF<3.16, n=15, MACEs%=21.0%);第四组(CFR≥2.52, sMBF≥3.16, n= 67, MACEs%=0.00%)。K-M生存曲线提示CFR和sMBF均受损与单独sMBF受损预后无明显差异(log-rank= 0.075, p = 0.78),但单独sMBF受损较单独CFR受损预后差(log-rank = 4.01, p = 0.04)。

图3. INOCA患者4种亚组的K-M生存曲线
(图源:Zhang H, et al., EJNMMI, 2023)
其次作者基于Cox多因素回归分析筛选出的变量构建了5种预后模型,通过计算模型一致性指数(C-index)证实纳入CFR无法提升模型预测能力,而纳入sMBF(C-index=0.92)则比CFR(C-index=0.86,p=0.022)有更显著的预后价值递增(表1)。
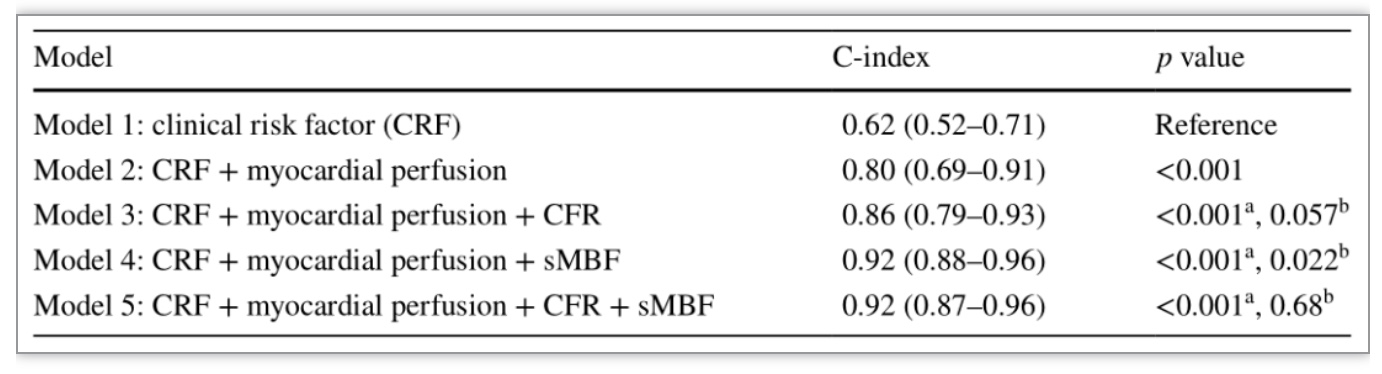
表1. 五种预后模型C-index比较
(表源:Zhang H, et al., EJNMMI, 2023)
最后作者通过净重新分类指数(NRI)及综合判别改善指数(IDI)全方位展示两种指标对预后模型改善情况。最终结果证实了sMBF(NRI = 0.19; IDI = 0.10)可为INOCA预后模型提供更显著的改善效能,并且sMBF和CFR预后价值均显著超过常规半定量心肌灌注显像参数(表1-2)。

表2. 五种预后模型NRI和IDI比较
(表源:Zhang H, et al., EJNMMI, 2023)

