细菌性阴道炎(BV, Bacterial Vaginitis)是世界范围内最常见的阴道感染,与早产、性传播感染和人类免疫缺陷病毒的获得和传播等重大公共卫生问题有关[1]。根据一项全球调查,超过70%的女性以前曾经历过阴道问题,并曾用药物治疗过这些感染。造成BV的主要原因是阴道微生物群的不平衡和其他潜在的相关[2]。在女性阴道中存在的多种微生物可以形成一个稳定的菌群生态平衡,其中阴道环境发生改变会影响菌群的平衡,引起菌群失衡[3-4]。在临床上主要通过服抗生素等药物缓解症状,只能起到缓解的作用,仍然存在较高的复发率[5]。对于持续性和复发性的BV人群,目前存在的治疗方法十分有限,急需探究新的、高效的BV治疗途径。而我们本篇文章以一个新的治疗策略来调节阴道菌群,从而达到治疗效果。本研究探究了合成菌群移植治疗加德纳菌所引起的细菌性阴道炎小鼠疾病,从免疫系统以及阴道菌群两方面阐述了合成菌群治疗细菌性阴道炎疾病的机制,为临床试验提供了理论依据。

细菌性阴道炎是一种由阴道菌群失调引起的疾病。阴道生态失调的特点是阴道微生物群紊乱,并与各种妇科疾病有关。由于其高复发率,迫切需要开发有效的治疗药物。本研究通过从健康女性阴道分泌物中分离筛选出抑制加德纳菌株生长的益生菌菌株,并将筛选到的菌株组成合成菌群,将合成菌群移植在体内验证其有效性,多角度探究合成菌群移植改善细菌性阴道炎疾病的机制。
本实验从五名健康女性阴道分泌物的样本中进行分离、纯化鉴定出能够抑制加德纳菌生长的乳酸菌,使其成为治疗细菌性阴道病的有前途的候选菌株。其次,通过建立细菌性阴道炎模型,研究阴道菌群移植或合成菌群移植(含卷曲乳杆菌、植物乳杆菌、唾液乳杆菌和鼠李糖乳杆菌)对阴道菌群失调的影响。实验结果表明,合成菌群移植(Synthetic Bacterial Consortia Transplantation, SBCT)和阴道菌群移植(Vaginal Microbiota Transplantation, VMT)治疗后细菌性阴道炎小鼠阴道内G. vaginalis的载菌量减少。通过H&E染色验证了菌群移植治疗能在一定程度上恢复阴道上皮细胞损伤。治疗两周后,SBCT组小鼠体内的促炎细胞因子(IL-1β和IL-8)分泌减少,抑制NF-κB活化。小鼠阴道组织中IL-17、iNOS、COX-2表达下调,IL-10、Foxp3表达上调。
此外,本次还重点研究了合成菌群移植和阴道菌群移植对微生物组的多样性和结构的影响,以及微生物组的变化与其预测功能之间的可能关系。从alpha-多样性和ß-多样性的分析来看,治疗后菌群的微生物多样性在一定程度上有所恢复以及菌群结构更相似且稳定。并且将受干扰的阴道菌群恢复到正常水平(乳酸菌增多,埃希菌减少),有效避免阴道菌群失调的复发。通过同源基因簇(COG)的方法进一步分析,BV相关样本中活跃的基因表达表明,微生物群的联合促进了基因表达机制。综上所述,合成菌群移植和阴道菌群移植可有效调节细菌性阴道炎小鼠对先天和适应性免疫反应,并通过促进乳酸菌生长和抑制病原体生长来维持阴道菌群平衡。
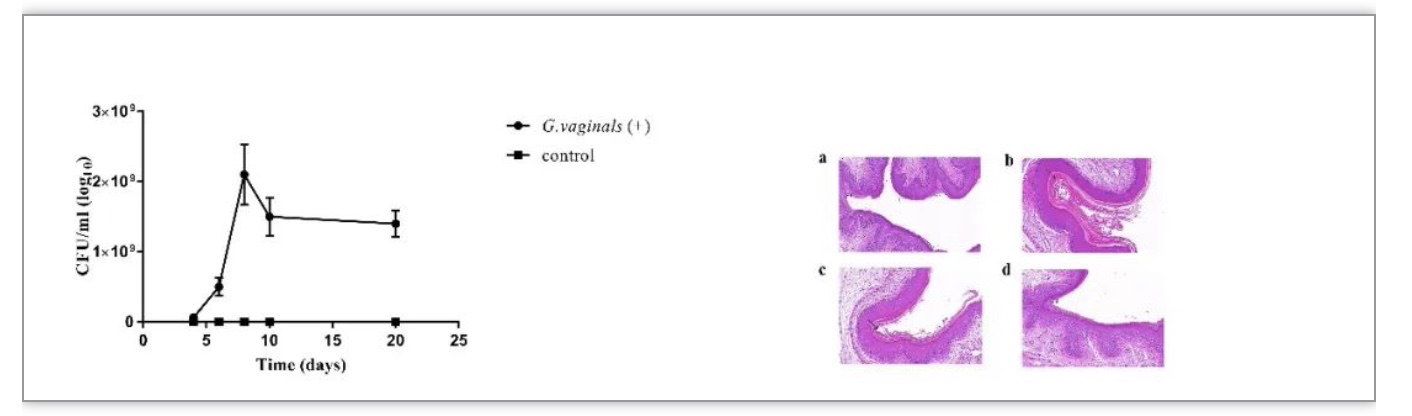
图1. 在第4、6、8和21天纵向评估阴道灌洗液中的细菌负荷与细菌性阴道病小鼠的组织病理学分析
(图源:Li, et al., Microbiome, 2023)
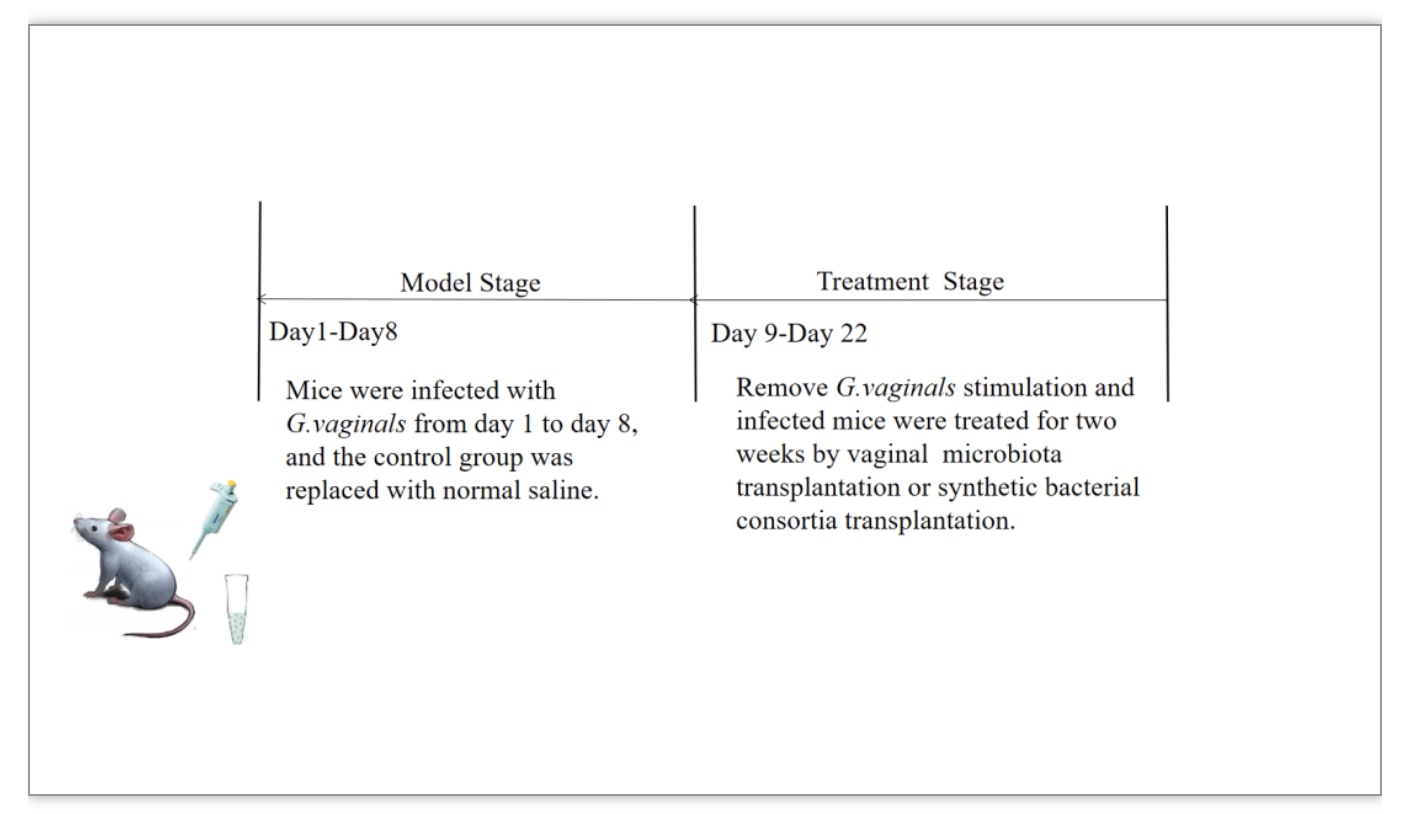
图2. 合成细菌联盟移植和阴道微生物群治疗阴道生态失调的实验方案
(图源:Li, et al., Microbiome, 2023)
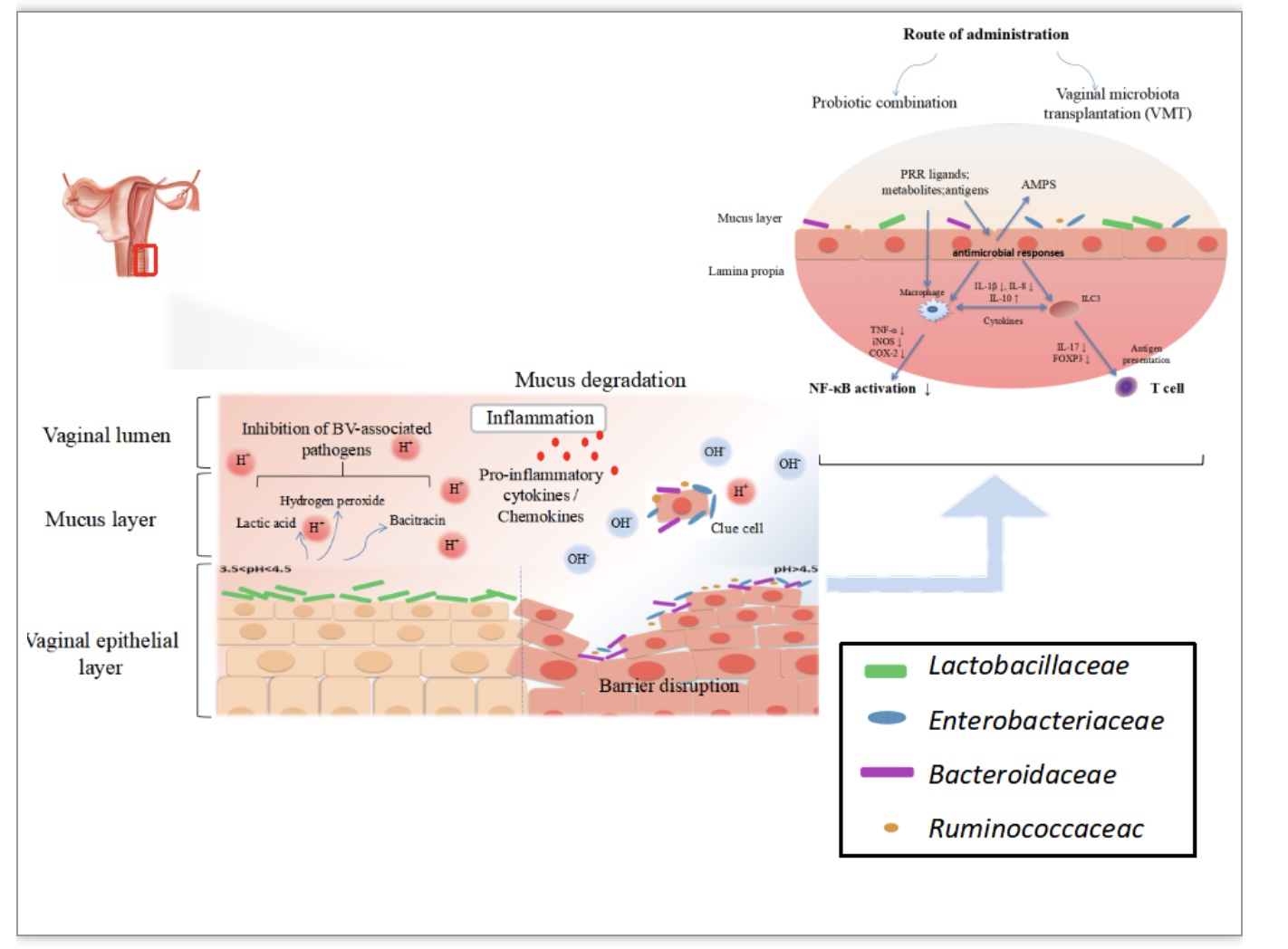
图3. 工作机制图
(图源:Li, et al., Microbiome, 2023)
细菌性阴道病的常规抗生素治疗导致了细菌耐药的加速过程,而益生菌是治疗细菌性阴道病的潜在替代方法。通过实验证明,合成菌群菌群能有效改善细菌性阴道炎疾病,合成菌群移植有可能作为治疗G. vaginalis感染引起的细菌性阴道病的潜在生物治疗剂。

