过氧化物酶体是几乎存在于所有真核细胞中的带膜细胞器,是一种很重要的代谢细胞器,内含有一种或多种氧化酶和过氧化氢酶[1]。由内质网产生,或通过线粒体和内质网来源的囊泡融合而产生。过氧化物酶体不仅在脂质的合成和转化中有重要作用,还能调节活性氧(reactive oxygen species, ROS)、活性氮,通过这些调节可减少机体的氧化损伤[2]。过氧化物酶体功能障碍或受损会导致机体的代谢障碍或氧化应激损伤。因此设计和开发人工过氧化物酶体(Artificial peroxisomes, APEXs)可用于疾病的诊断和治疗[3]。研究者们将天然酶、人工酶用细胞膜包裹合成APEXs,但对于其具体特点和应用仍缺乏系统的研究综述进行评价。因此,深入探讨并总结APEXs的特点和生物医学应用具有重要的临床意义。

一、APEXs中的催化剂
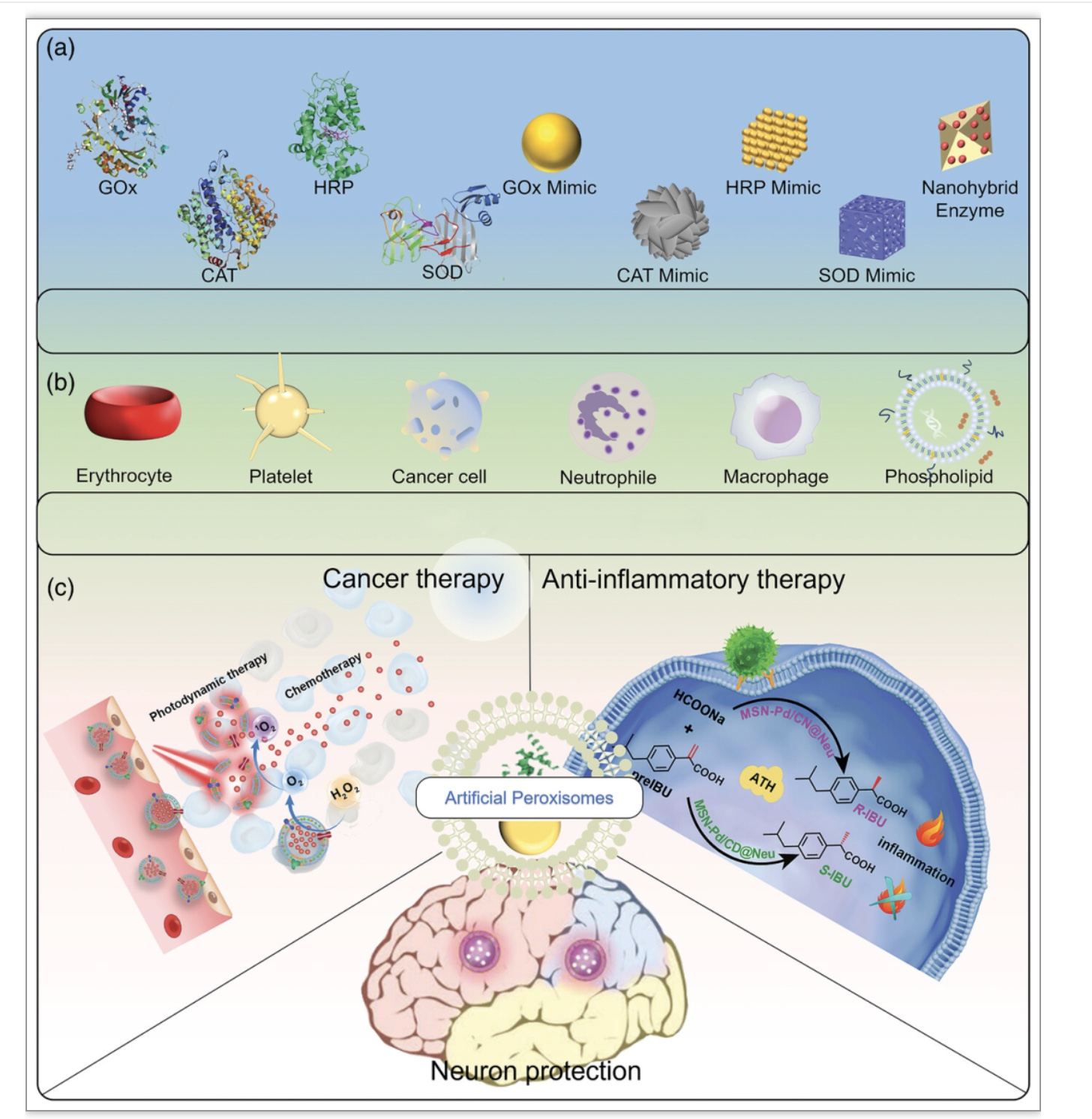
图1. APEXs的壳核结构和生物医学应用
虽然天然酶和生物大分子具有很高的催化活性和选择性,但却存在大量的内在局限性。尽管研究人员可通过生物矿化、脂质体包衣和与树突状分子结合等方式提高天然酶的稳定性,但天然酶的高成本、难回收等缺点限制了天然酶的应用,从而刺激了人工酶即模拟酶催化剂的出现和发展。模拟酶催化剂具有稳定性好、成本低以及纳米材料的其他特性,已成为生物医学领域用于疾病诊断和治疗的有前景的工具。作者介绍了分别模拟四种天然酶的模拟酶催化剂,即GOx模拟酶、POD模拟酶、CAT模拟酶、SOD模拟酶。和天然酶一样模拟酶催化剂可用于疾病的诊断和治疗,且通过调节活性中心可同时具有多酶活性。
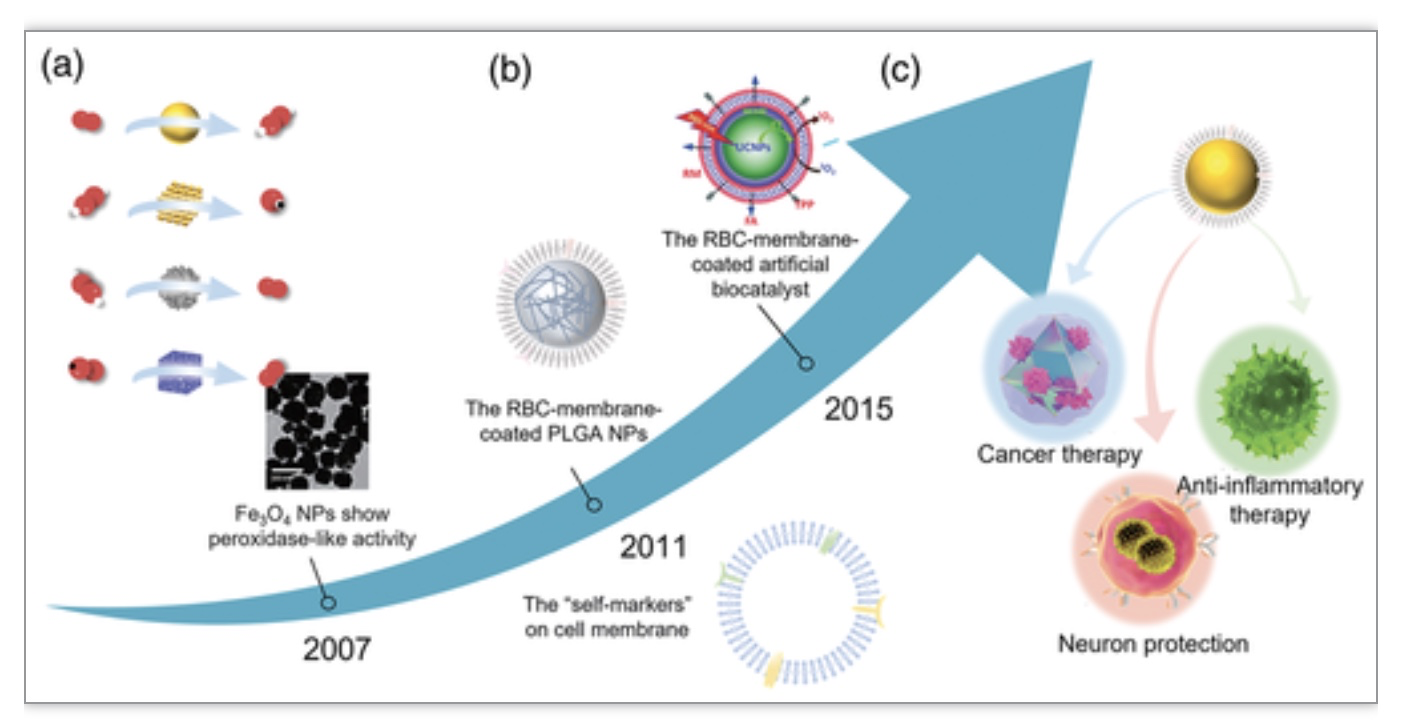
图2. 仿酶制剂和APEXs的发展历程
二、APEXs外层的细胞膜
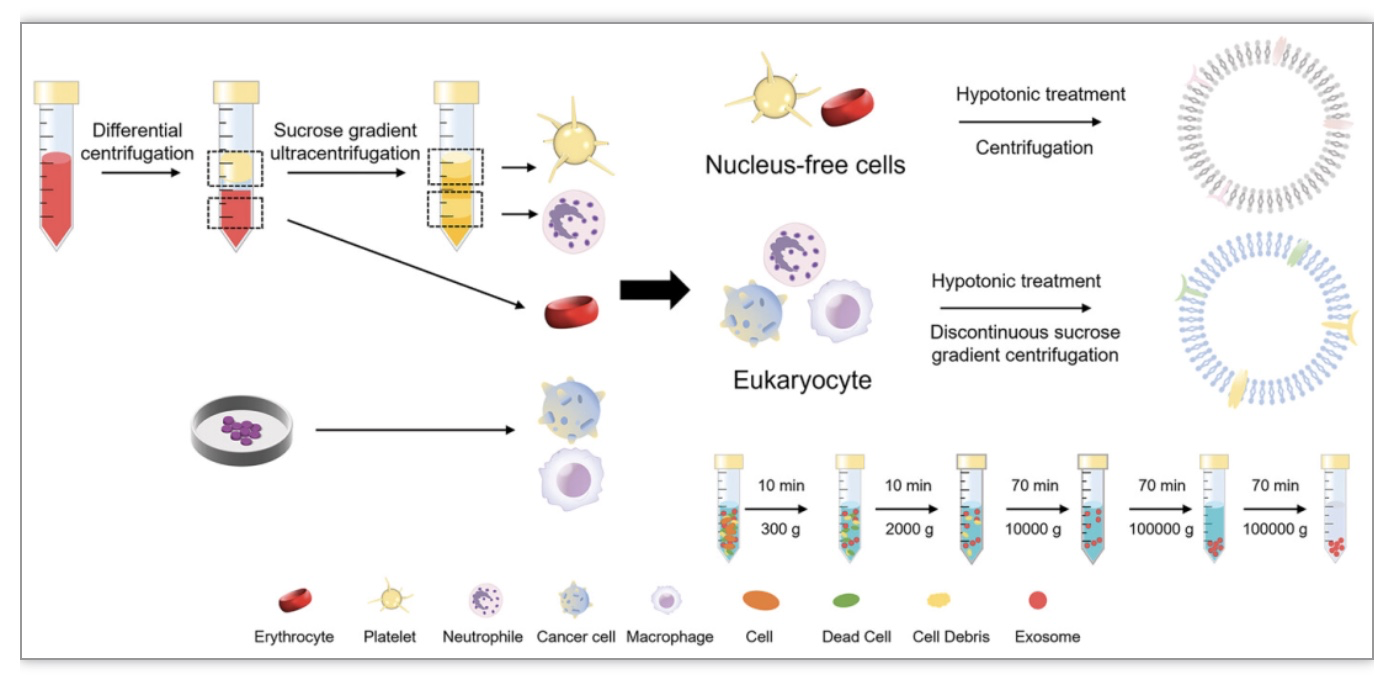
图3. 不同细胞膜的提取
不同细胞膜的提取方法不同。对于无核细胞,首先通过细胞培养或离心收获足够的细胞,通过反复细胞冻融或低渗裂解获得细胞膜,再通过离心去除可溶性蛋白,得到纯化的细胞膜碎片,最后通过聚碳酸酯多孔膜挤压,生成细胞膜衍生的纳米囊泡。与无核细胞相比真核细胞膜的提取更为复杂,需要通过不连续的蔗糖梯度离心去除细胞内的囊泡、生物大分子和细胞核。
不同来源的细胞膜有不同特点,比如红细胞膜可以增加血液循环时间和稳定性;血小板膜可以增加免疫逃逸、黏附抗原、靶向肿瘤;巨噬细胞膜可结合免疫调节分子CSF1、穿过血脑屏障;肿瘤细胞膜可特异性识别和靶向源肿瘤;脂质体膜可增强渗透和保留效应;细菌外膜囊泡可调节免疫和重编程肿瘤微环境;外泌体可靶向肿瘤、免疫逃逸。
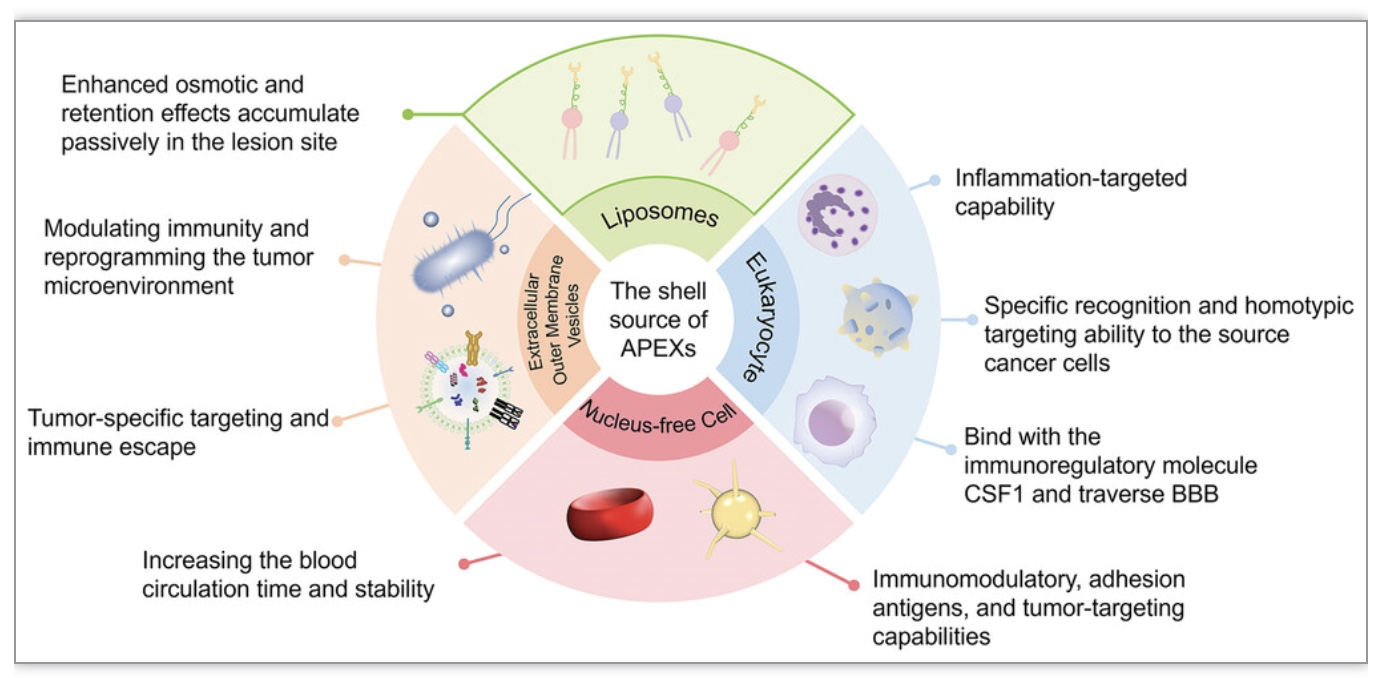
图4. 不同来源细胞膜的特点
三、APEXs的生物医学应用
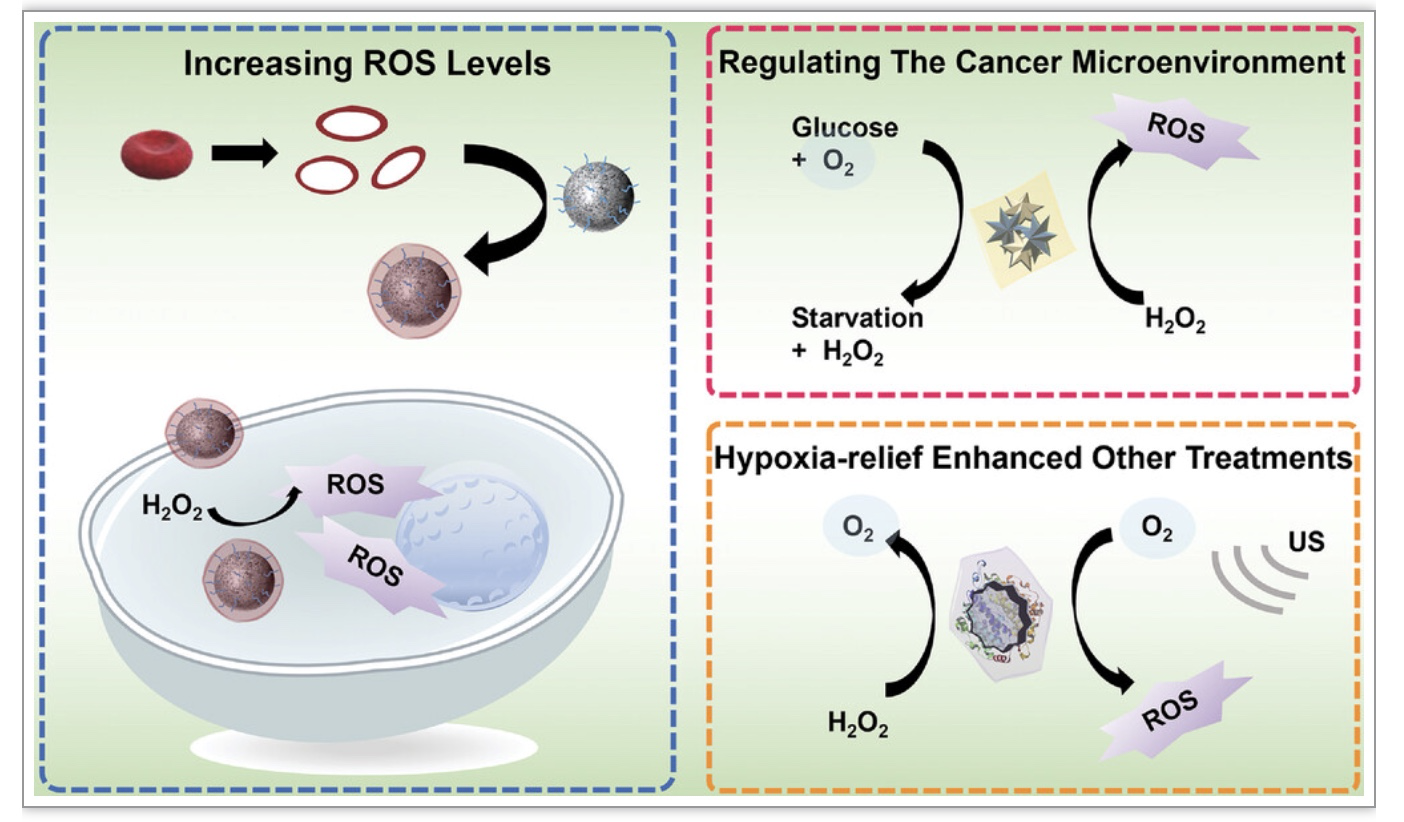
图5. APEXs通过三种方式实现抗肿瘤
APEXs可通过几种策略杀死癌细胞。一是通过增加活性氧水平来杀死癌细胞。二是调节肿瘤微环境(tumor microenvironment, TME),如消耗葡萄糖进行饥饿治疗。三是通过增加氧气水平来加强其他疗法。此外,用细胞膜伪装催化剂可以提高催化剂的循环时间和靶向能力。APEXs用于抗氧化和抗炎治疗,一方面依赖于APEXs中催化剂的抗氧化性能,另一方面依赖于APEXs外层的细胞膜,比如中性粒细胞膜可以延长催化剂的血液循环时间、靶向炎症病灶。APEXs的神经元保护作用主要归功于细胞膜能穿过血脑屏障的能力。
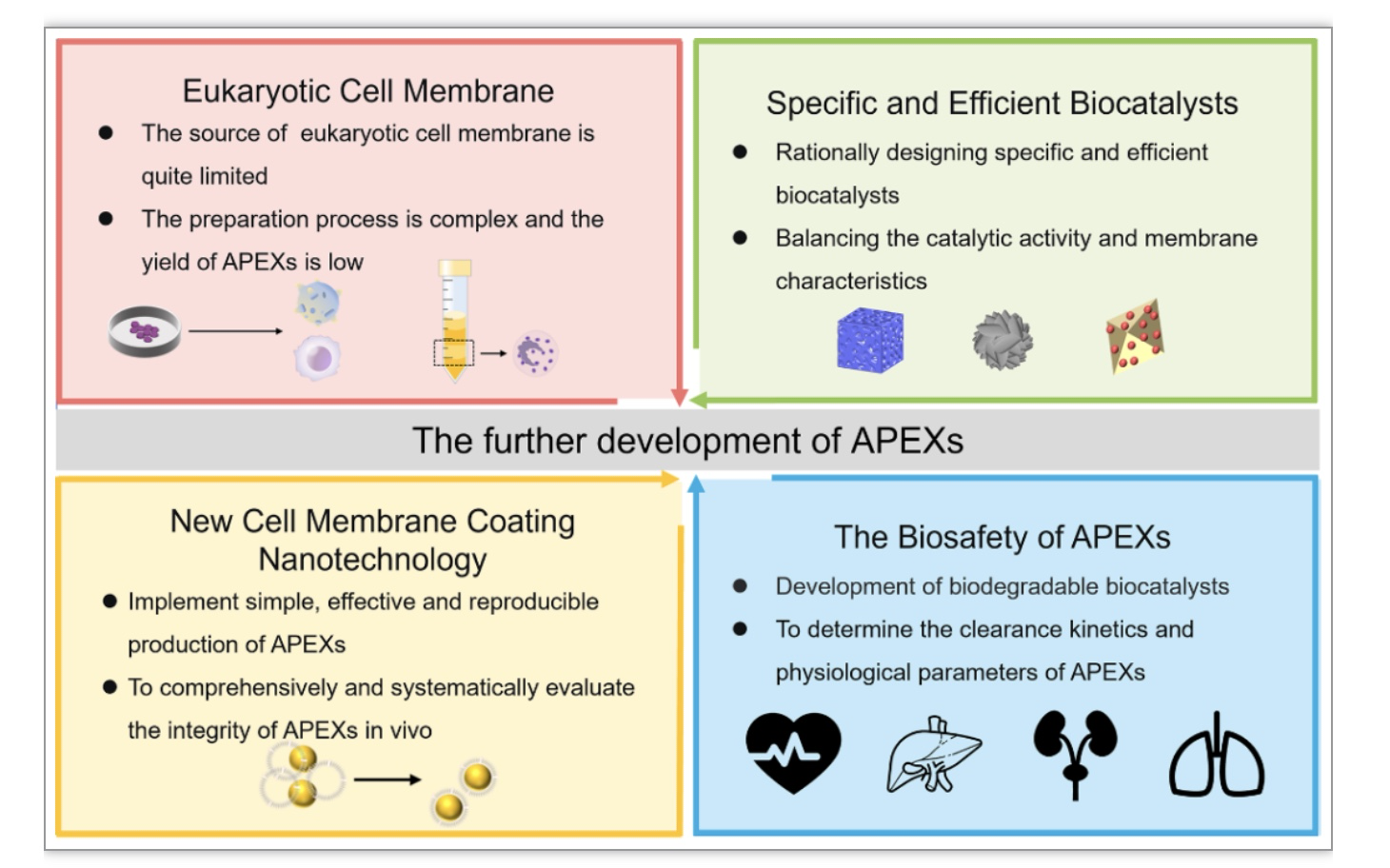
图6. APEXs的发展与未来
该文章指出,在后续APEXs的设计和应用中,以下几点值得注意:(1)寻找更稳定的真核细胞膜来源,探索更简单的真核细胞膜提取方法。真核细胞来源有限,膜提取过程较为复杂,这将限制APEXs的发展。虽然可以合成脂质体等人工膜,但天然膜上的蛋白质可以赋予APEXs更多的特性,如免疫逃逸和同源靶向能力。(2) 设计特异性、高效的催化剂,促进APEXs在生物医学上的应用。许多类型的研究表明,催化剂的结构,如尺寸、形态、组成和表面电荷等,是影响催化活性的关键因素。然而,考虑到催化剂表面的膜,可能需要抛弃催化剂的一些理化性质或结合天然酶,以更好地平衡催化活性和膜特性,以实现特定和高效的生物应用。(3) 探索新的细胞膜涂层纳米技术,用于生产简单、有效和可重复的APEXs。典型的膜涂覆工艺是挤压法,挤压法会导致APEXs的壳和核的损伤。此外,应最大限度地保留细胞膜和催化剂的完整性,以保持血液循环中的功能。(4)系统、综合的评价APEXs的生物安全性。APEXs进入人体后,会在体内的健康组织和器官中积累。尽管APEXs具有比裸催化剂更高的生物相容性,但生物安全性仍然是APEXs设计和应用阶段需要认真考虑的关键问题,例如开发可生物降解的催化剂,以减少APEXs在体内的长期积累。

