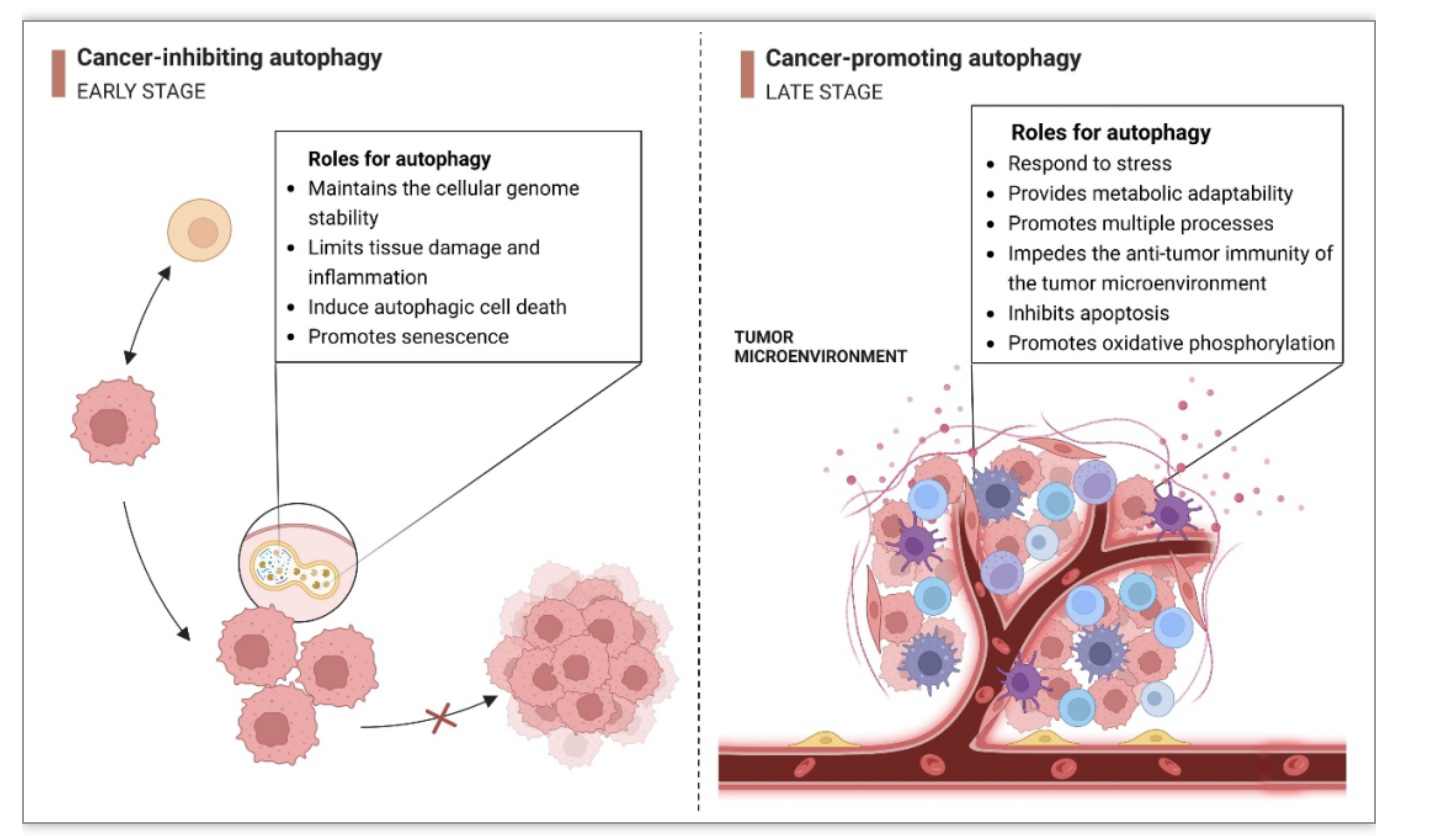
自噬(autophagy)是细胞在自噬相关基因(autophagy-related gene,ATG)的调控下利用溶酶体降解自身细胞质蛋白和受损细胞器的过程,其功能主要是作为一种生存适应机制,在病理和细胞应激状态下维持细胞内的平衡,包括内质网应激、营养物质的缺乏和缺氧等[1]。许多研究表明,自噬参与了癌变的各个阶段,包括肿瘤的发生、发展、代谢和转移,并且在许多癌症中发挥着双重作用[2, 3]。一方面,在肿瘤发生的早期阶段,自噬作为一种动态降解和质量控制机制,通过清除有缺陷的蛋白质和细胞器起到抑制癌变的作用[4, 5]。另一方面,一旦癌症发展到晚期,当肿瘤处于血管生成受限、营养缺乏和缺氧等压力下时,自噬就会成为一种支持肿瘤生存、生长、转移和侵袭的促生存机制[6, 7]。因此,根据肿瘤的不同阶段,通过靶向调控自噬途径进而促进或抑制自噬,将会是一种癌症预防和治疗的有效方法。在过去的五年里,长非编码RNAs(lncRNAs)在自噬中的生物学功能已被逐渐了解。许多研究表明,lncRNA通过调节ATG蛋白和自噬相关信号通路,可以激活或抑制自噬的发生,进而影响癌症发展。因此,自噬相关lncRNAs已被广泛研究其用于靶向治疗癌症的潜力[8-10]。
本文根据调控自噬不同阶段的lncRNAs来分类总结了其在癌症中的作用。此外,该综述还讨论了自噬相关的lncRNAs作为不同癌症的生物标志物和治疗新靶点的潜力和挑战,以期为癌症治疗中自噬调节策略提供一个新的方向。

自噬的调节在许多癌症的肿瘤抑制和促进中发挥双重作用。一方面,在疾病和应激条件下,自噬通过消除积累的受损蛋白质和细胞器,在维持细胞基因组稳定性方面发挥了重要作用。自噬缺陷已被证明会增加肿瘤前病变和肿瘤发病率,强调了自噬的肿瘤抑制功能。自噬可以通过维持基因组稳定性、限制组织损伤和炎症,以及在肿瘤发生的早期阶段诱导自噬性死亡来抑制肿瘤的发展。因此,将调控自噬和自噬相关性死亡作为癌症治疗方面新的研究方向具有重要意义。
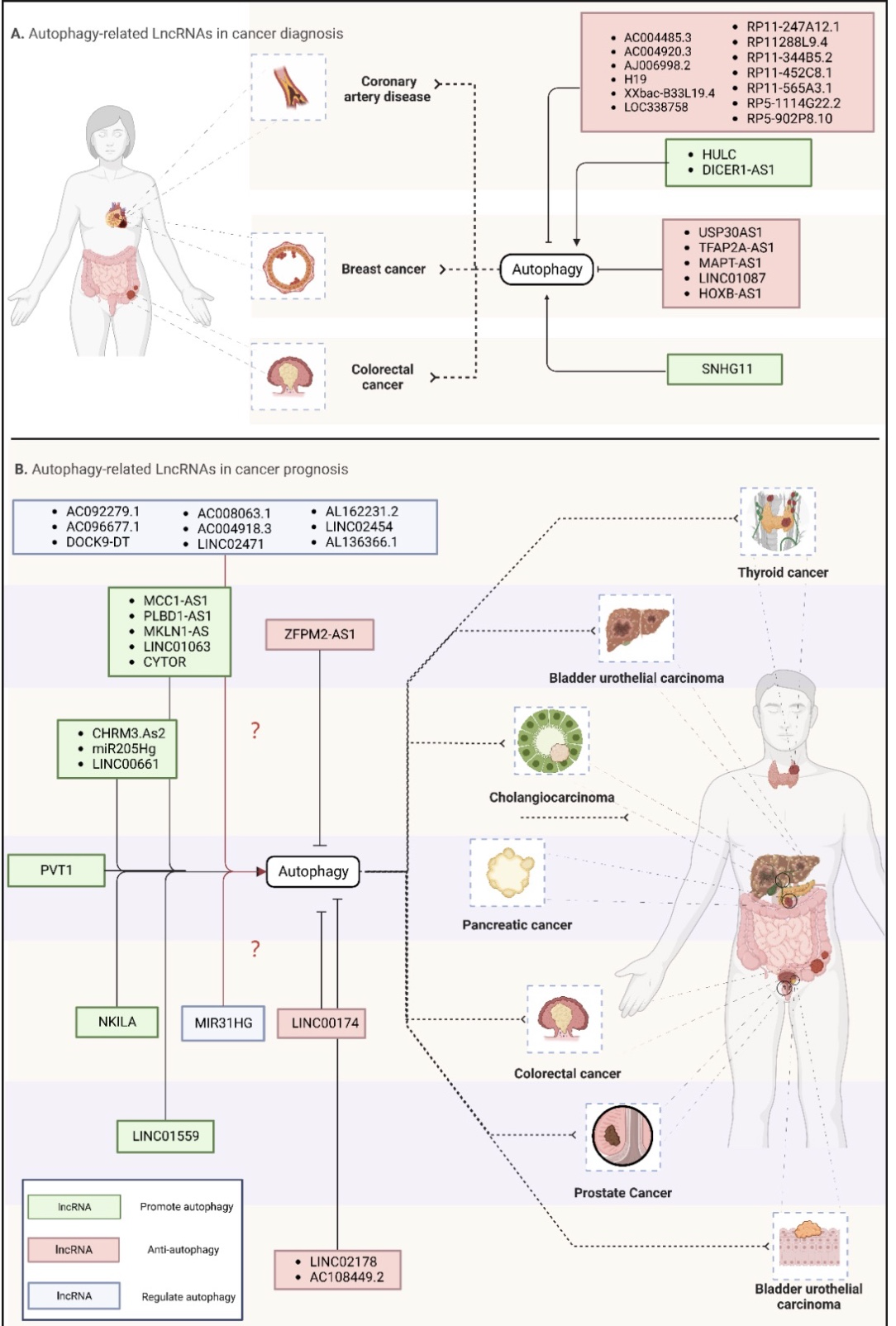
LncRNAs是一个长于200个核苷酸的RNA分子家族,具有开放阅读框的功能和编码蛋白质的潜力。随着高通量技术的兴起和传统方法的进一步发展,大量具有不同结构和功能的新型lncRNAs被发现。近年来,关于lncRNAs参与自噬和癌症的生物学相关研究激增。这些研究表明lncRNAs可以通过调节自噬不同阶段的ATG来影响肿瘤的发生、发展、转移、复发和预后。由于自噬在肿瘤中是一把双刃剑,所以调节自噬的lncRNAs在肿瘤发展中也具有双重功能。在功能上,大多数lncRNA通过ceRNA机制靶向自噬相关的miRNAs进而调节自噬过程,最终影响了肿瘤的发展。因此,根据肿瘤的不同阶段,通过靶向调控自噬的lncRNA进而促进或抑制自噬,将会是一种癌症预防和治疗的有效方法(图2)。

由于大多数癌症被诊断时已处于无法治愈的晚期,因此迫切需要开发可在早期阶段检测出癌症的可靠诊断生物标志物。lncRNAs因其在血液中能够以高度稳定的形式被检测到而获得了广泛关注。LncRNAs在血浆中的稳定性是通过广泛的二级结构、保护性外泌体的运输和稳定的翻译后修饰来维持的。因此,循环lncRNAs有可能作为可靠的癌症生物标志物发挥作用。然而,将lncRNA作为临床应用的诊断标志物之前,仍应满足几个条件。第一,作为一种诊断标记物,其异常表达应该出现在肿瘤的早期阶段。第二,现有的生物标志物形式在体内和实验条件下都应该保持相对稳定。第三,生物标志物应具有良好的诊断性能,如高准确性、敏感性以及特异性等。最后,作为某一恶性肿瘤的特异性生物标志物,其异常表达应该出现在大多数患有该肿瘤的患者体内,并且只出现在该特定恶性肿瘤患者体内。因此,符合上述条件的lncRNAs在未来极有可能成为癌症诊断的可靠生物标志物。
鉴于lncRNAs在癌症发展中的关键作用,靶向自噬相关lncRNAs可能会产生更有效的抗癌效果。例如,通过CRISPR/Cas9对靶标lncRNA进行基因重编辑,通过反义寡核苷酸(ASO)特异性阻断靶标自噬相关lncRNAs的转录或翻译来达到调控癌症中的自噬的目的以及通过应用RNA干扰(RNAi)技术沉默靶标自噬相关lncRNA等。然而,将自噬相关lncRNAs作为未来的癌症治疗靶点仍有许多问题有待解决。例如,免疫系统反应的激活、寻找合适的递送方式、有限的生物利用度和存在脱靶效应等(图4)。
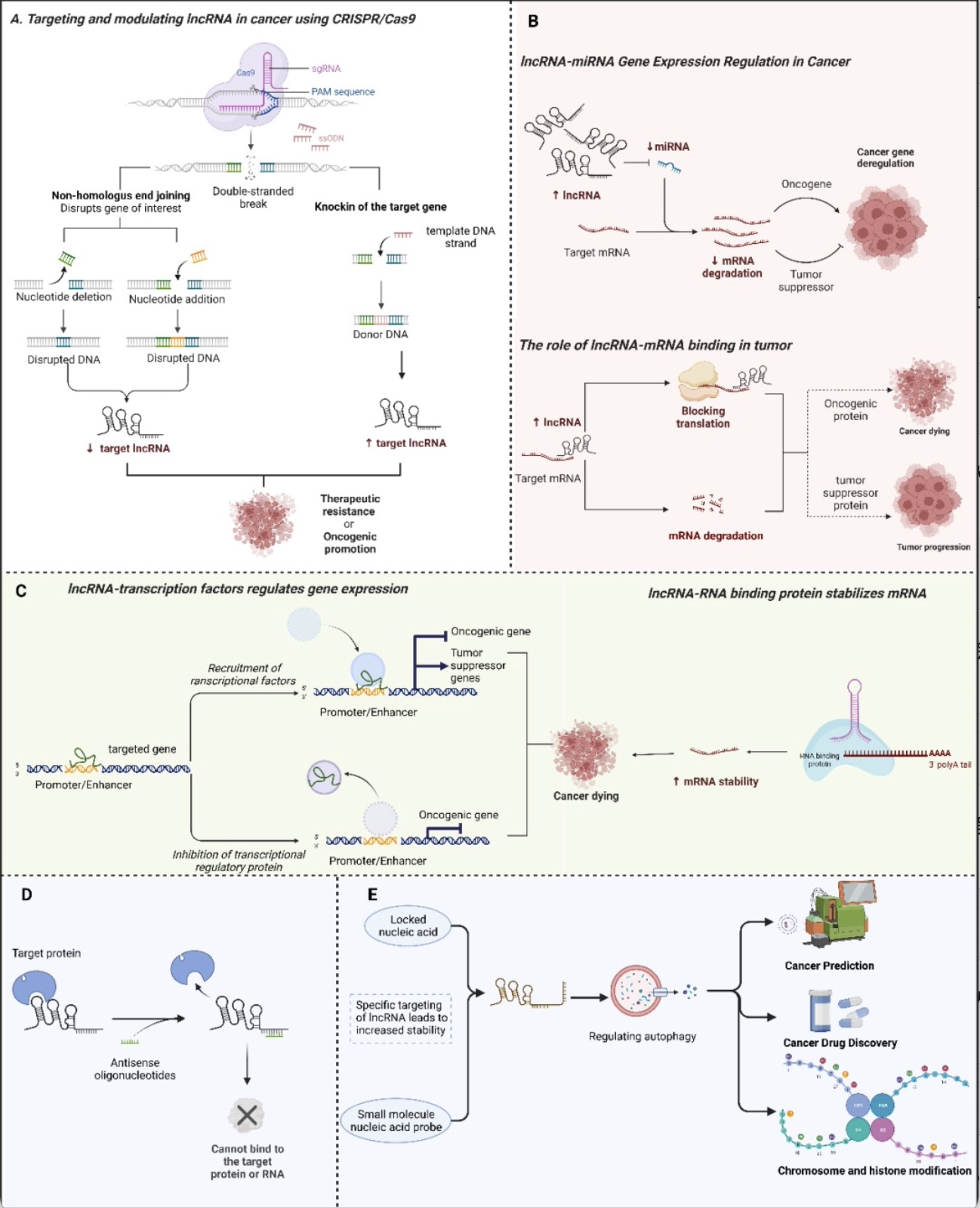
作者指出,具有自噬调控功能的lncRNAs在癌症中的复杂性可以归因于自噬在癌症发展过程中的动态作用。在功能上,大多数lncRNAs作为ceRNAs特异性地海绵化相应的自噬相关miRNAs来调节自噬。lncRNAs还具有更复杂的自噬调控机制,包括但不限于染色体和组蛋白修饰、转录调控和蛋白-蛋白相互作用,这些机制还有待进一步阐释。由于lncRNAs和自噬之间的密切关系,发现基于lncRNA的方法来监测或抑制自噬通量进行靶向治疗将是可行的。

