编码Wnt信号通路核心成分的基因,尤其是APC和β-catenin,是人类癌症中最常见的突变基因之一。约80%的结直肠癌的发生发展是由于APC肿瘤抑制因子的功能缺失引起的Wnt信号通路过度激活导致的。虽然大量的研究表明Wnt/β-catenin信号通路的异常激活在癌症的发展和癌症治疗耐药过程中起关键作用,但是仍然没有已批准的Wnt信号通路抑制剂用于治疗这些癌症。Wnt enhanceosome是Wnt信号转导的终端大分子机器,普遍认为是治疗APC或β-catenin突变驱动的癌症最有希望的靶点。然而,关于Wnt enhanceosome是如何装配的分子机制仍然知之甚少。

BCL9和Pygo是经典Wnt信号通路中依赖β-catenin的转录激活复合物(也被成为Wnt enhanceosome)所需的重要转录共激活因子。β-catenin结合BCL9的同源结构域2(HD2),BCL9-HD1则结合Pygo,该团队前期阐释了β-catenin与 BCL9相互作用[1]和BCL9与Pygo相互作用[2]的分子机制。然而Pygo是如何与整个Wnt enhanceosome相互作用的分子机制仍不清楚。Pygo的N端同源结构域(NHD)通过与LDB-SSBP复合物相互作用在Wnt/β-catenin靶基因的转录激活中起重要作用。LDB/SSBP复合物调节基因转录,介导长距离的增强子和启动子互作,调控细胞命运。但是 Pygo 和 LDB1-SSBP相互作用的结构基础仍然未知。
为揭示Wnt enhanceosome如何装配,研究人员运用哺乳细胞蛋白表达系统分别共表达了BCL9-Pygo和LDB1-SSBP复合物,并运用分子筛共迁移技术和生物膜层干涉技术(BLI)发现BCL9-Pygo和LDB1-SSBP复合物相互作用,且亲和力高达32 nM(图1)。此外,研究人员进一步证明BCL9-Pygo-LDB1-SSBP四元复合物的形成主要依赖于BCL9-HD1与Pygo的直接相互作用。
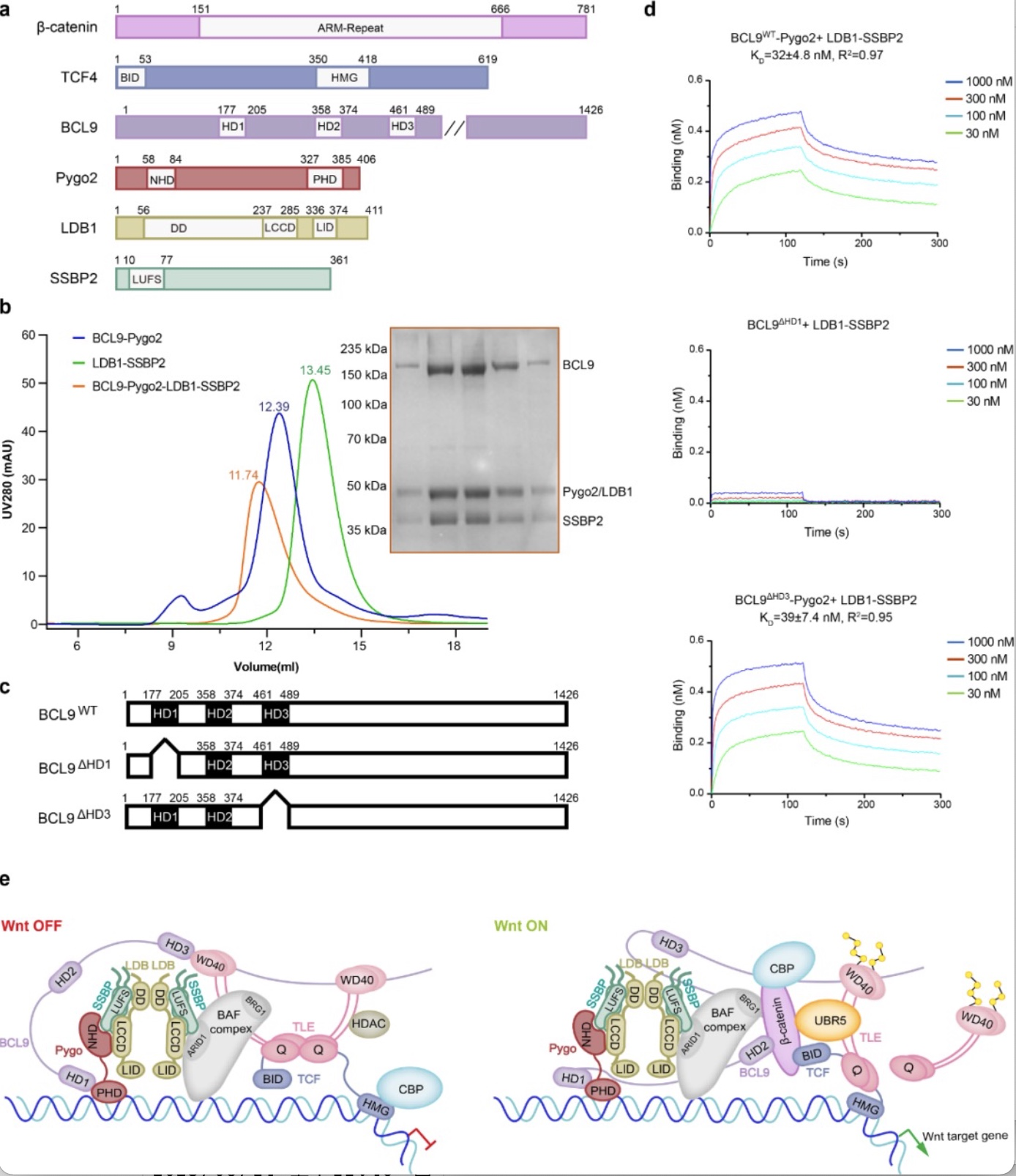
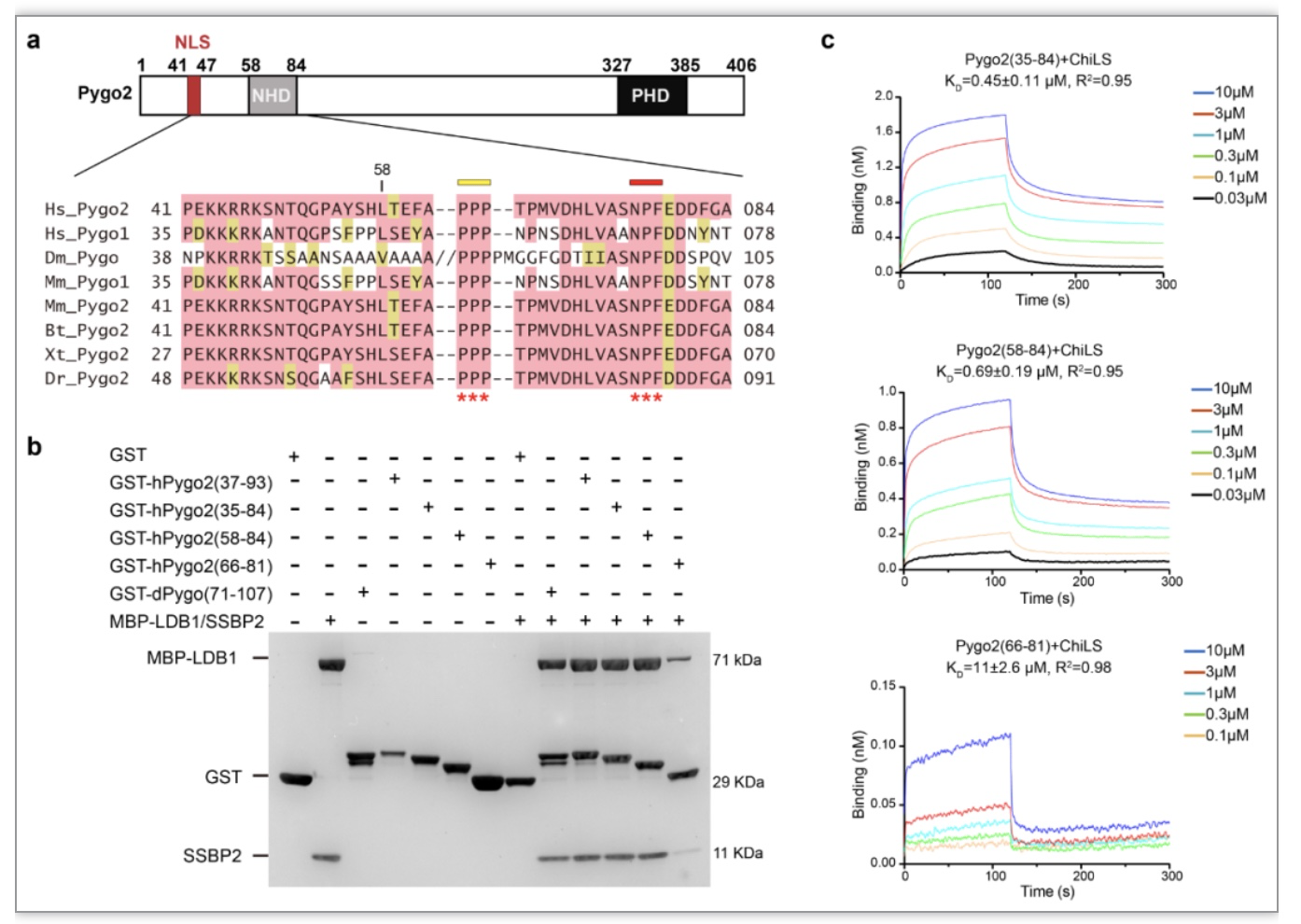
图2 Pygo与LDB1-SSBP相互作用
在此基础上,研究人员解析了人源Pygo-LDB1-SSBP三元复合物2.45 Å分辨率的晶体结构,阐明了Pygo与LDB1-SSBP相互作用的结构基础,研究发现一个LDB1-SSBP复合物可以同时结合两个Pygo分子,且Pygo-NHD内的NPF motif对Pygo和LDB-SSBP的相互作用至关重要,它深深的插入了LDB1-SSBP形成的相互作用面口袋内。这一NPF结合口袋为未来癌症药物的设计开发提供了重要的潜在药物靶点(图3)。此外,研究人员还运用CRISPR/Cas9基因编辑技术构建了双敲除LDB或Pygo的HEK293T细胞系,结合TOPflash实验和RNA-Seq技术进一步证明了Pygo-LDB1-SSBP相互作用关键氨基酸对于依赖于Wnt/β-catenin的基因转录的功能相关性。
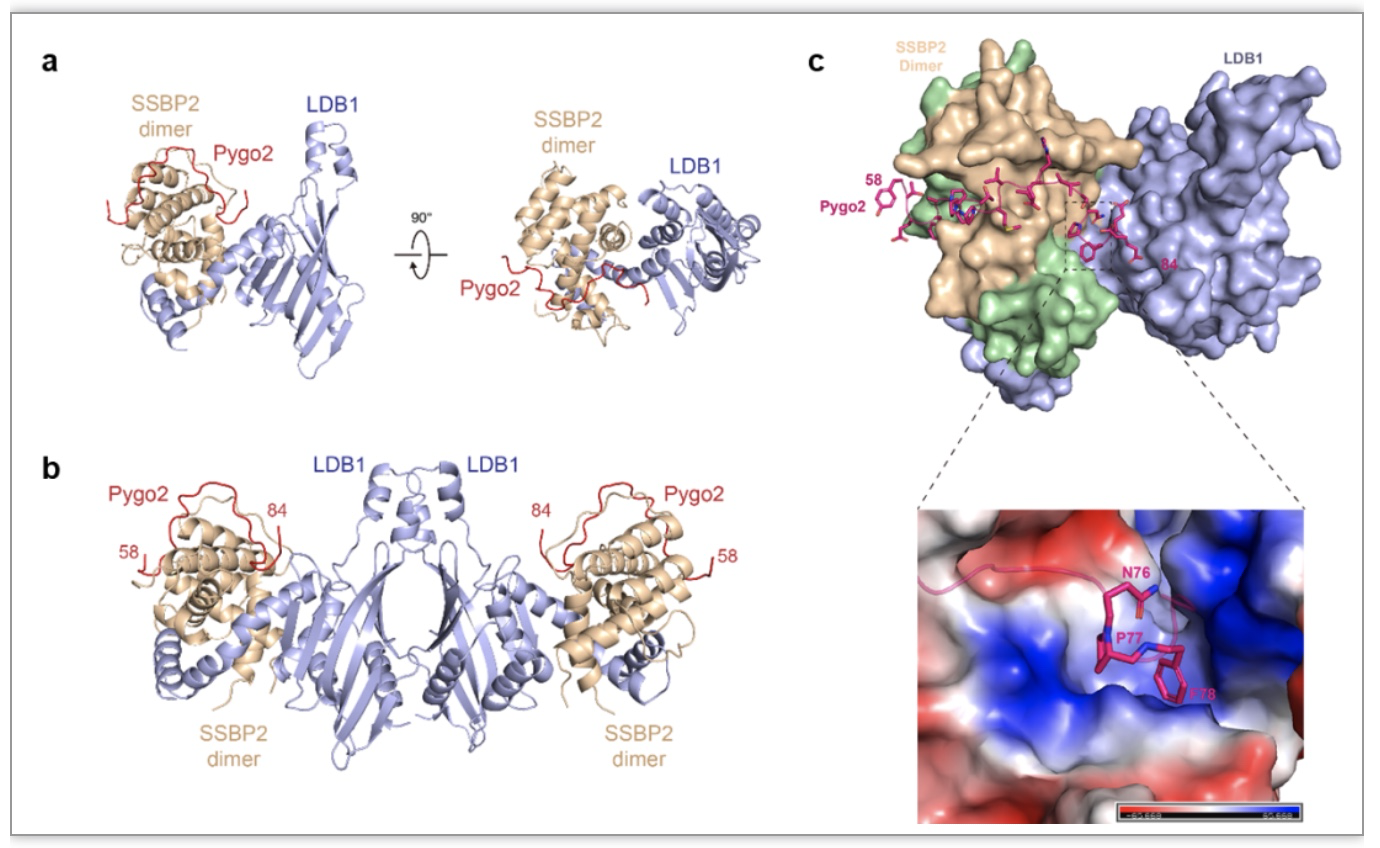
图3 Pygo-LDB1-SSBP三元复合物的晶体结构和相互作用面

