何为内毒素(Endotoxin):细菌内毒素,又称为“热原”,为区别于外毒素而称之为内毒素。内毒素在自然界中分布较广,主要存在于革兰氏阴性菌中,也存在于极少数革兰氏阳性菌、真菌、支原体及某些动植物组织中[1]。内毒素是革兰氏阴性菌细胞壁外层上的特有结构,细菌在存活状态时无法释放出来,只有当细菌死亡自溶时才能被释放到细胞外。细菌内毒素是由脂多糖(LPS)、蛋白质和磷脂组成的高分子量复合物(图1),可表现出多种毒性作用,发挥毒性的成分主要为类脂质A(Lipid A),而类脂质A是LPS活性不可或缺的部分,故将其视作LPS 的“生物活性中心”[2]。
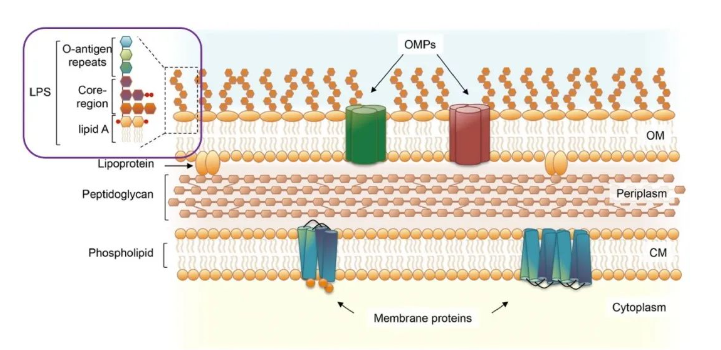
图1:内毒素结构
内毒素的危害:内毒素不仅会影响我们的生物医学实验结果,而且对动物和人类有危害作用。如在转染实验中,内毒素会与 DNA 竞争转染试剂,影响转染试验中目的 DNA 的摄取,显著降低了内毒素敏感细胞株的转染效率[3];内毒素还会诱导巨噬细胞和B细胞等免疫细胞发生非特异性免疫反应,从而导致转染结果的误读。有研究表明,细菌内毒素可降低基因免疫小鼠存活率和产仔率[4]。此外,内毒素可引起动物和人发烧、内毒素性休克综合征和补体级联的活化,这些反应包括免疫介质如IL-1和前列腺素的诱导合成等。因此,用于下游基因治疗、疫苗生产的质粒载体的内毒素含量就显得尤为重要。
内毒素的检测:
-
法规(药典):
细菌内毒素检查包括两种方法,即凝胶法和光度测定法,后者包括浊度法和显色基质法。
供试品检测时,可使用其中任何一种方法进行试验。
当测定结果有争议时,除另有规定外,以凝胶限度试验结果为准[5]。
(药典三部(2015 版)-通则-1143 细菌内毒素检查法)。
-
检测原理:
鲎试剂法是一种检测细菌内毒素灵敏度很高且专一性很强的方法。
其作用原理如下:
内毒素在钙、镁等二价阳离子的参与下,先后激活鲎试剂凝固酶系统的C因子、B因子、前凝固酶,最后将凝固蛋白原变成凝固蛋白[6](图2)。
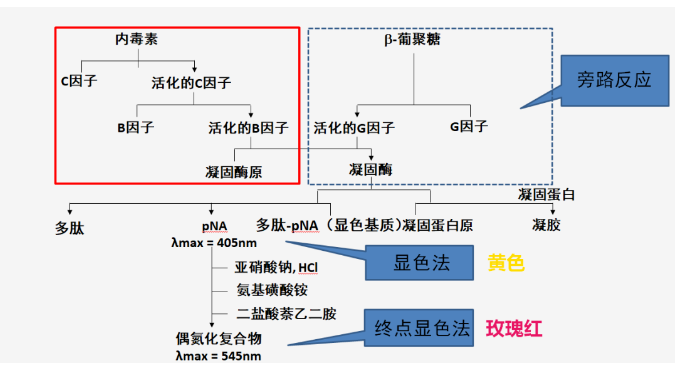
图2 内毒素检测原理
依据原理图,可以选择不同反应通路来确定不同的检测方法。
1.凝胶:对应定性的凝胶法和定量的动态浊度法;
2.黄色:对应动态显色法和微板重点显色基质法;
3.玫瑰红:试管终点显色法,操作繁琐,适用于样本量少,且成本高。
鲎试剂的现状和展望:
1968年,由Levin和Bang发现并建立了鲎试验法检查细菌内毒素,因其简便、快速、灵敏、重现性好等优点,成为药品检验中热原检查家兔法的替代方法[7]。目前有凝胶法(Cel.clot techique)、比浊法(turbidmetric assay)、比色法 (colorimetric assay)和免疫学方法等。鲎试剂具有无与伦比的天然优势:方便好用、快速灵敏、特异性强,很快就受到了欧美制药公司的追捧,目前已发展为一项热门产业。
目前,鲎试剂几乎是检测内毒素唯一使用的试剂,更是中国药典规定使用的试剂。由于鲎血液的稀有性和不可替代性,正在给“活化石”鲎带来危机。鲎资源仅分布于中国及东南亚一带和美国西海岸,我国鲎资源近年逐渐衰减 [8] ,以厦门为例,20 世纪90年代与20世纪50年代相比,鲎资源减少了80%~90%,现在主要栖息于人工建立的保护区[9]。
为了解决上述问题,重组C因子法是细菌内毒素检查法的补充替代方法,原理是将鲎试剂中的 C 因子采用生物技术重组获得,用来替代海洋生物鲎作为鲎试剂原料唯一来源[10 ]。鲎C因子是鲎血细胞中一种对内毒素敏感的丝氨酸蛋白酶原,能以高亲和力结合LPS的脂质A,从而激活启动整个鲎血细胞的血凝级联系统。因此,重组的鲎 C因子可代替鲎试剂用于内毒素检测,并采用显色法定量检测革兰氏阴性菌内毒素(图3)。此方法不再使用天然鲎血细胞,保护了鲎资源。目前鲎试剂检测法(LAL/TAL)正在缓慢地向重组因子C(rFc)法转换,来不断满足行业发展的需求。
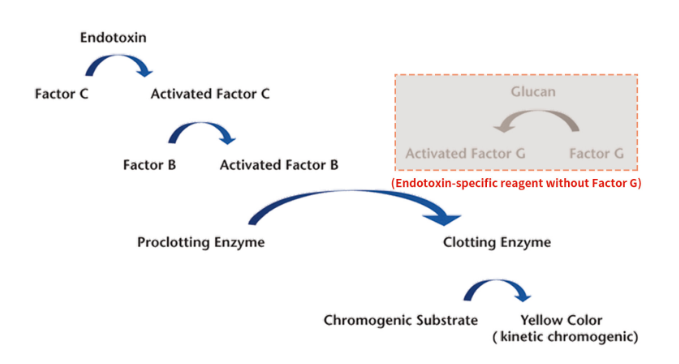
图3 基因重组级联试剂显色法原理
安升达采用的定量动态浊度检测法对质粒样品进行检测,定量TAL检测≤0.01EU/ml,可以完全覆盖各个等级质粒内毒素浓度要求。
-
科研级质粒DNA建议应用于分子克隆、测序、定点突变、Southern blot、文库构建、探针合成、转化等科研基础实验。
-
转染级(≤100EU/mg)质粒DNA建议应用于多种类型细胞的转染实验、病毒传导、CAR-T等细胞治疗相关病毒载体的生产制备、基因疫苗和基因治疗研究、抗体或蛋白生产、动物学研究等。
-
准医疗级别(≤10EU/mg)质粒DNA可用于CAR-T治疗、基因治疗、基因疫苗、临床研究等。
-
高标准大规格定制化最高可提供g级,内毒素≤5EU/mg的质粒。

