细胞自噬(autophagy)是一种“自食”的胞内机制,是细胞在自噬相关基因的调控下利用溶酶体降解自身受损的细胞器和大分子物质,以实现细胞本身的代谢需要和某些细胞器更新的过程。自噬性细胞死亡又称之为Ⅱ型程序性细胞死亡,细胞凋亡被称为1型程序性细胞死亡。它们的主要区别:细胞凋亡依靠的是胱冬肽酶等多种水解酶,而自噬纯粹是在溶酶体的作用下发生的,而不依赖于某些酶。
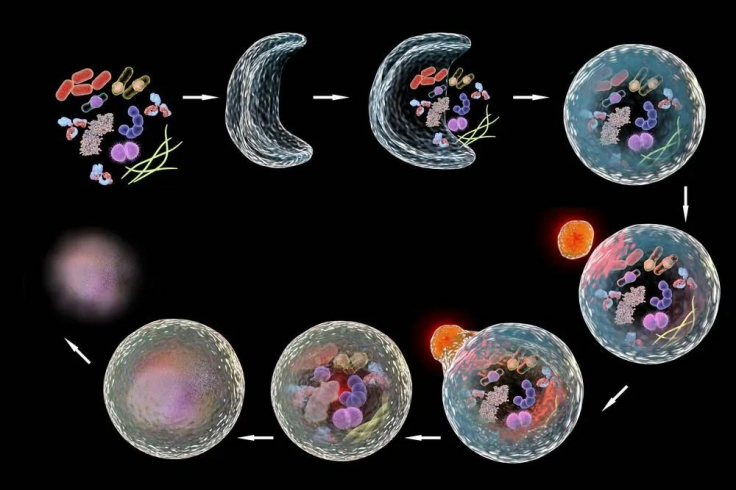
机体的生理和病理过程中都存在自噬现象,在生理条件下,细胞的基础自噬活性能清除细胞内老化、受损的生物大分子和细胞器等,以维持正常的细胞生物学功能;在饥饿、缺氧等代谢应激状态下,细胞通过自噬降解老化、受损的生物大分子和细胞器等,能获得能量来源和重建所需物质,以维持细胞的基本生命活动。因此,自噬作为细胞重要机制,不仅帮助维持生物体稳态,与个体成长、发育、分化、衰老密切相关,其功能的紊乱还参与肿瘤、自身免疫疾病、神经系统疾病、心脑血管病、代谢糖尿病等多种疾病的发生和发展。
说起自噬研究领域,那真是一个耀眼的明星,最近一个世纪里已经有两位科学家因此获得诺贝尔生理医学奖。1963年比利时科学家Christian de Duve首次在溶酶体国际会议上提出了“自噬”的概念,并于1974年Duve因发现溶酶体获得了诺贝尔生理或医学奖。但之后的几十年里,自噬一直还是个小众研究领域,直到2016 年日本细胞生物学家大隅良典因其在阐明细胞自噬的分子机制和生理功能上的开拓性研究荣获诺贝尔生理或医学奖。至此,自噬领域研究逐渐成为了科研界一颗耀眼的明星。
根据物质的性质和将物质运送至溶酶体的方法,可分为不同形式的自噬。目前,哺乳动物细胞自噬主要可分为巨自噬(macroautophagy)、微自噬(microautophagy)和分子伴侣介导的自噬(chaperone-mediated autophagy,CMA)。
2022年9月12日,湖南大学生命医学交叉研究院王立明教授(第一作者)、美国密歇根大学Daniel J. Klionsky教授和澳门大学的沈汉明教授联合在Nature Reviews Molecular Cell Biology杂志上发表题为:The emerging mechanisms and functions of microautophagy的综述文章。点击这里,查看原文

(DOI:10.1038/s41580-022-00529-z,IF: 113.915)
该综述全面深入地概括了近年来有关微自噬的研究进展,重点介绍了多种形式的选择性微自噬(selective microautophagy),还详细讨论了微自噬的分子调控机制,微自噬与巨自噬的区别与联系,以及微自噬与人类重大疾病(例如癌症和神经退行性疾病)发生和进展的关系。

巨自噬。巨自噬的典型特征是形成一个独特的双膜细胞器,即自噬小体。在巨自噬过程中,自噬物质被一种名为“吞噬体”的隔离膜所包围。然后,吞噬体通过招募来自不同来源的膜来进行扩张,并弯曲成球形,形成具有双膜的自噬小体。最后,自噬体与晚期核内体(形成双体)及溶酶体融合,完成自噬溶酶体的形成,在自噬溶酶体中隔离的物质被消化和降解(图1a)。
巨自噬可以以环境依赖的方式靶向特定的物质。线粒体自噬、内质网(ER)自噬、溶酶体自噬、蛋白质聚集自噬、核糖体自噬和异种自噬(微生物)等等都属于巨自噬形式。
伴侣蛋白介导的自噬。在伴侣介导的自噬过程中,具有KFERQ样基序的胞质蛋白被伴侣蛋白HSPA8识别,并通过溶酶体相关膜蛋白2A(LAMP2A)和溶酶体HSPA8传递到溶酶体进行降解(图1b)。
微自噬。微自噬是真核细胞直接降解各种自噬物质的过程。在微自噬过程中,自噬物质通过膜突出和内陷直接被溶酶体和晚期核内体吸收,自噬物质在内溶酶体腔内降解(图1c)。大多数对微自噬的研究都集中在与溶酶体、液泡或核内体相关的变化上。因此,根据溶酶体的形态学变化,科学家提出了三种不同类型的微自噬:1型,溶酶体或空泡突出;2型,溶酶体或空泡内陷;3型,内吞体内陷。每种类型的潜在机制和生物学功能仍不明确。
巨自噬,是科学家研究最早,最透彻的,所以我们通常所说的自噬一般就是巨自噬。
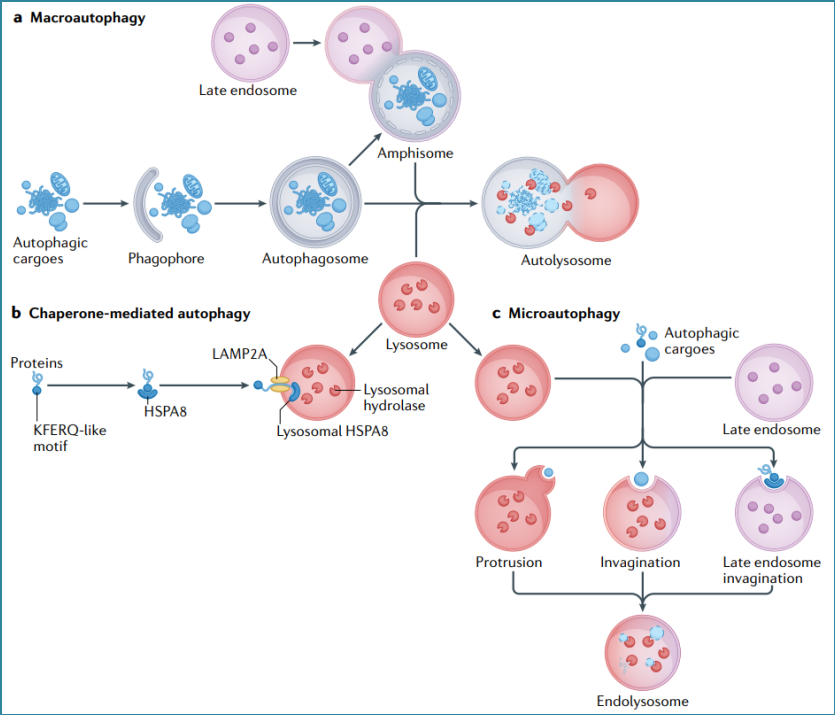
图1 巨自噬,分子伴侣介导自噬(CMA)和微自噬

