LINE-1是现今发现的人类基因组中唯一具有自主转座能力的转座子,它能够编码自身转座所必需的蛋白和酶。LINE-1广泛分布在基因组中,在人基因组中有近 500, 000个拷贝,约占人体基因组的17%(Goodier and Kazazian, 2008)。活跃的LINE-1转座在生物进化和物种形成等方面曾发挥过巨大的作用,但对个体来说,LINE-1的插入-复制引发的基因突变会导致基因疾病以及肿瘤的发生。近来研究表明,LINE-1还与机体衰老有密切的联系,其活化产生的cDNA会诱发Ⅰ型干扰素反应,而这是细胞衰老的标志,因此LINE-1的逆转录酶可能是治疗衰老相关疾病的潜在靶点(De Cecco et al., 2019)。
为了维持基因组的稳定性,宿主进化出多种方式对LINE-1的转座的各个环节进行调控,包括转录前、转录和转录后等过程。现已发现多种宿主因子具有抑制LINE-1的活性,例如SAMHD1蛋白、APOBEC3家族和MOV10等(Hu et al., 2015, Li et al., 2013, Khatua et al., 2010)。MOV10是先前发现的一种广谱抗逆转录病毒因子,具有强烈的抗LINE-1活性,前期研究表明MOV10是通过诱导LINE-1 mRNA的降解发挥其活性的,但具体机制尚不清楚。

本论文中,研究者首先通过免疫沉淀质谱对与MOV10相互结合的蛋白进行鉴定,发现多种参与RNA降解的蛋白因子,其中DCP2排名靠前,并且是RNA降解途径中的关键脱帽酶。
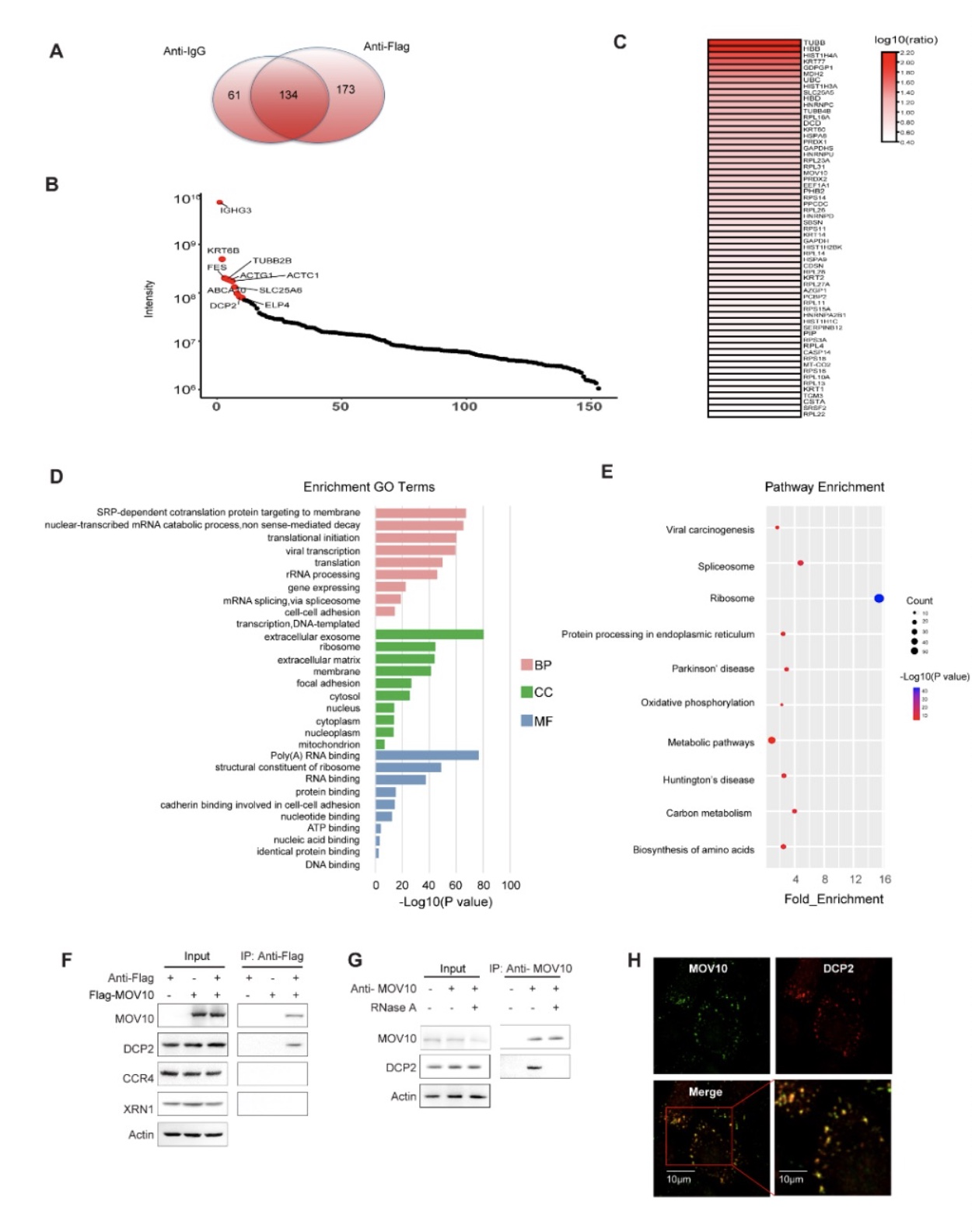
图1.MOV10与DCP2具有相互作用
DCP2酶在RNA降解过程中发挥的作用是水解mRNA 5’端的7-甲基鸟苷帽子,且该过程是不可逆的(Garneau et al., 2007),因此研究者推测DCP2是通过水解LINE-1 RNA的帽子介导LINE-1 RNA的降解。为了验证这一推测,研究者用m7G-cap特异抗体进行免疫沉淀,RT-PCR结果表明MOV10与DCP2协同介导LINE-1 RNA的脱帽,敲减MOV10后,DCP2对LINE-1 RNA的脱帽作用减弱,表明DCP2对LINE-1 RNA的脱帽作用依赖于MOV10。
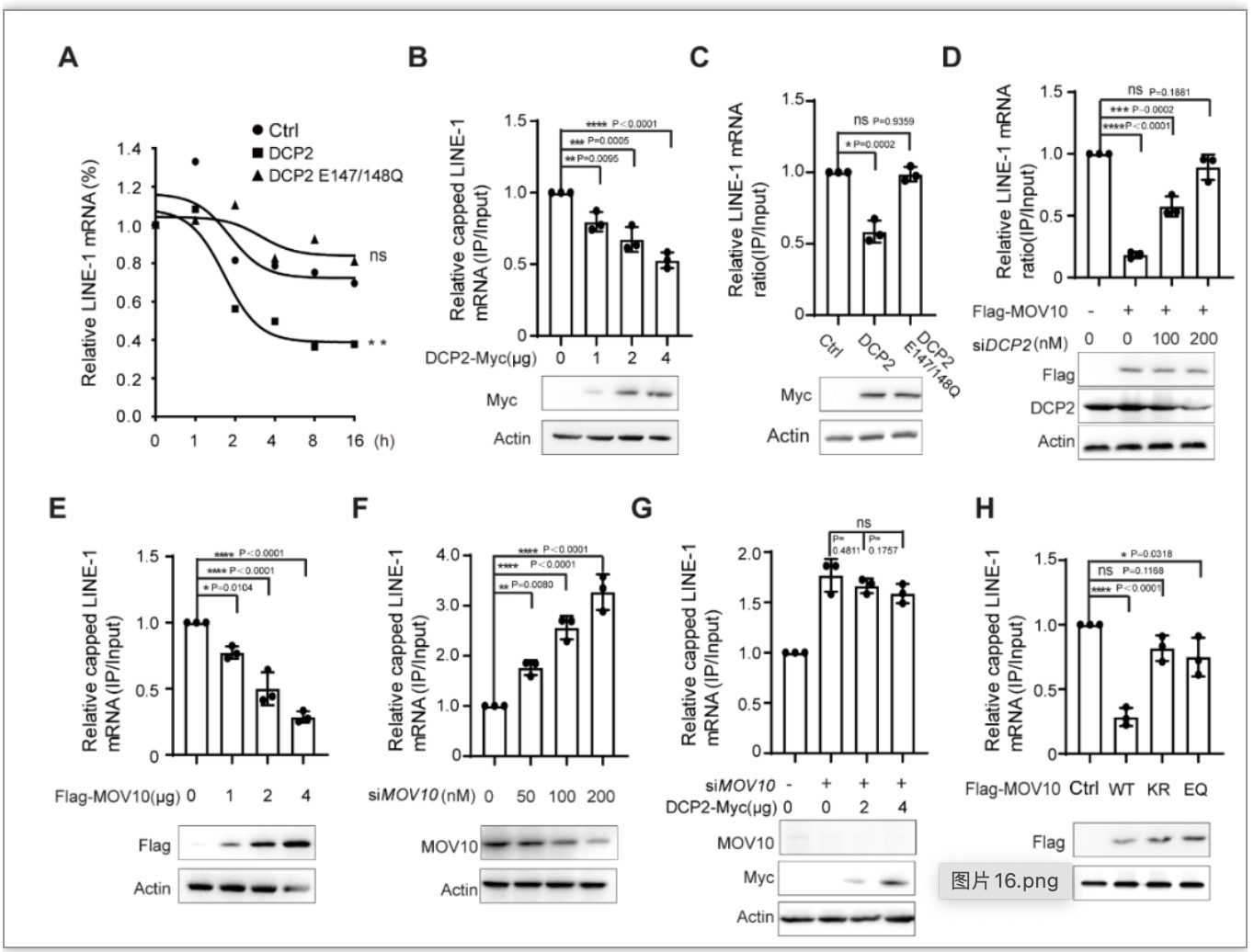
图2. DCP2对LINE-1 RNA的作用依赖于MOV10
先前的研究表明MOV10和LINE-1 RNP会相互结合(Li et al., 2013),本研究发现MOV10与DCP2具有相互作用,因此研究者推测MOV10可以介导LINE-1 RNP及DCP2形成DCP2/MOV10/LINE-1 RNP复合物(DMLC复合物)。激光共聚焦和免疫共沉淀结果表明MOV10过表达时,LINE-1 RNP与DCP2之间的相互作用增强,三者在胞质中发生进一步的聚集,形成更大的聚集颗粒。
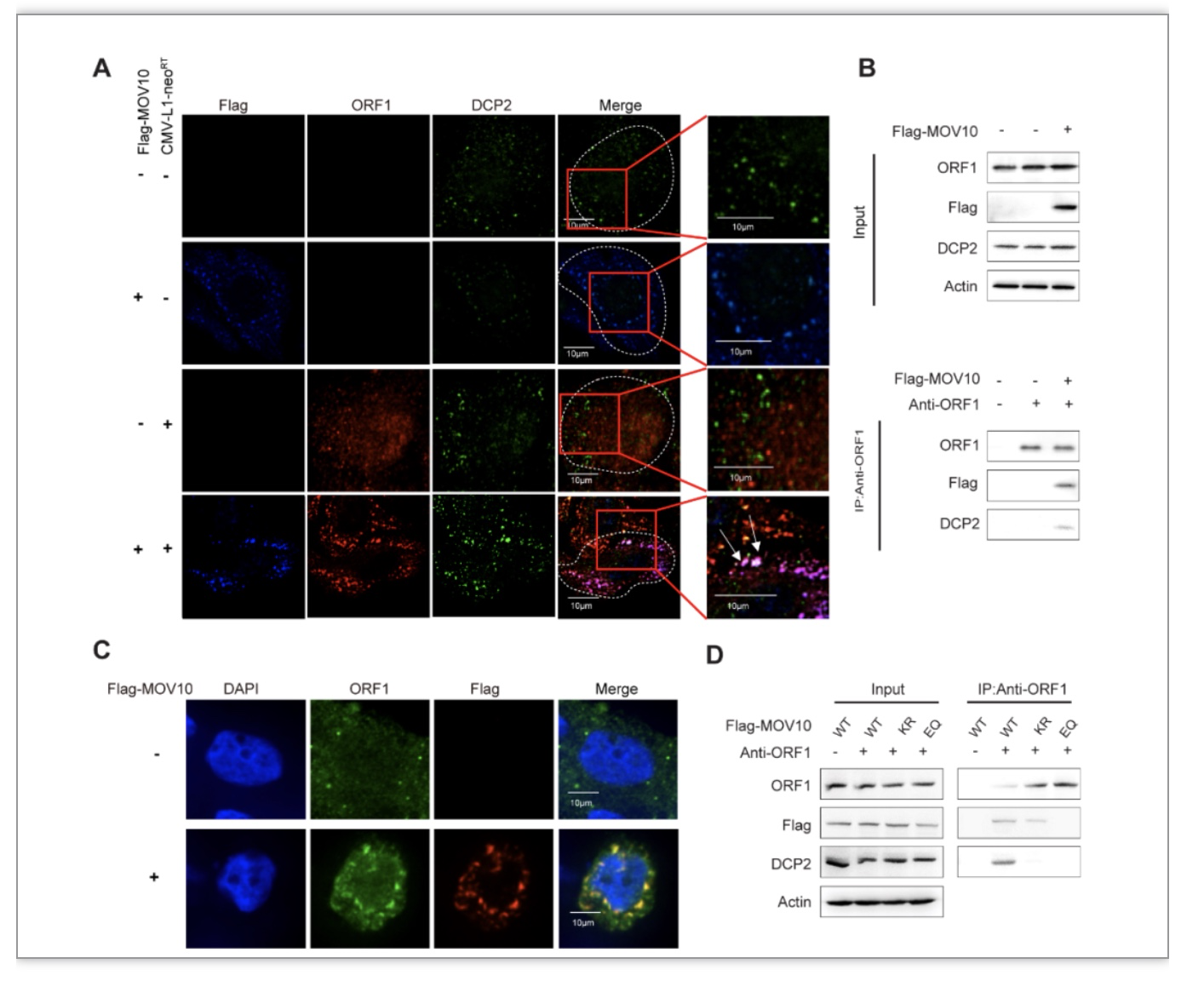
图3.MOV10促进MOV10 / LINE-1 RNP / DCP2复合物的形成
最新的研究表明,ORF1蛋白可以形成相分离(Newton et al., 2021),因此研究者推测,MOV10介导形成的大颗粒是否具有相分离特性。进一步研究发现,MOV10是通过相分离作用介导DMLC复合物所在的大颗粒结构的形成,在体外系统中加入MOV10蛋白后,ORF1相分离现象增强, MOV10会促进ORF1相分离的形成。
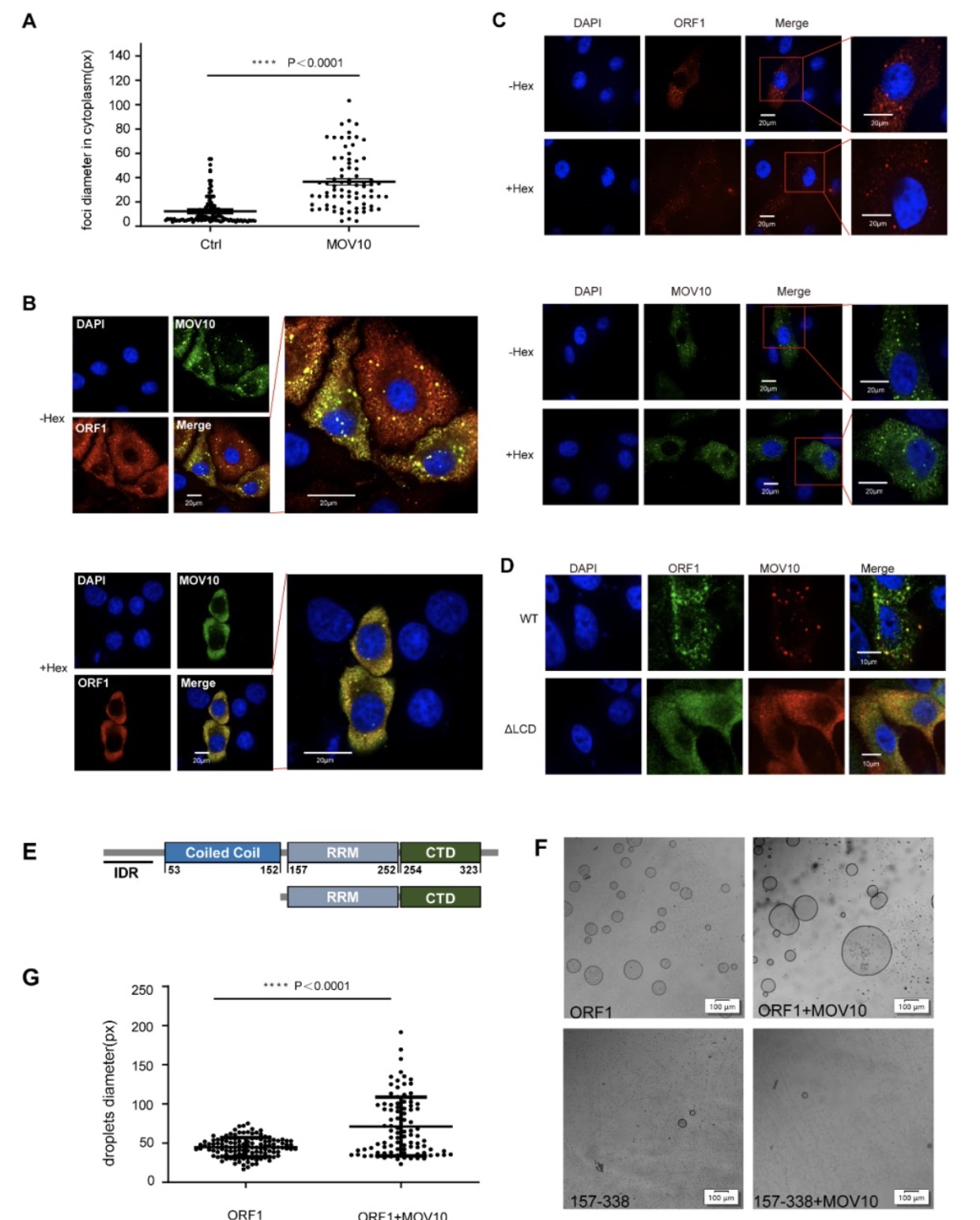
图4.MOV10通过相分离介导DMCL复合物所在的大颗粒结构的形成

图5.MOV10与DCP2协同介导LINE-1 RNA脱帽机制图

