多发性骨髓瘤(MM)是一种以骨髓浆细胞克隆性扩增和免疫球蛋白异常积累为特征的b细胞肿瘤,以溶解性骨病为标志。在CAR细胞治疗MM的潜在靶点中,b细胞成熟抗原(b cell maturity antigen, BCMA)因其在b细胞系细胞中的限制性表达模式和在恶性浆细胞中的普遍表达而成为一个理想的靶点。本研究通过试验发现CXCR4和抗BCMA CAR在NK细胞上的共同表达可能是控制MM进展的有效途径。
01
CXCR4R334X转染提高NK细胞的迁移和骨髓归属能力
作者开发了一种NK细胞扩增方案,并评估该扩增方法对CXCR4表达的影响。试验结果表明,与新鲜分离的NK细胞相比,体外扩增的NK细胞上CXCR4表达降低(图1A)。接着作者用编码野生型CXCR4 (CXCR4WT)或CXCR4R334X的mRNA电穿孔NK细胞,发现CXCR4R334X mRNA和CXCR4WT mRNA的电穿孔不影响NK细胞的溶细胞功能,并且CXCR4修饰的两种NK细胞能够像模拟电穿孔NK细胞一样有效地裂解K562细胞(图1B-D)。
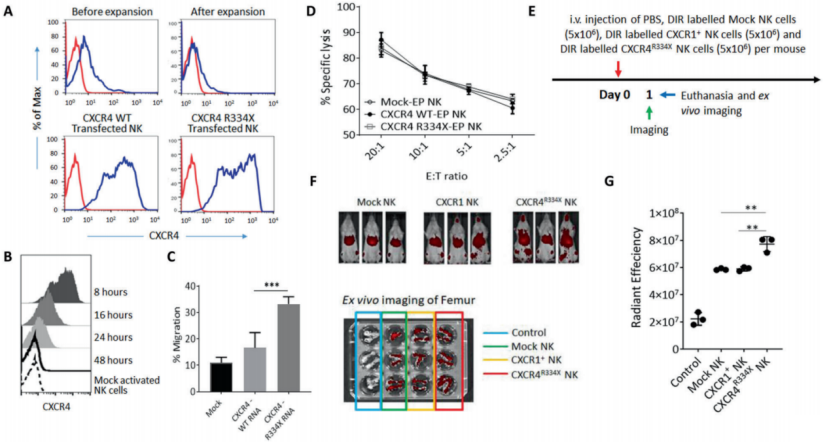
图1. 通过mRNA电穿孔过表达CXCR4R334X可提高NK细胞的迁移和归属能力.
为了测试CXCR4R334X修饰的NK细胞是否能更有效地迁移到NSG小鼠的骨髓隔室,作者将Dir(PerkinElmer)标记的NK模式细胞、CXCR1修饰的NK细胞或CXCR4R334X NK细胞注射到NSG小鼠尾静脉进行体内实验,结果表明在体外扩增的NK细胞上过表达CXCR4可有效促进其向骨髓迁移(图1E-G)。
02
两种抗BCMA CAR-NK细胞的比较
为了研究抗BCMA CAR-NK细胞对MM的影响,作者用两种第一代CARs得到了两种类型的抗BCMA CAR-NK细胞αBCMAz和αBCMAp(图2A),并实现了NK细胞的生存能力70-80%,其中约90%的NK细胞被转染表达CARs(图2B)。此外,作者发现αBCMAp NK细胞,αBCMAp NK细胞表面CAR表达的下调速度比αBCMAz NK细胞快(图2C)。为了便于评估抗BCMA CAR-NK细胞,作者分析了细胞表面BCMA的表达,发现在三种MM细胞系KMS-11、KMS-18和U266上观察到BCMA的高水平表面表达,但在AML细胞系KG-1、CD14单核细胞和原代B细胞上观察不到BCMA的表达(图2D)。
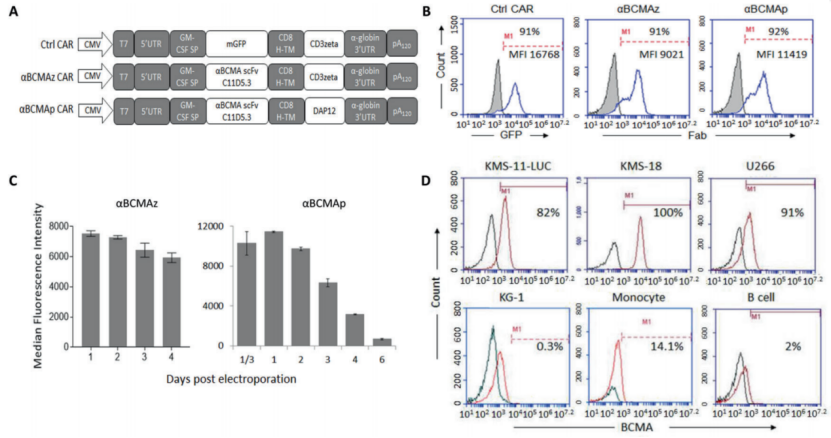
图2. anti-BCMA mRNA CAR在NK细胞上的表达及BCMA在不同肿瘤细胞和原代细胞上的表达.
作者进一步研究了MM细胞系激活CAR-NK细胞后IFN-γ的释放和脱颗粒作用,结果表明与Ctrl CAR-NK细胞相比,αBCMAz和αBCMAp NK细胞被检测的MM细胞系显著激活,而AML KG-1细胞系则没有,并且两种CAR-NK细胞之间没有统计学上的显著差异(图3A)。另外KMS-11和KMS-18细胞激活后,αBCMAz NK细胞的脱颗粒水平略高于αBCMAp NK细胞,(图3B)。作者进一步进行细胞毒性实验,用EuTDA试剂盒(PerkinElmer)比较αBCMAz和αBCMAp NK细胞对MM细胞系的细胞裂解能力,观察到两者之间没有明显差异,但均比ctrl CAR-NK细胞更有效。以KG-1细胞、原代B细胞或CD14单核细胞为靶细胞时,两种CAR-NK细胞的细胞裂解活性均较低或无裂解活性(图3C)。
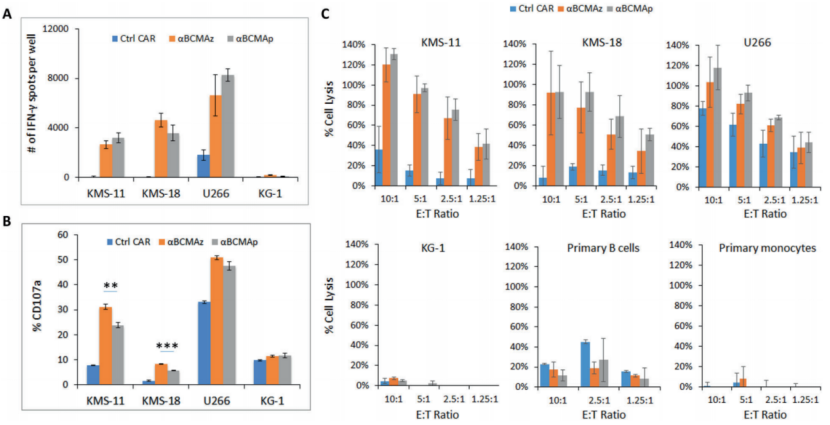
图3. 体外抗BCMA CAR-NK细胞对MM细胞系KMS-11、KMS-18和U266的活性。
03
CXCR4R334X与抗BCMA CAR在NK细胞上的共表达改善MM生长控制
作者以αBCMAz NK细胞进行后续实验,将CXCR4R334X和抗BCMA CAR共电孔植入NK细胞,以研究它们对MM的作用。作者检测了BCMA CAR(使用抗小鼠Fab抗体)和CXCR4的共表达,并观察到大约82%的修饰NK细胞共表达这两种分子(图4A)。证实CXCR4R334X可以有效地增强共转染的NK细胞向含有CXCL12的培养基的迁移(图4B)。且CXCR4的表达不影响抗BCMA CAR-NK细胞对靶肿瘤细胞株KMS-11的裂解活性(图4C)。
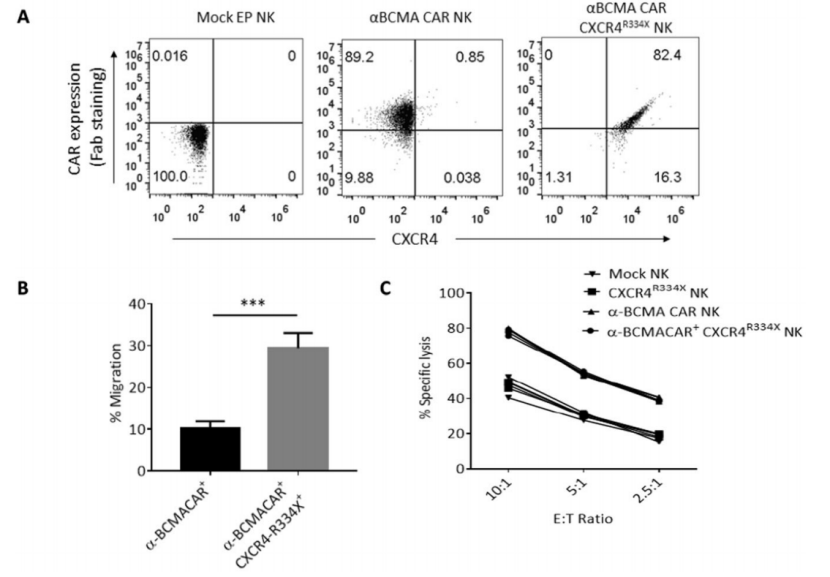
图4. BCMA CAR修饰、CXCR4过表达NK细胞的体外功能.
作者通过体内生物荧光成像(BLI)监测发现,与其他三组小鼠相比,用共表达CXCR4R334X和抗BCMA CAR的NK细胞处理的小鼠表现出明显的MM异种移植生长减慢(图5B)。另外mGFP CAR-NK细胞处理小鼠与anti-BCMA CAR-NK细胞处理小鼠的肿瘤负荷总通量值有统计学差异;NK细胞共同表达CXCR4R334X和anti-BCMA CAR的处理进一步降低了通量值(图5C)。作者对股骨区域的生物发光信号进行了特定的定量分析(图5D)发现,在抗bcma CAR-NK细胞中包含CXCR4R334X可减少MM异种移植的体内进展。用共表达CXCR4R334X和抗BCMA CAR的NK细胞处理的MM细胞接种小鼠的生存期显著延长(图5E)。这些结果表明,CXCR4R334X介导的骨髓浸润能很好地提高抗BCMA CAR-NK细胞对MM的根除效果。
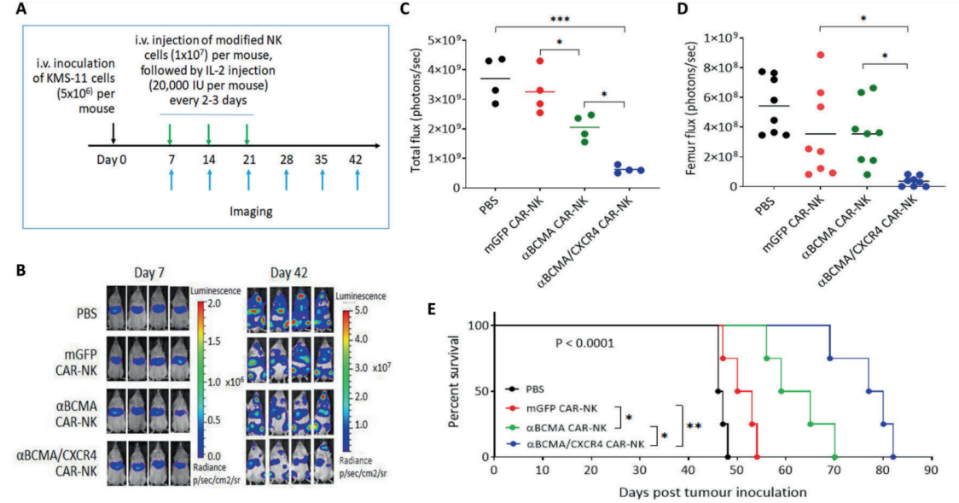
图5. BMCA CAR修饰过表达CXCR4R334X的NK细胞对MM生长的体内控制.
参考文献:
Ng YY, Du Z, Zhang X, et al.. CXCR4 and anti-BCMA CAR co-modified natural killer cells suppress multiple myeloma progression in a xenograft mouse model. Cancer Gene Ther. 2022 May; 29(5): 475-483.
来源于优宁维药物研发官网

